Автор обзора Наталья Генш
За последние годы отмечается существенное улучшение исходов инфаркта миокарда (ИМ), включая снижение внутригоспитальной и годичной смертности, что, по мнению экспертов, напрямую связано с повышением качества лечения, в том числе с проведением оптимальной фармакотерапии в острой фазе ИМ [1]. Неизменным компонентом медикаментозной терапии ИМ являются ингибиторы ангиотензин-превращающего фермента (ИАПФ), которые через влияние на активность нейрогуморальных систем, нормализацию гемодинамики, предотвращение ремоделирования миокарда и развития дисфункции левого желудочка (ЛЖ) уменьшают летальность в госпитальном периоде острого ИМ и увеличивают выживаемость постинфарктных больных в отдаленные периоды заболевания. Учитывая положительное влияние на исходы, европейское и северо-американское кардиологические сообщества рекомендуют применение ИАПФ при остром ИМ у больных высокого риска (с передней локализацией ИМ, сердечной недостаточностью (СН) или дисфункцией ЛЖ [класс рекомендаций I]) и считают целесообразным назначение этой группы лекарственных средств у всех остальных больных при отсутствии противопоказаний (класс рекомендации IIа) [1, 2]. Традиционно в руководствах указана лишь фармакологическая группа препаратов, что позволяет предполагать равнозначную эффективность и безопасность всех представителей ИАПФ у больных с острым ИМ. Тем не менее, ИАПФ — довольно разнородный класс, и его представители в значительной мере отличаются друг от друга по структуре и свойствам, что необходимо учитывать при выборе препарата в конкретной клинической ситуации. Среди современных представителей ИАПФ наибольшим потенциалом положительного воздействия на течение и исходы ИМ обладает зофеноприл. Отличительные черты зофеноприла и важнейшие доказательства его эффективности и безопасности при остром ИМ представлены в настоящем обзоре.
Особенности строения и механизма действия зофеноприла
Зофеноприл — представитель нового поколения ИАПФ. Он является пролекарством и в результате гидролиза преобразуется в активную форму препарата — зофеноприлат. Зофеноприл не только влияет на уровень АД, но и обладает целым рядом дополнительных эффектов, отличающих его от других ИАПФ [3] и связанных с высокой липофильностью и высокой тканевой аффинностью препарата, а также с наличием в его структуре двух сульфгидрильных (SН) групп.
SH-группа. Зофеноприл является единственным представителем класса ИАПФ, в химической структуре которого содержатся две SH-группы. Каптоприл, близкий по строению к зофеноприлу, обладает лишь одной сульфгидрильной группой, что, по-видимому, объясняет существующее различие в мощности антиоксидантных эффектов обоих препаратов. Эта структурная особенность определяет ряд плейотропных свойств зофеноприла, включая антиоксидантный, антиишемический, противовоспалительный и антиатерогенный эффекты, а также участие в восстановлении функции эндотелия (через стимуляцию высвобождения, торможение инактивации и потенцирование активности оксида азота) и чувствительности тканей к нитратам [4-6]. По данным исследований антиоксидантные возможности зофеноприла связаны со способностью нейтрализовать активные формы кислорода и другие виды свободных радикалов — этот эффект проявляется при клинически достижимой тканевой концентрации препарата и вносит весомый вклад в кардио- и вазопротекцию [3, 7, 8]. Наличие в структуре зофеноприла сульфгидрильной группы также определяет способность препарата открывать АТФ-зависимые калиевые каналы [6], что в условиях ишемии миокарда приводит к активации внутриклеточных адаптивных процессов, более экономному потреблению энергии, защите клеток от повреждения, повышению жизнеспособности кардиомиоцитов и уменьшению размеров зоны инфаркта — то есть к развитию кардиопротекторного эффекта [9]. Показано, что на фоне действия зофеноприла происходит улучшение коронарного кровотока и сократительной функции ЛЖ, уменьшается электрическая нестабильность миокарда [10] и снижается риск фатальных желудочковых тахиаритмий [11]. Перечисленные возможности зофеноприла значительно превышают защитные эффекты несульфгидрильных ИАПФ.
Липофильность. Зофеноприл отличается высокой липофильностью и входит в тройку самых липофильных ИАПФ (фозиноприл, зофеноприл, трандолаприл). Благодаря этому свойству препарат легко проникает в органы и ткани, где эффективно подавляет чрезмерную активность локальных ренин-ангиотензиновых систем (РАС). Блокируя тканевые АПФ, расположенные на мембране эндотелиальных и гладкомышечных клеток, зофеноприл реализует органопротекторный эффект [12], что в условиях миокардиальной ишемии способствует улучшению коронарного кровотока, угнетению клеточной гипертрофии и патологического ремоделирования миокарда [13-15].
Высокая тканевая аффинность. Еще одним отличием зофеноприла является самое высокое среди существующих ИАПФ сродство к тканям миокарда, а также более избирательное, выраженное и продолжительное взаимодействие активного метаболита с миокардиальными АПФ. Именно благодаря высокой аффинности препарата к тканевым АПФ миокарда снижение активности фермента в тканях сердца на 70-90% сохраняется в течение 24 ч, несмотря на довольно короткий период полужизни зофеноприлата, циркулирующего в крови (5,5 ч) [16, 17]. Немаловажно, что в миокард поступает не только фармакологически активный зофеноприлат, но и пролекарство зофеноприл, который уже в тканях сердца местно гидролизуется в активный метаболит. Этот феномен открывает возможность для внутриклеточной активности препарата и еще более усиливает его защитный эффект [18].
Клиническое значение тканевой аффинности зависит от характера сердечно-сосудистой патологии, ставшей показанием к назначению ИАПФ: играющее лишь вспомогательную роль в условиях неосложненной АГ (клиническая значимость в исследованиях не доказана) высокое сродство к миокардиальным АПФ, свойственное зофеноприлу, приобретает решающее значение при ИМ и других формах ишемической болезни сердца (ИБС). Подтверждение этой зависимости было получено в клинических исследованиях проекта SMILE (Survival of Miocardial Infarction Long-term Evalution), в которых именно высокая тканевая аффинность зофеноприла в сочетании с антиоксидантными свойствами и антиишемическим эффектом определила положительный эффект лечения, отмеченный в различных подгруппах больных с острым ИМ [19-22].
Эффективность и безопасность зофеноприла у больных с острым ИМ - проект SMILE
Проект SMILE стал логическим продолжением более ранних исследований, направленных на изучение возможностей ИАПФ в условиях острого ИМ и поиск оптимальной стратегии назначения этой группы препаратов. Эта исследовательская программа включила четыре клинических исследования, проведенных с целью изучения эффективности и безопасности зофеноприла у различных категорий больных с острым ИМ (табл. 1). В двух исследованиях (SMILE-1 и 2) изучались возможности непродолжительной (6 нед) терапии зофеноприлом, начатой в течение суток после развития ИМ. В третьем (SMILE- ISCHEMIA) - оценивался антиишемический эффект 6-месячной терапии, назначенной в среднем через 6 нед после развития острого ИМ; в SMILE-4 зофеноприл назначался на протяжении суток после развития ИМ и принимался в течение года вместе с препаратом ацетилсалициловой кислоты (АСК). Все исследования проекта SMILE были рандомизированными, двойными слепыми, многоцентровыми программами; исследования SMILE-1 и SMILE- ISCHEMIA контролировались плацебо, в SMILE-2 и 4 применялись активные компараторы лизиноприл и рамиприл. Краткое описание дизайна и наиболее важных результатов исследований SMILE представлено ниже.

В SMILE-1 [19] оценивались эффекты 6-недельной терапии зофеноприлом и влияние препарата на кратковременные и долгосрочные исходы у больных с острым передним ИМ. В исследовании приняли участие 1556 пациентов в возрасте от 18 до 80 лет с передним ИМ, развившимся в течение 24 ч до рандомизации, по разным причинам не получившие терапию тромболитическими препаратами. Участники исследования были случайно распределены в группу плацебо (n=784) или группу зофеноприла (n=772 пациентов). Начальная доза зофеноприла составила 7,5 мг дважды с интервалом 12 ч, после чего доза постепенно удваивалась до целевого уровня 30 мг два раза в день, если позволяло систолическое АД (САД — не менее 100 мм рт. ст.) и отсутствовали симптомы гипотензии. Исследуемая терапия продолжалась в течение 6 нед, после чего начинался период последующего наблюдения продолжительностью 48±4 нед, в течение которого больные получали стандартное лечение. После завершения 6-недельного периода лечения оценивалась первичная конечная точка исследования, включавшая случаи смерти и развития тяжелой застойной СН; через год после развития ИМ оценивался уровень выживаемости в исследуемых группах.
Частота случаев смерти или тяжелой застойной СН за 6 нед лечения была снижена в группе зофеноприла (7,1%) по сравнению с группой плацебо (10,6%); совокупное снижение риска смерти или тяжелой застойной СН составило 34% (95% доверительный интервал 8-54%, р=0,018). Оценка отдельных компонентов первичной конечной точки показала достоверное снижение риска застойной СН (- 46%,95% ДИ 11-71%, р=0,018) и статистически незначимое влияние на риск смерти (-25%, 95% ДИ 11-60%, р=0,19) (рис. 1).
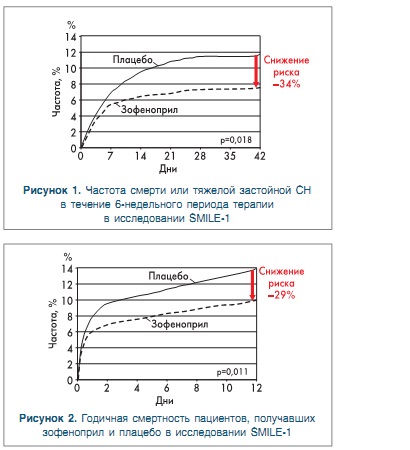
Через год наблюдения уровень смертности был достоверно ниже в группе зофеноприла (10%), чем в группе плацебо (14,1%); снижение риска смерти составило 29% (95% ДИ 6-51%, р=0,011) (рис. 2). Таким образом, 6-недельная терапия зофеноприлом, начатая в первые сутки после развития острого ИМ, обеспечила значительное улучшение кратковременных и долгосрочных исходов. Полученный длительный и устойчивый положительный эффект непродолжительного курса терапии было решено связать с защитным воздействием препарата и блокадой негативных влияний нейрогуморальной активации [23-27]. По результатам исследования был сделан вывод о целесообразности применения стратегии раннего назначения ИАПФ у больных с ИМ группы высокого риска, особенно у пациентов с обширным передним ИМ. Следует отметить благоприятный профиль безопасности зофеноприла у исследуемой категории больных — частота отмены лечения из-за тяжелой или симптоматической гипотензии (САД менее 90 мм рт. ст.) и частота развития гипотензии на фоне приема первой дозы препарата были сопоставимы у пациентов, получавших зофеноприл и плацебо (3,8 га 2,7% и 0,6 га 0,3% соответственно) [19]. Нельзя обойти вниманием тот факт, что влияние непродолжительной терапии зофеноприлом на риск ранней смерти больных с острым ИМ (снижение риска на 25%) значительно превышало аналогичные эффекты каптоприла (исследование 1818-4, снижение риска смерти на 7%) и лизиноприла (исследование GI88I-3, снижение риска смерти на 11%) и значимо коррелировало с высокой аффинностью зофеноприла к миокардиальным ИАПФ [18, 28, 29]. Ретроспективный анализ результатов исследования 8М1ЬЕ-1, проведенный для оценки влияния артериальной гипертензии (АГ) на клиническую эффективность ранней терапии зофеноприлом у пациентов с передним ИМ, показал наличие эффекта ИАПФ только у больных с сопутствующей АГ (рис. 3) [30].
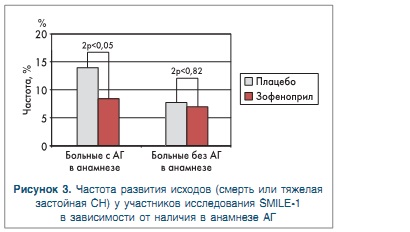
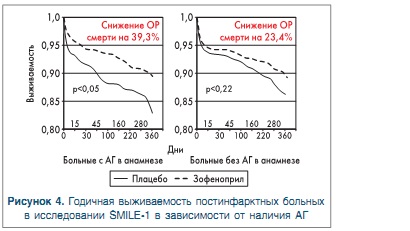
В подгруппе больных с АГ, получавших зофеноприл, относительный риск смерти и тяжелой застойной СН в течение 6 нед лечения снизился на 40% (относительный риск 0,60, 95% ДИ 0,45-0,81; двусторонний р<0,05), через год наблюдения относительный риск смерти был снижен на 39,3% (ОР 0,61 95% ДИ 0,23-0,89; двусторонний р<0,05). В подгруппе пациентов, не имевших в анамнезе АГ, показатели ОР для комбинации смерть + застойная СН в течение 6 нед и смерти в течение года составили 0,89 (95% ДИ 0,74-1,08; двусторонний р=0,62; снижение ОР на 11%) и 0,77 (95% ДИ 0,52-1,17; двусторонний р=0,22; снижение ОР на 23,4%) соответственно (рис. 4) (несмотря на тенденцию к улучшению 6-недельной и годичной выживаемости, изменения, отражающие уровень смертности, не достигли статистической значимости). Возможным объяснением подобного влияния зофеноприла на исходы ИМ у больных с АГ было названо предупреждение негативного воздействия подъемов АД на ремоделирование миокарда и развитие дисфункции ЛЖ [30]. Вторым этапом проекта SMILE стало исследование SMILE-2 [20], сравнивавшее эффективность и безопасность зофеноприла и лизиноприла у пациентов с острым ИМ различной локализации, получивших внутривенную тромболитическую терапию (n=1024).
Целью этого исследования была оценка способности различных по структуре и свойствам препаратов вызывать развитие тяжелой артериальной гипотензии. ставшей причиной неудовлетворительных результатов раннего применения ИАПФ при ИМ в некоторых предыдущих исследованиях. Пациенты в возрасте 18-75 лет были рандомизированы на пероральный прием зофеноприла (60 мг/сут) или лизиноприла (10 мг/сут); прием ИАПФ начинался через 1,5-12 ч после завершения тромболитической терапии и продолжался в течение 6 нед (первоначальные дозы составили 7,5 мг 2 раза в день для зофеноприла и 2,5 мг/сут — для лизиноприла с последующим титрованием дозы до целевого уровня). Первичной конечной точкой исследования была частота тяжелой артериальной гипотензии (САД менее 90 мм рт. ст.), общая или связанная с исследуемым лечением. Вторичные конечные точки включали следующие показатели: уровень общей смертности через 6 нед, частота тяжелой СН, фракция выброса (ФВ) ЛЖ, частота проведения экстренной коронарной реваскуляризации, частота развития стенокардии, частота повторного ИМ и доля пациентов с ухудшением функции почек.
Общая частота тяжелой гипотензии была несколько меньшей в группе зофеноприла по сравнению с группой лизиноприла (10,9 vs 11,7%, двусторонний р=0,38, разница статистически не значима). В то же время разница в частоте тяжелой гипотензии, связанной с приемом исследуемого препарата, была статистически значимой в пользу группы, получавшей зофеноприл (6,7 vs 9,8%, двусторонний р=0,048). Результат сравнения показателей, отражавших частоту развития тяжелой гипотензии в течение первых 48 ч лечения, также свидетельствовал о преимуществе зофеноприла (3,2 vs 5,8% в группе лизиноприла, двусторонний р=0,031) и отражал высокую безопасность препарата в первые дни после госпитализации по поводу ИМ, в период наивысшего риска дестабилизации гемодинамики и развития побочных эффектов ИАПФ [31].
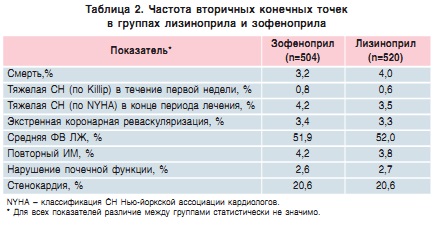
Уровень смертности за 6 нед лечения составил 3,2 и 4,0% в группах зофеноприла и лизиноприла соответственно (снижение смертности в группе зофеноприла — на 20%) — это различие не достигло статистической значимости (р=0,38) из-за недостаточной мощности исследования. Разница в частоте развития серьезных сердечнососудистых осложнений и других вторичных конечных точек исследования была статистически не достоверной (табл. 2) [20].
Преждевременно прекратили лечение 22,4 и 24,8% пациентов, получавших зофеноприл и лизиноприл соответственно. Тяжелая гипотензия была наиболее частой причиной прекращения терапии в обеих группах, зарегистрированной в 9,9 и 11,3% случаев соответственно. Таким образом, было показано, что зофеноприл и лизиноприл являются безопасными препаратами, применение которых при ИМ ассоциируется с низкой частотой развития тяжелой артериальной гипотензии. Благоприятный профиль безопасности исследуемых препаратов авторы SMILE-2 связали с постепенным увеличением используемых доз, что предотвратило активную блокаду РАС в острой фазе ИМ и повысило степень контроля АД. Небольшое, но значительное преимущество зофеноприла в отношении развития тяжелой гипотензии объяснялось более коротким периодом полувыведения препарата — эта фармакокинетическая особенность улучшила переносимость терапии и снизила риск гипотонических осложнений во время острой фазы ИМ [20, 32].
Результаты исследования SMILE-2 расширяют выводы, сделанные по завершении исследования SMILE-1, подтверждая хорошую переносимость зофеноприла больными с ИМ различной локализации при назначении ИАПФ в течение 24 ч с момента развития симптомов острого ИМ с условием постепенного увеличения дозы препарата. Результаты обоих исследований поддерживают применение ИАПФ, в частности зофеноприла, с адекватным титрованием дозы (во избежание тяжелой гипотензии) во время острой фазы ИМ.
Следующим этапом проекта SMILE стало изучение эффектов долгосрочной терапии зофеноприлом у пациентов с сохранной функцией ЛЖ (ФВ ЛЖ более 40%), не имеющих других показаний к назначению ИАПФ, кроме недавно перенесенного ИМ. Этой цели было посвящено исследование SMILE-ISHEMIA [21], включившее 349 постинфарктных больных (среднее время от развития ИМ до рандомизации 44±1 день). На основании результатов рандомизации пациенты получали либо зофеноприл (3060 мг/сут, n=177), либо плацебо (n=172) в течение 6 мес. Начальная доза зофеноприла составляла 7,5 мг 2 раза в день и постепенно повышалась до 30 мг 2 раза в день, если позволяло САД (более 100 мм рт. ст.) и не было симптомов артериальной гипотонии. Первичной комбинированной конечной точкой было любое клинически значимое проявление ишемии, включая появление значительных патологических изменений сегмента ST-T во время амбулаторного суточного мониторирования ЭКГ (СМ ЭКГ), развитие приступа стенокардии или появление отклонений на ЭКГ во время стандартного нагрузочного теста, развитие повторного ИМ и возникновение показаний для коронарной реваскуляризации. Вторичная конечная точка должна была оценить влияние зофеноприла на вероятность развития каждого явления из комбинированной первичной конечной точки и любого серьезного сердечно-сосудистого события, включая летальный исход.
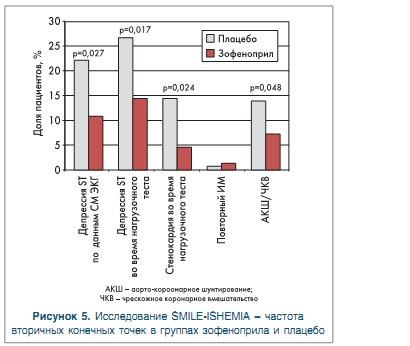
Частота первичной конечной точки составила 20,3% в группе зофеноприла и 35,9% — в группе плацебо (р=0,001) в отсутствие различий между группами по уровням АД, ФВ ЛЖ и характеру сопутствующей терапии на конец исследования. За время СМ ЭКГ депрессия сегмента 8Т-Т была зарегистрирована у 22,2 и 10,7% пациентов в группах плацебо и зофеноприла соответственно (р=0,027); депрессия сегмента 8Т-Т в ответ на нагрузочный тест — у 18,4 и 9,9% пациентов соответственно (р=0,024). При этом глубина депрессий 8Т-Т и их средняя продолжительность были значительно меньшими в группе зофеноприла. Также в группе зофенопри- ла была меньшей частота жалоб на стенокардию (3,3 га 9,9% в группе плацебо; р=0,017) и частота серьезных желудочковых аритмий (2,7 га 7,2%; р=0,048), был зарегистрирован более низкий уровень основных сердечно-сосудистых событий (4,5 га 12,7% в группе плацебо, р=0,041), а также меньшая частота развития и прогрессирования хронической СН. Частота развития побочных эффектов в группах зофеноприла и плацебо была сопоставимой. Таким образом. в исследовании SMILE-ISCHEMIA зофеноприл достоверно снижал частоту и выраженность эпизодов спонтанной и индуцированной ишемии миокарда, одновременно уменьшая риск основных неблагоприятных сердечно-сосудистых событий. Обнаруженный антиишемический эффект препарата не зависел от его антигипертензивного влияния. воздействия на функцию ЛЖ и сопутствующие заболевания и, предположительно, был связан с плейотропными возможностями зофеноприла. SMILE-ISCHEMIA стало первым исследованием, в котором была продемонстрирована эффективность ИАПФ у пациентов с относительно низким риском. предшествующим ИМ и хронической ИБС без дисфункции ЛЖ и АГ. Результаты этого исследования дополняют данные, полученные в других исследованиях проекта SMILE, и расширяют возможные показания к применению зофеноприла с целью предотвращения сердечно-сосудистых событий, включая ранний и поздний период после перенесенного ИМ [21].
Последним исследованием в рамках проекта SMILE стало исследование SMILE-4 [22] по сравнению безопасности и эффективности зофеноприла (60 мг/сут) и рами- прила (10 мг/сут), назначаемых в комбинации с АСК (100 мг/сут), у пациентов (n=771) с дисфункцией ЛЖ (клинические признаки СН или ФВ ЛЖ <45%) на фоне острого ИМ. В основу этого исследования легло представление о том, что положительные эффекты ИАПФ, связанные с увеличением синтеза вазодилатирующих простагландинов (простациклина и простагландина E2), могут блокироваться одновременным назначением препаратов АСК. Была выдвинута гипотеза, согласно которой зофеноприл и рамиприл в связи с различием их фармакологических свойств по-разному взаимодействуют с АСК, различным образом воздействуя на заболеваемость и смертность кардиологических больных.
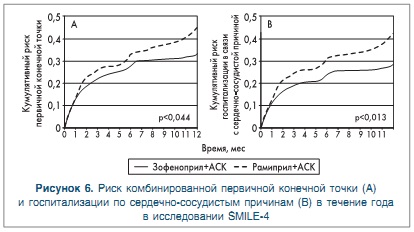
Пациенты (возраст 18-85 лет) включались в исследование в течение 24 ч после развития острого ИМ; на протяжении первых 4 дней все участники (из этических соображений) получали зофеноприл в нарастающей дозе, на пятый день пациенты были рандомизированы в соотношении 1:1 на прием зофеноприла в дозе 30 мг 2 раза в сутки или рамиприла в дозе 5 мг 2 раза в сутки в течение 12 мес. Начиная с первого дня ИМ, все пациенты получали АСК в дозе 100 мг/сут. Первичная комбинированная конечная точка исследования включала сердечно-сосудистую смерть и госпитализацию в связи с сердечно-сосудистой причиной в течение периода терапии.
За период лечения первичная конечная точка была зарегистрирована у 37% пациентов в группе рамиприла и у 29% — в группе зофеноприла: терапия зофеноприлом, таким образом, ассоциировалась со значимым 30% снижением риска комбинированной конечной точки исследования (ОР 0.70. 95% ДИ 0.51-0.96. р=0.028). Частота госпитализации в связи с сердечно-сосудистой причиной была значительно (на 35%) снижена у пациентов из группы зофеноприла в сравнении с больными из группы рамиприла (24 vs 33%. ОР 0.64. 95% ДИ 0.46-0.88. p=0.006). Показатель. отражавший частоту смерти от сердечно-сосудистых причин в течение года лечения, значительных различий между группами не имел (5 vs 3% в группах зофеноприла и рамиприла соответственно, ОР 1,51, 95% ДИ 0.70-3.27, р=0,293) (рис. 6).
Таким образом, у больных с дисфункцией ЛЖ на фоне острого ИМ эффективность комбинации зофеноприла и АСК превосходила эффективность комбинации рамиприла и АСК, при этом снижение частоты первичной конечной точки в группе зофеноприла достигалось в основном снижением частоты госпитализаций в связи с сердечно-сосудистой причиной. Этот результат, по мнению авторов исследования, может означать, что клинический эффект сульфгидрильных ИАПФ лишь частично связан с простагландин- опосредованными процессами, зависящими от индометацина или АСК, и в значительной степени реализуется через иные механизмы [22].
Результаты вышеприведенных исследований были суммированы и проанализированы в сводном анализе SMILE-overall [33], основной целью которого была оценка кумулятивной эффективности зофеноприла у 3630 пациентов с ИБС, принявших участие в исследованиях проекта SMILE. Все полученные данные были рассмотрены в совокупности для оценки влияния зофеноприла на годичную сердечно-сосудистую смертность и заболеваемость в сравнении с плацебо или активными компараторами (лизиноприл, рамиприл). Вторичной целью анализа была оценка влияния зофеноприла на различные подгруппы пациентов, выделяемые с учетом 1) демографических характеристик, 2) контрольного препарата, 3) типа исхода, 4) причины смерти, 5) уровня ФВ ЛЖ, 6) частоты госпитализации и 7) сопутствующего лечения.
Результаты анализа показали, что применение зофеноприла ассоциировалось со значительным снижением уровня сердечно-сосудистой смертности по сравнению с плацебо (ОР 0,42, 95% ДИ 0,32-0,56) при отсутствии достоверных различий между зофеноприлом и другими сравниваемыми ИАПФ. Общий уровень смертности и заболеваемости был достоверно снижен у пациентов, получавших зофеноприл, по сравнению с плацебо (р<0,001) и другими ИАПФ (р<0,001) в основном за счет более низкой частоты госпитализации в группах зофеноприла. Кроме того, срок выживаемости без развития нежелательных событий был значительно большим у пациентов, получавших зофеноприл, по сравнению с другими ИАПФ (10,4 мес, 95% ДИ 10,1-10,5 мес vs 8,9 мес, 95% ДИ 8,4-9,4 мес, р<0,0001) (рис. 7). Различия в исходах по подгруппам с учетом возраста, пола, анамнеза, уровня ФВ ЛЖ и сопутствующей терапии, выявлены не были.
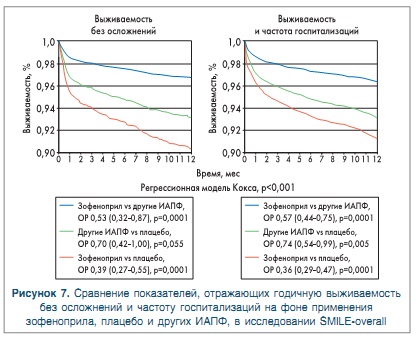
Таким образом, результаты анализа SMILE-overall подтвердили положительный эффект терапии зофеноприлом у пациентов с ИБС, перенесших острый ИМ. Снижение уровня смертности и заболеваемости, отмеченное в группе зофеноприла по сравнению с другими ИАПФ, поддерживает мнение о том, что структурные, физико-химические и фармакологические характеристики ИАПФ влияют на эффективность препаратов этой группы у больных с ИБС.
Таким образом, анализ результатов исследовательской программы SMILE позволяет заключить, что:
1. терапию постепенно нарастающими дозами зофеноприла следует начинать уже в первые сутки после развития ИМ — такая стратегия эффективна и безопасна;
2. зофеноприл может назначаться различным категориям больных с ИМ, но наибольшая польза достигается у больных из группы высокого риска (например, у больных с сопутствующей АГ);
3. применение зофеноприла с первых суток заболевания улучшает краткосрочные и долговременные исходы ИМ;
4. длительный (6-12 мес) прием зофеноприла у больных ИБС с сохраненной систолической функцией, перенесших ИМ от 1 до 6 нед назад, оказывает значительный антиишемический эффект и снижает риск развития нежелательных сердечно-сосудистых исходов;
5. зофеноприл, назначенный при ИБС, снижает уровень заболеваемости эффективнее других ИАПФ, отличных по строению и свойствам;
6. применение одновременно с АСК влияет на эффекты зофеноприла в меньшей степени, чем на эффекты других ИАПФ.
Благоприятные результаты проекта SMILE убедительно доказали эффективность и безопасность терапии зофеноприлом у пациентов с ИБС, в том числе в условиях острого ИМ. Полученные данные подчеркивают клиническую значимость внутриклассовых отличий ИАПФ и определяют важную роль зофеноприла в профилактике и лечении заболеваний сердечно-сосудистой системы.
Литература
1. 2013 ACCF/AHA Guideline for the Management of ST-Elevation Myocardial Infarction A Report of the Аmerican College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines. Circulation. 2013; 127.
2. ESC Guidelines for the management of acute myocardial infarction in patients presenting with ST-segment elevation. European Heart Journal2012; 33: 2569-2619.
3. Evangelista E., Manzini S. Antioxidant and Cardioprotective Properties of the Sulphydryl Angiotensinconverting Enzyme Inhibitor Zofenopril. The Journal of International Medical Research 2005; 33: 42-54.
4. Subissi A., Evangelista S., Giachetti A. Preclinical profile of zofenopril: an angiotensin converting enzyme inhibitor with peculiar cardioprotective properties. Cardiovascular Drug Review 1999; 17(2): 115-33.
5. Liu X., Engelman R., Rousou J. et al. Attenuation of myocardial reperfusion injury by sulfhydryl-containing angiotensin converting enzyme inhibitors. Cardiovasc Drugs Ther 1992; 6(4): 437-43.
6. Sargent C., Sleph P., Dzwonczyk S. et al. Cardioprotection in ischemic rat hearts with the SH-containing angiotensin-converting enzyme inhibitor zofenopril: possible involvement of the ATP-sensitive potassium channel. J Pharmacol Exp Ther 1993; 265(2): 609-18.
7. Mak I., Freedman A., Dickens B., Weglicki W. Protective effects of sulfhydryl-containing angiotensin converting enzyme inhibitors against free radical injury in endothelial cells. Biochem Pharmacol 1990; 40: 2169 - 2175
8. Cominacini L., Pasini A., Garbin U. et al: Zofenopril inhibits the expression of the adhesion molecules on endothelial cells by reducing reactive oxygen species. Am J Hypertens 2002; 15: 891 - 895.
9. Frascarelli S., Ghelardoni S., Ronca-Testoni .S, Zucchi R. Cardioprotective effect of zofenopril in perfused rat heart subjected to ischemia and reperfusion. J Cardiovasc Pharmacol 2004; 43: 294-299.
10. Tio R., de Langen C., de Graeff P. et al. The effects of oral pretreatment with zofenopril, an angiotensin-converting enzyme inhibitor, on early reperfusion and subsequent electrophysiologic stability in the pig. Cardiovasc Drugs Ther. 1990; 4(3): 695-703.
11. Grover G., Sleph P., Dzwonczyk S. et al/ Effects of different angiotensin-converting enzyme (ACE) inhibitors on ischemic isolated rat hearts: relationship between cardiac ACE inhibition and cardioprotection. J Pharmacol Exp Ther 1991; 257: 919-929.
12. Ranadive S., Chen A., Serajuddin A. Relative lipophilicities and structural-pharmacological considerations of various angiotensinconverting enzyme (ACE) inhibitors. Pharm Res. 1992; 9(11): 1480-6.
13. McDonald K., Garr M., Carlyle P. et al. Relative effects of alpha 1-adrenoceptor blockade, converting enzyme inhibitor therapy, and angiotensin II subtype 1 receptor blockade on ventricular remodeling in the dog. Circulation. 1994; 90(6): 3034-46.
14. Pinto Y., van Wijngaarden J., van Gilst W. et al. The effects of short- and long-term treatment with an ACE-inhibitor in rats with myocardial infarction. Basic Res Cardiol. 1991; 86 Suppl 1:165-72.
15. McDonald K., Carlyle P., Matthews J. et al: Early ventricular remodeling after myocardial damage and its attenuation by converting enzyme inhibition. Trans Assoc Am Physicians 1990; 103: 229-235.
16. Cushman D., Wang F., Fung W. et al. Comparisons in vitro, ex vivo, and in vivo of the the actions of seven structurally diverse inhibitors of angiotensin converting enzyme (ACE). - Brit. J. Clin. Pharmacol., 1989; 28 (suppl. 2): 115S-131S.
17. Cushman D., Wang F., Fung W. et al. Differentiation of angiotensin converting enzyme (ACE) inhibitors by selective inhibition of ACE in physiologically important target organs. - Amer. J. Hypertension, 1989; 2 (4): 294-306.
18. Преображенский Д.В., Сидоренко Б.А., Бугримова М.Аи др. Зофеноприл - кардиоселективный ингибитор ангиотензин- превращающего фермента: клиническая фармакология и использование при лечении сердечно-сосудистых заболеваний. Болезни сердца и сосудов. 2007 (4). http://www.con- silium-medicum.com/magazines/cm/medicum/article/15584
19. Borghi C.. Bacchelli S.. Esposti D. D.. et al.. on behalf of the SMILE study investigators. Effects of the early ACE inhibition in diabetic nonthrombolyzed patients with anterior acute myocardial infarction. - Diabetes Care. 2003; 26: 1862-1868.
20. Borghi C.. Ambrosioni E.. on behalf of the SMILE-2 working party. Double-blind comparison between zofenopril and lisinopril in patients with acute myocardial infarction: Results of the Survival of Myocardial Infarction Long-term Evaluation-2 (SMILE-2) study. - Am Heart J 2003; 145 (1): 80-87.
21. Borghi C.. Ambrosioni E.. on behalf of the SMILE-3 working party. Effects of zofenopril on ischemia following myocardial infarction: the SMILE-3 study. - AHA Scientific Session-2003; abstract 3129.
22. Borghi C.. Ambrosioni E. et al. Comparison Between Zofenopril and Ramipril in Combination With Acetylsalicylic Acid in Patients With Left Ventricular Systolic Dysfunction After Acute Myocardial Infarction: Results of a Randomized. Double-Blind. ParallelGroup. Multicenter. European Study (SMILE-4). Clin Cardiol 2012: 7; 416-423.
23. Graeff P.. van Gilst W.. Bel K. et al. Concentration-dependent protection by captopril against myocardial damage during ischemia and reperfusion in a closed chest pig model. J Cardiovasc Pharmacol 1987; 9: Suppl 2: S37-S42.
24. Sogaard P.. Nogaard A.. Gotzsche C-O. et al. Therapeutic effects of captopril on ischemia and dysfunction of the left ventricle after Q-wave and non-Q-wave myocardial infarction. Am Heart J 1994; 127: 1-7.
25. Przyklenk K.. Kloner R. Angiotensin converting enzyme inhibitors improve contractile function of stunned myocardium by different mechanisms of action. Am Heart J 1991; 121: 1319-30.
26. Tan L.. Jalil J.. Pick R. et al. Cardiac myocyte necrosis induced by angiotensin II. Circ Res 1991; 69: 1185-95.
27. Rouleau J.. de Champlain J.. Klein M. et al. Activation of neurohumoral systems in postinfarction left ventricular dysfunction. J Am Coll Cardiol 1993; 22: 390-8.
28. GISSI-3: effects of lisinopril and transdermal glyceryl trinitrate singly and together on 6-week mortality and ventricular function after acute myocardial infarction. Lancet 1994; 343: 1115-22.
29. ISIS-4 (Fourth International Study of Infarct Survival) Collaborative. A randomised factorial trial assessing early oral captopril. oral mononitrate. and intravenous magnesium sulphate in 58050 patients with suspected acute myocardial infarction. Lancet 1995; 345: 669-85.
30. Borghi C.. Bacchelli S.. Esposti D. D.. et al.. on behalf of the SMILE study investigators. Effects of the administration of an angiotensin-converting enzyme inhibitor during the acute myocardial infarction in patients with arterial hypertension. - Am J Hypert. 1999; 12: 665-672.
31. ACE Inhibitor Myocardial Infarction Collaborative Group. Indications for ACE inhibitors in the early treatment of acute myocardial infarction: systematic overview of individual data from 100.000 patients in randomized trials. Circulation 1998; 97: 2202-12.
32. DeForrest J.. Waldron T.. Krapcho J. et al. Preclinical pharmacology of zofenopril. an inhibitor of angiotensin II converting enzyme. J Cardiovasc Pharmacol 1989; 13: 887-94.
33. Borghi C. Cardioprotective role of ACE-I in patients with acute MI: THE SMILE -OVERALL PROJECT. JACC March 27. 2012: 59(13); abst.
Комментарий специалиста

В современном быстро меняющемся мире достаточно сложно остановить мгновенье, оглянуться вокруг, задуматься о сделанном, простить себя и получить прощение от других. Мы не успеваем... Похожая ситуация складывается и в профессиональной сфере. Выручает лишь то, что наши клинические достижения не столь уж стремительны (например, по сравнению с биомедицинскими дисциплинами, от которых мы отстали, похоже, навсегда). Итак, попытаемся оценить наши старые и новые знания о возможности современной терапии, направленной на снижение активности ренин-ангиотензин-альдостероновой системы (РААС) путем использования ингибиторов аннгиотензин-превращающего фермента (ИАПФ) у больных с некротическим повреждением сердца - инфарктом миокарда.
Любое повреждение организма вызывает ответную реакцию, направленную на восстановление былого физиологического равновесия и стимуляцию механизмов восстановления (репарации). В этой связи активация РААС является древнейшей филогенетической реакцией, направленной на выживание организма как при острой катастрофе (кровотечение, повреждение тканей), так и в условиях восстановления (активация коллагенообразования и фиброза, поддержание достаточного уровня перфузии жизненно важных органов, стимуляция гипертрофии мышечных волокон и т.д.). Почему же сегодня мы рассматриваем этот процесс как патологический и активно ищем способы его подавления? По-видимому, изменение среды обитания человека, его образа жизни привело к тому, что некогда защитные реакции организма в новых условиях становятся избыточными и мы имеем дело с их гиперактивацией, вызывающей формирование новых патологических кругов, участвующих в прогрессировании и хронизации болезни.
Если рассматривать проблему применения ИАПФ у больных острым инфарктом миокарда (ОИМ) в историческом контексте, стоит отметить, что начало использования препаратов этой группы приходится на 80-е годы прошлого столетия и связано с окончанием исследований каптопри- ла у больных с артериальной гипертензией и сердечной недостаточностью. Приятно отметить, что уже в начале 80-х годов сотрудники кафедры госпитальной терапии Киевского медицинского института одними из первых в СССР начали изучение эффективности каптоприла у больных ОИМ. В конце 80-х - начале 90-х годов появились результаты первых крупных рандомизированных плацебо-контролируе- мых слепых клинических исследований с участием больных ОИМ с дисфункцией левого желудочка (ЛЖ), которые продемонстрировали уменьшение прогрессирования процессов патологического ремоделирования ЛЖ, сердечной недостаточности и риска смерти при длительном наблюдении исследования SAVE (каптоприл) и SOLVD (эналаприл)). В дальнейшем позитивные результаты были получены при использовании рамиприла (AIRE) и трандолаприла (TRACE). Препараты назначались в разные сроки после развития ОИМ (чаще с 3 по 7-16 сутки) в связи с опасением развития нежелательной гипотензии у больных при совместном использовании ИАПФ с нитратами, диуретиками и β-блокаторами. Неблагоприятные последствия медикаментозной гипотензии были тогда же продемонстрированы в исследовании CONSENSUS, в котором больным в первые сутки заболевания назначали внутривенную форму эналаприла с последующим переходом на таблетированный препарат. В дальнейшем была проведена оценка результатов раннего назначения ИАПФ с первых суток ОИМ независимо от наличия дисфункции ЛЖ (GISSI III, ATLAS (лизиноприл), ISIS-4, Chinese (каптоприл)), которая подтвердила гипотезу о роли гиперактивации РААС в развитии неблагоприятных событий после перенесенного ОИМ. В этот же период (в середине 90-х годов) были получены результаты первого исследования SMILE. Его дизайн был построен по традиционной для того времени схеме с включением больных ОИМ с наибольшим риском развития и прогрессирования сердечной недостаточности - с передней локализацией поражения, без проведения реваскуляризации миокарда (больные включались в исследование в течение первых суток после развития ОИМ). Результатом исследования стало ожидаемое снижение риска развития комбинированной конечной точки (смерть+ застойная сердечная недостаточность) на 34% при отсутствии достоверного влияния на риск развития смерти (снижение на 25% было статистически недостоверным ввиду недостаточного числа включенных в исследование больных - 1556). Фактически, современные кардиологи всего мира используют рекомендации по лечению ОИМ, основанные на результатах анализов различных исследований, проведенных в конце прошлого столетия. Тот период ознаменовал огромный прорыв в кардиологии, позволивший внедрить ИАПФ в клиническую практику и спасти сотни тысяч жизней. В начале этого тысячелетия были проведены лишь отдельные исследования, расширившие показания к использованию ИАПФ после ОИМ, среди которых следует выделить PREAMI (периндоприл у больных пожилого возраста), FAMI (фозиноприл) и продолжение серии исследований SMILE с зофеноприлом. Почему исследователи продолжили изучение определенных ИАПФ? Это обусловлено нерешенными клиническими вопросами, появившимися в связи с накоплением знаний и опыта в отношении блокады РААС. Стало понятно, в связи с чем развивается дилатация полости ЛЖ, почему происходит прогрессирование сердечной недостаточности при ОИМ и каким образом внедрение методов реваскуляризации миокарда совместно с блокадой РААС (β-блокатор, ИАПФ, блокатор рецепторов альдосте-рона) способно предотвратить или уменьшить эти нежелательные последствия коронарной катастрофы. В то же время на фоне стремления к индивидуализированному лечению больных и понимания того, что классовый эффект препаратов может не сработать в условиях современной терапии, возникает потребность в более глубоком анализе фармакологических различий существующих ИАПФ и сравнении их эффективности. Именно этим клинически значимым задачам и были посвящены исследования ИАПФ, проведенные в XXI веке.
В обзоре отмечены уникальные особенности зофеноприла – высокая тканевая аффинность, связанная со способностью препарата растворяться в жирах (в отличие от водорастворимого каптоприла), и наличие в структуре сульфгидрильной группы (другие липофильные ИАПФ ее не имеют), которая обусловливает дополнительные антиоксидантные эффекты препарата. При этом показано, что зофеноприл, как и другие ИАПФ, обладает способностью предотвращать дилатацию полости ЛЖ и развитие застойной сердечной недостаточности после ОИМ, что можно рассматривать как опосредованное защитное действие на сердечно-сосудистую систему.
Итак, несколько слов о программе SMILE. Цель опубликованных в 2003 году исследований состояла в том, чтобы получить ответы на вопросы о безопасности применения ИАПФ после проведения фармакологической реваску- ляризации миокарда при помощи фибринолитических агентов (риск гипотензии, особенно на фоне стрептокиназы) через сравнение уже доказавших свою эффективность препаратов - лизиноприла и зофеноприла (SMILE-2), а также о наличии антиишемических свойств у зофеноприла (SMILE-3) при его назначении в более поздние сроки после перенесенного ОИМ (1-6 недель) у больных без абсолютных показаний к назначению ИАПФ (отсутствие дисфункции ЛЖ или сопутствующей артериальной гипертензии). Оказалось, что медленное увеличение дозы зофено- прила с 7,5 мг дважды в день до 30 мг дважды в день сопровождается меньшей частотой гипотензивных реакций, чем титрация лизиноприла с 2,5 мг до 10 мг в сутки. При этом по клиническому течению группы больных не различались. В исследовании по оценке антиишемического действия зофеноприла по сравнению с плацебо обнаружено достоверное уменьшение различных маркеров ишемии, по данным холтеровского мониторирования, нагрузочных тестов и показателям, отражающим потребность в ревас- куляризации. Полученные результаты вдохновили клиницистов на подготовку и проведение нового исследования по сравнению зофеноприла с рамиприлом, хорошо себя зарекомендовавшим у больных с ОИМ из группы высокого сосудистого риска в исследованиях AIRE и HOPE. Оба препарата имеют высокую тканевую аффинность, но в силу своих фармакологических особенностей могут по-разному взаимодействовать с малыми дозами ацетилсалициловой кислоты (АСК). Всем известна дискуссия середины 2000-х годов о возможной нивелировке эффекта ИАПФ при их сочетании с АСК, в том числе о негативном действии АСК при лечении сердечной недостаточности. Для поиска окончательного решения этой проблемы, крайне важного с практической точки зрения, и было проведено исследование SMILE-4, результаты которого опубликованы в 2012 году. Авторы показали, что назначение зофеноприла на фоне использования 100 мг АСК в первые 24 часа ОИМ у больных с дисфункцией ЛЖ и прием препарата на протяжении 12 месяцев по сравнению с рамиприлом (титрации доз соответственно до 60 мг и 10 мг в сутки) приводит к достоверному снижению конечной точки (смерть + повторные госпитализации) за счет уменьшения числа госпитализаций по сердечно-сосудистым причинам.
В заключение хотелось бы отметить, что к группе ИАПФ, доказавших свою эффективность у больных, перенесших ОИМ, добавился еще один препарат. И не только по данным литературных источников, но и в реальной клинической практике. Зофеноприл уже зарегистрирован и может использоваться клиницистами Украины. Показания для его назначения те же, что и для других ИАПФ после ОИМ - сердечная недостаточность, артериальная гипертензия и сахарный диабет. Но с позиции современных данных, показавших, что использование ИАПФ приносит пользу всем больным после ОИМ, возможности для применения препаратов этой группы расширяются. При этом следует помнить о максимальной пользе зофеноприла у больных с артериальной гипертензией, выраженном антиишемическом эффекте при отсутствии у пациента гипертензии и признаков сердечной недостаточности, лучшем профиле безопасности по сравнению с лизиноприлом и меньшем клинически значимом взаимодействии с АСК у больных на фоне дисфункции ЛЖ. Эти особенности создают предпосылки для новых возможностей при индивидуализации лечения больных с ОИМ и пациентов, перенесших коронарную катастрофу. Желаю всем удачи на этом пути!