Візір В.А., Волошина І.М.
Запорізький державний медичний університет, кафедра внутрішніх хвороб № 2
ЛЕРКАНІДИПІН: НОВІ АСПЕКТИ ПАТОГЕНЕТИЧНОГО ЛІКУВАННЯ У ХВОРИХ НА ГІПЕРТОНІЧНУ ХВОРОБУ
Резюме. Стаття присвячена оцінці впливу лерканідипіну на гемодинамічні та нейроімунологічні показники у хворих на гіпертонічну хворобу різного додаткового ризику та із супутнім ожирінням. Установлено, що тривале лікування лерканідипіном суттєво впливає на рівень артеріального тиску та здатність корегувати діастолічну дисфункцію лівого шлуночка. Лерканідипін реалізує свої ефекти завдяки збільшенню плазмового вмісту вазодилатуючого кальцитонін-ген-регулюючого пептиду.
Ключові слова: гіпертонічна хвороба, лерканідипін.
Вступ
Гіпертонічна хвороба (ГХ) є одним із найбільш поширених захворювань – кількість хворих, які страждають від АГ, у світі становить близько одного мільярда [2, 3]. Неконтрольована артеріальна гіпертензія (АГ) асоціюється з високим ризиком виникнення кардіоваскулярних, цереброваскулярних та ренальних ускладнень. Безсумнівними є факти достовірного зниження частоти цих ускладнень у пацієнтів з АГ, які ефективно лікуються [11]. Основними фармакологічними групами для лікування АГ є інгібітори ангіотензинперетворюючого ферменту (іАПФ), блокатори повільних кальцієвих каналів, діуретики, бета-блокатори та антагоністи рецепторів ангіотензину ІІ [2, 3]. У проведеному масштабному метааналізі не було встановлено суттєвих переваг однієї групи препаратів перед іншою щодо здатності знижувати артеріальний тиск (АТ), а в чинних вітчизняних та європейських рекомендаціях із лікування АГ вказується на необхідність враховувати ініціальний кардіоваскулярний ризик пацієнта та супутні захворювання при виборі антигіпертензивної терапії [2, 3, 7].
Незважаючи на накопичений досвід застосування антигіпертензивних препаратів та результати порівняльної ефективності різних фармакологічних чинників між собою, актуальним залишається вивчення нових властивостей препаратів та механізмів їх впливу на основні ланки патогенезу захворювання.
Одним із препаратів, що найбільш ефективно знижують АТ, є антагоніст кальцію лерканідипін [5, 9]. Його перевагами є висока ліпофільність, мембраноконтрольована фармакокінетика й один із найкращих профілів переносимості в класі [7]. Лерканідипін конкурентно зв’язується з дигідропіридиновими локусами кальцієвих каналів L-типу в гладком’язових клітинах судин і кардіоміоцитах, пригнічуючи трансмембранний потік іонів кальцію і сприяючи розслабленню гладкої мускулатури. Завдяки високій ліпофільності лерканідипін добре розчиняється в мембранних структурах і здатний накопичуватися всередині гідрофобного компартменту подвійного фосфоліпідного шару клітинних мембран. У ряді клінічних порівняльних досліджень продемонстрована висока антигіпертензивна ефективність лерканідипіну [7]. Була виявлена тотожна антигіпертензивна ефективність лерканідипіну в добовій дозі 20 мг і амлодипіну в дозі 10 мг у подвійному сліпому перехресному дослідженні хворих на АГ 1-2-го ступеня [6]. На сьогодні бракує міжнародних рандомізованих багатоцентрових досліджень із вивчення антигіпертензивної дії лерканідипіну та його здатності зменшувати ступінь ризику серцево-судинних ускладнень у хворих на гіпертонічну хворобу. Актуальним залишається вивчення впливу препарату на гемодинамічні та нейроімунологічні показники.
Метою дослідження стала оцінка впливу лерканідипіну на гемодинамічні та нейроімунологічні показники у хворих на гіпертонічну хворобу різного додаткового ступеня ризику.
Матеріал та методи дослідження
Обстежені 44 пацієнти (25 чоловіків, 19 жінок; віком 40—68 років, середній вік 57,0 ± 3,5 року) із ГХ ІІ (22 особи) та ІІІ стадій (22 особи) згідно з рекомендаціями Української асоціації кардіологів [3]. Контрольну групу становили 20 практично здорових нормотензивних пацієнтів (11 чоловіків, 9 жінок) віком 37–57 років, середній вік 50,0 ± 4,1 року.
 Критерії включення хворих у дослідження: установлений діагноз ГХ ІІ або ІІІ стадії, наявність перенесеного ішемічного інсульту давністю більше ніж 1 рік (у випадку ГХ III стадії), вік хворих більше ніж 18 років, синусовий ритм серця, згода на участь у дослідженні. Критерії виключення: наявність симптоматичних артеріальних гіпертензій, серцева недостатність III—IV функціонального класу за NYHA, цукровий діабет, гострий коронарний синдром в анамнезі давністю менше ніж 6 місяців, фракція викиду лівого шлуночка < 45 %, тяжка ниркова та печінкова недостатність.
Критерії включення хворих у дослідження: установлений діагноз ГХ ІІ або ІІІ стадії, наявність перенесеного ішемічного інсульту давністю більше ніж 1 рік (у випадку ГХ III стадії), вік хворих більше ніж 18 років, синусовий ритм серця, згода на участь у дослідженні. Критерії виключення: наявність симптоматичних артеріальних гіпертензій, серцева недостатність III—IV функціонального класу за NYHA, цукровий діабет, гострий коронарний синдром в анамнезі давністю менше ніж 6 місяців, фракція викиду лівого шлуночка < 45 %, тяжка ниркова та печінкова недостатність.
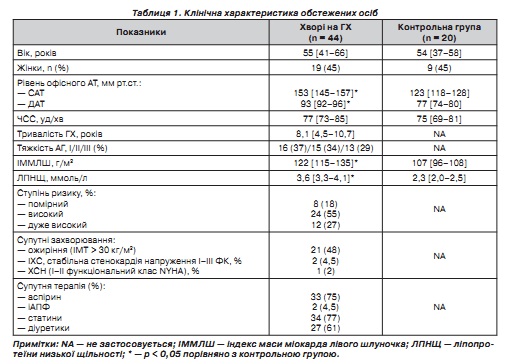
Параметри гемодинаміки визначали за допомогою вимірювання клінічного АТ, дуплексної ехокардіографії для визначення структурно-функціональних змін серця. Нейроімунологічні показники — плазмовий рівень нейропептиду Y (NPY), норадреналіну, кальцитонін-ген-регулюючого пептиду (КГРП), трансформуючого фактора росту β1 (ТФР-β1) та концентрацію інтерлейкінів-6, -10 (ІЛ) – визначали на базі центральної науково-дослідної лабораторії ЗДМУ за допомогою імуноферментного аналізу з використанням реактивів Peninsula (Велика Британія), IBL (Німеччина), Invitrogen (США), ЗАТ «Вектор- Бест» (Росія) відповідно. Усі показники, що вивчалися, були визначені двічі: до початку лікування та через 1 рік. Лерканідипін (Леркамен®, «Берлін-Хемі АГ») призначався в дозі 10—20 мг на добу per os. Клінічна характеристика обстежених осіб, супутні захворювання і терапія наведені в табл. 1. Як видно з даних табл. 1, обидві групи були порівнянними між собою за віком та статтю. Привертає увагу велика кількість осіб із супутнім ожирінням.
Більшості хворих (75 %) було призначено аспірин та статини, що пов’язано з потребою корекції високого та дуже високого додаткового ризику в пацієнтів. Отримані результати представляли у вигляді середньої (M), похибки середньої (m) або 95% довірчого інтервалу. Внутрішньо- і міжгрупові відмінності оцінювали за допомогою двовибіркового Т-тесту або χ2-тесту залежно від виду даних у рамках програми StatPlus 2009. Статистично значущими вважали відмінності між показниками при відхиленні нульової гіпотези й рівні значущості p < 0,05 [1].
Результати та їх обговорення
Аналіз отриманих результатів показав, що на початку лікування хворі на ГХ значно відрізнялися за показниками кардіогемодинаміки та нейроімунологічним статусом від аналогічних значень у контрольній групі (табл. 2, 3). Рівень АТ, кількість хворих із діастолічною дисфункцією ЛШ, величини LAVI та ІММЛШ були значно більшими за аналогічні в нормотензивних осіб. Жоден хворий на ГХ не мав адекватного контролю АТ до лікування. Частота серцевих скорочень та фракція викиду ЛШ були порівнянними з показниками в контрольній групі. Протягом одного року антигіпертензивного лікування відбулися суттєві зміни показників, що вивчались, в обстежених осіб. Відзначено достовірне зниження рівня САТ і ДАТ на тлі прийому лерканідипіну. Через рік лікування в більшості хворих спостерігали адекватний контроль АТ. Частота верифікації діастолічної дисфункції ЛШ на тлі лікування зменшилася вдвічі (р < 0,05), про що додатково свідчило зменшення показника LAVI на 14 % (р < 0,05) у групі прийому лерканідипіну. Зазначені зміни кардіогемодинаміки на тлі лікування блокатором повільних кальцієвих каналів були реалізовані, очевидно, завдяки впливу на різні ланки патогенезу ГХ, що можна прослідкувати за динамікою нейроімунних показників (табл. 3).
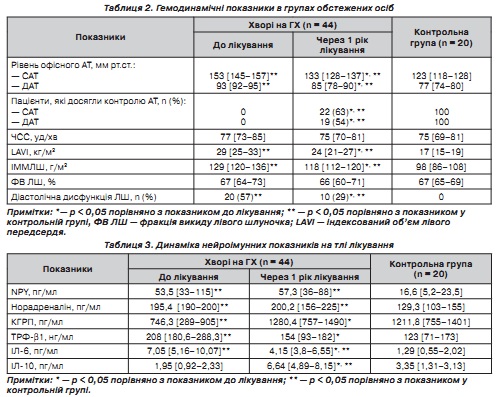 До початку лікування у хворих на ГХ відзначалася активація симпатичної ланки автономної нервової системи: спостерігалося підвищення плазмового вмісту норадреналіну та нейропептиду Y; рівень вазодилатуючого кальцитонін-ген-регулюючого пептиду був нижчим, ніж у контрольній групі, що свідчило про пригнічення вазодилатації. Достовірно вищою в пацієнтів із ГХ виявилася плазмова концентрація трансформуючого фактора росту β1, що є відображенням активації фібротичних процесів [10]. Порівняно з контрольною групою в гі- пертензивних хворих був наявний імунологічний дисбаланс, що проявлявся збільшеним умістом прозапального ІЛ-6 та зменшенням рівня протизапального та імуномодулюючого ІЛ-10. Через 1 рік лікування плазмовий рівень КГРП зріс на 71 % (р < 0,05). Рівні трансформуючого фактора росту β1 та прозапального ІЛ-6 зменшилися на 25 % ф < 0,05) та 41 % ф < 0,05) відповідно. Антигіпертензивне лікування призвело також до збільшення рівня ІЛ-10 у сироватці крові в 3,4 раза. Рівні плазмових маркерів активності симпатичної нервової системи — норадреналін та NPY — достовірно не змінилися під впливом лерканідипіну. Таким чином, антигіпертензивне лікування лерканідипіном протягом одного року асоціювалося з позитивними змінами кардіогемодинаміки у хворих на ГХ, що є результатом впливу лікування на різні патогенетичні ланки захворювання. Лерканідипін реалізує свої ефекти завдяки збільшенню плазмового вмісту КГРП та подальшій системній вазодилатації, а також частково знижуючи рівні фіброзогенного ТФР-βl та прозапального ІЛ-6. Антипроліферативні властивості блокатора потенціалзалежних кальцієвих каналів щодо гладком’язових клітин були описані раніше в експерименті [8]. Результати високої ефективності лерканідипіну у хворих на ГХ із наслідками інсульту та в осіб з ожирінням є перспективними для подальших досліджень застосування препарату в цього контингенту хворих.
До початку лікування у хворих на ГХ відзначалася активація симпатичної ланки автономної нервової системи: спостерігалося підвищення плазмового вмісту норадреналіну та нейропептиду Y; рівень вазодилатуючого кальцитонін-ген-регулюючого пептиду був нижчим, ніж у контрольній групі, що свідчило про пригнічення вазодилатації. Достовірно вищою в пацієнтів із ГХ виявилася плазмова концентрація трансформуючого фактора росту β1, що є відображенням активації фібротичних процесів [10]. Порівняно з контрольною групою в гі- пертензивних хворих був наявний імунологічний дисбаланс, що проявлявся збільшеним умістом прозапального ІЛ-6 та зменшенням рівня протизапального та імуномодулюючого ІЛ-10. Через 1 рік лікування плазмовий рівень КГРП зріс на 71 % (р < 0,05). Рівні трансформуючого фактора росту β1 та прозапального ІЛ-6 зменшилися на 25 % ф < 0,05) та 41 % ф < 0,05) відповідно. Антигіпертензивне лікування призвело також до збільшення рівня ІЛ-10 у сироватці крові в 3,4 раза. Рівні плазмових маркерів активності симпатичної нервової системи — норадреналін та NPY — достовірно не змінилися під впливом лерканідипіну. Таким чином, антигіпертензивне лікування лерканідипіном протягом одного року асоціювалося з позитивними змінами кардіогемодинаміки у хворих на ГХ, що є результатом впливу лікування на різні патогенетичні ланки захворювання. Лерканідипін реалізує свої ефекти завдяки збільшенню плазмового вмісту КГРП та подальшій системній вазодилатації, а також частково знижуючи рівні фіброзогенного ТФР-βl та прозапального ІЛ-6. Антипроліферативні властивості блокатора потенціалзалежних кальцієвих каналів щодо гладком’язових клітин були описані раніше в експерименті [8]. Результати високої ефективності лерканідипіну у хворих на ГХ із наслідками інсульту та в осіб з ожирінням є перспективними для подальших досліджень застосування препарату в цього контингенту хворих.
Висновки
1. Лерканідипін проявляє високу антигіпертензивну ефективність при лікуванні хворих на гіпертонічну хворобу помірного, високого, дуже високого додаткового ризику, а також у пацієнтів із супутнім ожирінням.
2. Лерканідипін реалізує свої ефекти завдяки збільшенню плазмового вмісту вазодилатуючого кальцитонін-ген-регулюючого пептиду, знижуючи плазмовий рівень трансформуючого фактора росту β1, без негативного впливу на симпатичну активацію.
Перспективи подальших досліджень. Зважаючи на отримані дані щодо нових механізмів дії та ефективності лерканідипіну у хворих на ГХ ІІІ стадії, які перенесли ішемічний інсульт, перспективним вважаємо проведення подальших рандомізованих клінічних досліджень щодо вивчення ефективності цього препарату в первинній та вторинній профілактиці інсультів.
Список літератури
1. Герасимов А.Н. Медицинская статистика / А.Н. Герасимов. — М.: Медицинское информ. агентство, 2007. — 480 с.
2. Рекомендації Української Асоціації кардіологів з профілактики та лікування артеріальної гіпертензії. Посібник до Національної програми профілактики і лікування артеріальної гіпертензії. — К. : ППВМБ, 2008. — 80 с.
3. Сіренко Ю.М. Гіпертонічна хвороба і артеріальні гіпертензії / Ю.М. Сіренко. — Донецьк, 2011. — 304 с.
4. Bang L.M. Lercanidipine: A Review of its Efficacy in the Management of Hypertension / Bang L.M., Chapman T.M., Goa K.L. // Drugs. — 2003. — Vol. 63, № 22. — Р. 2449-2472.
5. Benazepril plus amlodipine or hydrochlorothiazide for hypertension in high-risk patients / Jamerson K., Weber M.A., Bakris G.L. [et al.] ACCOMPLISH Trial Investigators // N. Engl. J. Med. — 2008. — Vol. 359. — P. 2417-2428.
6. Double-blind crossover study of lercanidipine versus amlodipine in the treatment of mild-to-moderate essential hypertension / De Giorgio L.A., Orlandini F., Malasoma P. еt al. // Curr. Ther. Res. — 1999. — 60. — 511-20.
7. Law M.R. Use of blood pressure lowering drugs in the prevention of cardiovascular disease: meta-analysis of 147 randomised trials in the context of expectations from prospective epidemiological studies / Law M.R., Morris J.K., Wald N.J. // B.M.J. — 2009. — Vol. 338. — P. 1665-1683.
8. Novel mechanisms of the antiproliferative effects of amlodipine in vascular smooth muscle cells from spontaneously hypertensive rats / Lai Y.M., Fukuda N., Su J.Z. [et al]// Hypertens. Res. — 2002. — Vol. 25. — P. 109-115.
9. Telmisartan, ramipril, or both in patients at high risk for vascular events / ONTARGET Investigators: Yusuf S., Teo K.K., Pogue J. [et al.]//N. Engl. J. Med. — 2008. — Vol. 358. — P. 1547-1559.
10. TGF-β1 mediates the hypertrophic cardiomyocyte growth induced by angiotensin II/Schultz J.E.J., Witt S.A., Glascock B.J. [et al.]// J. Clin. Invest. — 2002. — Vol. 109. — P. 787-796.
11. The seventh report of the Joint National Committee on prevention detection, evaluation and treatment of high blood pressure. The JNC VII Report / Chobanian A.V., Bakris G.L., Black H.R. [et al.]// JAMA. — 2003. — Vol. 289. — P. 2560-2573.