Рекомендації робочої групи з функціональної діагностики Асоціації кардіологів України та Всеукраїнської асоціації фахівців з ехокардіографії
Члени робочої групи з підготовки рекомендацій: акад. НАМН України, проф. В.М. Коваленко, проф. Сичов О.С., проф. М.М. Долженко, проф. Ю.А. Іванів, к.м.н. С.І. Деяк, к.м.н. С.В. Поташев, Н.М. Носенко
Зміст
Вступ . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
I. Фізіологія . . . . . . . . . . . . . . . . . . . . . . . .
II. Кореляція морфологічних та функціональних змін при діастолічній дисфункції . . . . . . . . . . . . . . . . . . . . . . .
A. Гіпертрофія ЛШ . . . . . . . . . . . . . . . . . . .
B. Об'єм ЛП . . . . . . . . . . . . . . . . . . . . . .
C. Функція ЛП . . . . . . . . . . . . . . . . . . . . .
D. Систолічний та діастолічний таск у легеневій артерії . . . . .
III. Трансмітральний кровоток . . . . . . . . . . . . . . . . . . . . . . .
A. Отримання та доступність . . . . . . . . . . . . .
B. Виміри . . . . . . . . . . . . . . . . . . . .
C. Нормальні значення . . . . . . . . . . . . . . . . . . . .
D. Типи кровотоку та гемодинаміка . . . . . . . .
E. Клінічне застосування у пацієнтів зі зниженною та нормальною ФВ . . . . . . . . . . . . . . . . . . .
F. Обмеження . . . . . . . . . . . . . . . . . . . . . .
IV. Проба Вальсальви. . . . . . . . . . . . . . . . . . . .
A. Виконання та отримання . . . . . . . . . . . .
B. Клінічне застосування . . . . . . . . . . . . . . . . .
C. Обмеження . . . . . . . . . . . . . . . . . . . . . .
V. Кровоток в легеневих венах . . . . . . . . . . . . . . . .
A. Отримання та доступність . . . . . . . . . . . . .
B. Виміри . . . . . . . . . . . . . . . . . . . .
C. Гемодинамічні детермінанти . . . . . . . . . . . .
D. Нормальні значення . . . . . . . . . . . . . . . . . . . .
E. Клінічне застосування у пацієнтів зі зниженною та нормальною ФВ . . . . . . . . . . . . . . . . . . .
F. Обмеження . . . . . . . . . . . . . . . . . . . . . .
VI. Швидкість розповсюдження діастолічного кровотоку в ЛШ за даними кольорового М-режиму . . . . . . .
A. Отриманная, доступність та виміри . . . .
B. Гемодинамічні детермінанти . . . . . . . . . . . .
C. Клінічне застосування . . . . . . . . . . . . . . . . .
D. Обмеження . . . . . . . . . . . . . . . . . . . . . .
VII. Рання та пізня швидкості діастолічного руху мітрального кільця за даними тканинної допплерографії . . . . . . . . . . . . . . . . . . . . . . . . .
A. Отримання та доступність . . . . . . . . . . . . .
B. Виміри . . . . . . . . . . . . . . . . . . . .
C. Гемодинамічні детермінанти . . . . . . . . . . . .
D. Нормальні значення . . . . . . . . . . . . . . . . . . . .
E. Клінічне застосування . . . . . . . . . . . . . . . . .
F. Обмеження . . . . . . . . . . . . . . . . . . . . . .
VIII. Виміри деформації . . . . . . . . . . . . . .
IX. Розкручування лівого шлуночка . . . . . . . . . . . . . .
A. Клінічне застосування . . . . . . . . . . . . . . . . .
B. Обмеження . . . . . . . . . . . . . . . . . . . . . .
X. Оцінка розслаблення лівого шлуночка . . . . . .
A. Пряме визначення . . . . . . . . . . . . . . . . . .
1. IVRT. . . . . . . . . . . . . . . . . . . . . . . .
2. Постійно-хвильовий сигнал аортальної регургітації . . . . . . . . .
3. Постійно-хвильовий сигнал мітральної регургітації . . . . . . . . . . . . . . . . . . .
B. Сурогатні виміри . . . . . . . . . . . . . .
1. Швидкості трансмітрального кровотоку . . . . . . . . . . . . .
2. Спектри руху мітрального кільця за тканинним допплером . . . . . . . . .
3. Vp у кольоровому М-режимі . . . . . . . . . . . . . . . . .
XI. Визначення жорсткості лівого шлуночка. . . . . . . .
A. Пряме визначення . . . . . . . . . . . . . . . . . .
B. Сурогатні виміри . . . . . . . . . . . . . .
1. DT раннього трансмітрального кровотоку Е . . . . . . . . . . . . .
2. Тривалість хвилі А . . . . . . . . . . . . . . .
XII. Діастолічний стрес-тест. . . . . . . . . . . . . . . . . . .
XIII. Інші причини симптомів серцевої недостатності у пацієнтів з нормальною фракцією викиду . . . . . . .
A. Хвороби перикарду . . . . . . . . . . . . . . . . .
B. Мітральний стеноз . . . . . . . . . . . . . . . . . . . .
C. Мітральна регургітація . . . . . . . . . . . . . . . . . . . . . . . . . .
XIV. Оцінка тиску наповнення лівого шлуночка в особливих популяціях . . . . . . . . . . . . . . . . . . .
A. Фібриляція передсердь . . . . . . . . . . . . . . . . . .
B. Синусова тахікардія . . . . . . . . . . . . . . . . . .
C. Рекстриктивна кардіоміопатія . . . . . . . . . . . .
D. Гіпертрофічна кардіоміопатія . . . . . . . . . . .
E. Легенева гіпертензія . . . . . . . . . . . . . .
XV. Прогноз . . . . . . . . . . . . . . . . . . . . . . . . .
XVI. Рекомендації для клінічних закладів . . . . .
A. Оцінка тиску наповнення ЛШ у хворих із зниженою ФВ . . . . . . . . . . . . . . . . . . . .
B. Оцінка тиску наповнення ЛШ у хворих з нормальною ФВ. . . . . . . . . . . . . . . . . . . . . .
C. Класифікація діастолічної дисфункції . . . . . . . . . . .
XVII. Рекомендації до застосування в наукових дослідженнях та клінічних випробуваннях . . . . . . . . . . . . . . .
Вступ
Оцінка діастолічної функції лівого шлуночка (ЛШ) повинна бути інтегральною частиною рутинного ехокардіографічного дослідження, особливо у пацієнтів із скаргами на задишку чи іншими симптомами серцевої недостатності (СН). Близько половини усіх хворих з вперше встановленим діагнозом СН мають нормальну або субнормальну (незначно знижену) фракцію викиду (ФВ) ЛШ. Цим пацієнтам встановлюється «діастолічна СН» [1], що за класифікацією Українського товариства кардіологів відповідає діагнозу «СН із збереженою скоротливою функцією ЛШ”. Оцінка діастолічної функції та тиску наповнення ЛШ має величезне клінічне значення для диференційної діагностики цього стану від інших хвороб, що супроводжуються задишкою, таких як легенева гіпертензія та інші, для оцінки прогнозу та визначення підлеглої кардіальної патологію з метою вибору найкращої лікувальної стратегії.
Тиск наповнення ЛШ оцінюється інвазивним шляхом з визначенням середнього тиску заклинювання легеневих капілярів чи середнього тиску в лівому передсерді (ЛП) (в обох випадках за відсутності мітрального стенозу), кінцево-діастолічного тиску ЛШ (КДТ ЛШ; тиск в момент початку комплексу QRS ЕКГ або безпосередньо після закінчення трансмітральної хвилі А), та діастолічного тиску в ЛШ перед хвилею А (Рис. 1). Хоча значення цих тисків є різними в абсолютних значеннях, вони близько пов’язані, та передбачувано збільшуються при патології міокарду, при чому КДТ ЛШ збільшується раніше підвищення середнього тиску в ЛП. Протягом останніх двадцяти з чимось років ехокардіографія (ЕхоКГ) грала центральну роль в оцінці діастолічної функції ЛШ. Мета даного документу – забезпечити зрозумілий огляд технік та методик, та важливість оцінюваних параметрів діастоли ЛШ, а також надати рекомендації з номенклатури та відображення даних про діастолічну функцію ЛШ в заключеннях ехокардіографічного обстеження у дорослих. Дані рекомендації базуються на Рекомендаціях Європейської асоціації з ЕхоКГ, критичному огляді наявних літературних даних та експертному консенсусі членів Всеукраїнської асоціації фахівців з ЕхоКГ.
I. Фізіологія
Оптимальная функція ЛШ залежить від його здатності циклічно змінюватися в діапазоні двох станів: 1) податливої камери в діастолу, що дозволяє ЛШ наповнюватися кров’ю з ЛП з відносно низьким тиском в ньому; 2) жорсткої камери в систолу з швидко наростаючим тиском, що виганяє ударний об’єм на високому артеріальному рівні тиску. Шлуночок, таким чином, має дві функції, що слідують по черзі: систолічне вигнання та діастолічне наповнення.
Крім того, ударний об’єм (УО) має зростати у відповідь на потребу, таку як фізичні вправи та ін., без підвищення тиску в ЛП [2]. Теоретично оптимальна крива тиску в ЛШ має чотирьохкутний контур із швидким підйомом до пікового кінцево-систолічного та швидким падінням до низького діастолічного тиску, що забезпечує максимальну тривалість діастолічного наповнення ЛШ. Ця теоретично оптимальна ситуація досягається циклічною взаємодією міофіламентів, та має на увазі неушкоджену функцію мітрального (МК) та аортального клапанів. Діастола починається із закриттям аортального клапана (АК), та включає в себе чотири фази: 1) швидке падіння тиску в ЛШ підчас ізоволюмічного розслаблення (IR чи IVRT); 2) швидке наповнення; 3) діастазу (не завжди – при повільнішій частоті скорочень); та 4) скорочення передсердя [2].
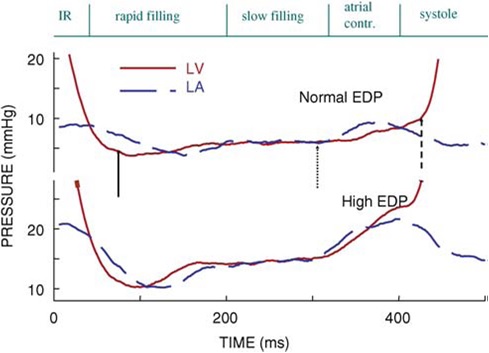
Рис. 1 Чотири фази діастоли розмежовані у зв’язку з послідовним записом кривих тиску в ЛП та ЛШ у собаки під анестезією. Перше перехрестя відповідає закінченню ізоволюмічної релаксації (IR) та відкриттю МК. В першу фазу тиск в ЛП перевищує тиск в ЛШ, що викликає швидке прискорення трансмітрального кровотоку. Пік раннього трансмітрального потоку Е грубо відповідає другому перехрестю тиску. Безпосередньо після цього тиск в ЛШ починає перевищувати тиск в ЛП, що сповільнює трансмітральних кровотоку. Ці дві фази відповідають швидкому наповненню ЛШ, якому наслідує повільне наповнення при майже відсутній різниці між ЛШ та ЛП (діастаза). Підчас скорочення передсердя тиск в ЛП знов перевищує тиск в ЛШ. Товста стрілка вказує на момент мінімального тиску в ЛШ, крапчаста – на рівень тиску в ЛШ перед хвилею А (систолою передсердя), а пунктирна – на КДТ ЛШ. Верхні графіки були записані при нормальному КДТ = 8 мм Hg. Нижні графіки були записані після перевантаження об’ємом та підвищення КДТ ЛШ до 24 мм Hg. Помітьте, що на нижніх графіках різниці між тисками в ЛШ та ЛП суттєво більші, що відбиває зниження податливості ЛП та ЛШ. Скорочення передсердя призводить до різкого підвищення тиску в ЛШ, а тиск в ЛП з трудом досягає рівня підвищення КДТ ЛШ. (Courtesy of T. C. Gillebert and A. F. Leite-Moreira.)
Підвищення тиску наповнення ЛШ є головним фізіологічним наслідком діастолічної дисфункції [2]. Тиски наповнення вважаються підвищенними при підвищенні тиску заклинювання легеневих капілярів (ТЗЛК) до 12 мм Hg і вище, або при КДТ ЛШ ≥ 16 мм Hg [1]. У здорових суб’єктів тиск наповнення ЛШ підчас фізичного навантаження змінюється мінімально. Підвищення тиску наповнення ЛШ підчас фізичного навантаження обмежує толерантність до навантаження та може свідчити про діастолічну дисфункцію. Тиск наповнення ЛШ визначається характером наповнення та пасивними властивостями стінок ЛШ, але також може бути модульованим неповним розслабленням міокарда та варіабельністю тонусу міокарда.
На молекулярному рівні циклічна взаємодія міофіламентів призводить до формування циклу скорочення та розслаблення міокарду. Розслаблення (релаксація) є процесом, під час якого міокард після скорочення повертається до своїх початкових ненапружених довжини та тонусу. В нормальних серця в умовах нормального навантаження релаксація міокарду є практично повною при мінімальному тиску в ЛШ. Скорочення та релаксація міокарду відносяться до одного й того ж самого молекулярного процесу транзиторної активації міозитів та дуже тісно взаємопов’язані [3]. Ступінь релаксації контролюється рівнем навантаження, інактивації та асинхронії [2].
Підвищення післянавантаження або пізнього систолічного навантаження сповільнює релаксацію міокарда, особливо в комбінації з підвищеним переднавантаженням, таким чином додаючи до підвищення тиску наповнення [4]. Інактивація міокарда пов’язана з процесами вивільнення кальцію із цитозоля та роз’єднанням містків, що знаходяться під впливом ряду протеїнів, регулюючих гомеостаз кальцію [5], цикл зчеплення-розчеплення містків актину-міозину [2], та енергетичні процеси в міокарді [3]. Мінімальні регіональні варіації скорочення та розслаблення по часу є фізіологічними. Втім, диссинхронія релаксації буде призводити до порушення взаємодії між раннім розтягуванням стінок в деяких сегментах та постсистолічним скороченням інших сегментів, що буде додавати до сповільнення глобальної релаксації ЛШ та підвищенню тиску його наповнення [6].
Швидкість загальної релаксації ЛШ відображається моно експоненціальною кривою падіння тиску в ЛШ, що передбачає високу кореляцію (r >0,97) з реальним моноекспоненціальним падінням тиску в порожнині ЛШ. Тау (τ) є широко загальноприйнятим інвазивним показником релаксації ЛШ, що досягає свого значення на 97% через час, що відповідає 3,5τ після dP/dtmin. Діастолічна дисфункції визначається значенням τ >48 мс [1]. На додаток, швидкість релаксації має оцінюватися також за допомогою dP/dtmin ЛШ, та (непрямо) часом ізоволюмічної релаксації (IVRT), або часовим інтервалом між закриттям аортального клапану (АК) та відкриттям мітрального клапану (МК).
Наповнення ЛШ визначається взаємодією між тисками наповнення ЛШ та властивостями наповнення. Ці властивості наповнення описуються жорсткістю (ΔP/ΔV), або зворотно пропорційно податливістю (compliance) (ΔP/ΔV), та звичайно відносяться до кінцево-діастолічних властивостей. coммonly refer to end-diastolic properties. Ці кінцево-діастолічні властивості визначаються декількома зовнішніми та внутрішніми факторами. До зовнішніх переважно відносяться тиск з боку перикарду та міжшлуночкова взаємодія. Внутрішні фактори включають жорсткість міокарду (кардіоміоцитів та екстрацелюлярного матриксу), міокардіальне напруження, геометрію порожнини та товщину стінок [5].
Жорсткість камери описує взаємозв’язок тиску-об’єму ЛШ, що мають декілька вимірів. Робоча жорсткість в будь-який момент часу дорівнює нахилу тангенціальної дотичної до кривої (ΔP/ΔV ) та може бути приблизно обчислена тілько з двома точними вимірами тиску-об’єму . Діастолічна дисфункції визначається при значенні нахилуs >0,20 мм Hg/mL [7]. З іншого боку, можливо охарактеризувати жорсткість камери ЛШ через тривалість діастоли кривою експоненти, що відповідає відношенню тиску до об’єму ЛШ. Відповідна крива може бути застосована до взаємовідносини тиску та об’єму одного скорочення ЛШ чи до кінцево-діастолічної кривої тиску об’єму, побудованої за допомогою усереднення правого нижнього кута множинних петель тиску-об’єму, отриманих при різних тисках наповнення (різних умовах переднавантаження). Останній метод має перевагу, як такий, що є менш залежним від моментального міокардіального розслаблення.
Певний аспект діастолічної функції пов'язаний з повздовжньою функцією та скручуванням (торсією). Torrent-Guasp та спіавт. [8] описали, як шлуночки мають до певної міри асимілюватися у єдиний м’язовий тяж, що починається з правого шлуночка (ПШ) під коренем легеневої артерії (ЛА) та формує подвійну спіраль, що розповсюджується на ЛШ, де її інший кінець прикріплюється до аорти. Ця подвійна спіральна орієнтація м’язових волокон призводить до систолічного скручування (торсії) та діастолічного розкручування (торсіонної віддачі).
Ключові моменти
(1) Діастолічна функція є пов’язаною з розслабленням (релаксацією) міокарду та пасивними властивостями ЛШ, та модулюється тонусом міокарду.
(2) Розслаблення міокарду визначається навантаженням, інактивацією та неоднорідністю міокарда.
(3) Жорсткість міокарда визначається кардіоміоцитами та інтерстиціальним матріксом (ступенем вираженості фіброзу).
II. Взаємозв'язок морфологічних та функціональних змін при діастолічній дисфункції
A. Гіпертрофія ЛШ
Хоча діастолічна дисфункція не є рідкою у пацієнтів з нормальною товщиною стінок ЛШ, гіпертрофія ЛШ є однією з найчастіших її причин. У пацієнтів з діастолічної серцевою недостатністю (СН), тобто СН із збереженою систолічною функцією ЛШ, часто спостерігається концентрична гіпертрофія (підвищення маси та відносної товщини стінок) чи ремоделювання (нормальна маса при підвищенні відносної товщини стінок) ЛШ. І навпаки, ексцентрична гіпертрофія ЛШ (збільшена маса при нормальній віносній товщині стінок) звичайно виявляється у хворих із зниженою ФВ ЛШ. Внаслідок високої розповсюдженості гіпертензії, особливо в літній популяції, гіпертрофія ЛШ є дуже частим явищем, а гіпертензивне серце є найчастішим станом, що призводить до діастолічної СН.
Найкращим, хоча й самим трудомістким методом визначення маси міокарду (ММ) ЛШ є 3-вимірна ЕхоКГ [9]. Тим не менш, цілком можливим та доречним в рутинній клінічній практиці є вимірювання ММ ЛШ за допомого 2-вимірної ЕхоКГ згідно нещодавно опублікованих рекомендацій Української асоціації фахівців з ЕхоКГ та Американського товариства з ЕхоКГ [10]. Для клінічних цілей бажано визначати принаймні товщину стінок ЛШ, а краще і масу та індекс маси міокарда ЛШ для більш точного заключення про діастолічну функцію та тиск наповнення ЛШ.
При патологічній гіпертрофії міокарду розслаблення ЛШ звичайно сповільнене, що знижує долю раннього діастолічного наповнення. При наявності нормального тиску в ЛП сповільнення релаксації приводить до збільшення питомої ваги систоли передсердь у загальному наповненні ЛШ. Таким чином, переважання питомої ваги раннього наповнення, а не передсердного, у хворих з патологічною гіпертрофією свідчить про підвищений тиск наповнення ЛШ.
B. Об'єм ЛП
Визначення об’єму ЛП є високо відтворюваним та надійним у більшості випадків, при чому найбільш точні вимірювання відтворюються в апікальних 4- та 2-камерних доступах [10]. Ця оцінка є клінічно важливою, тому що існує достовірний високий взаємозв’язок між ремоделюванням ЛП та ехокардіографічними показниками діастолічної функції [11]. Втім, допплерівські швидкості та часові інтервали відбивають миттєві тиски наповнення безпосередньо в момент визначення, в той час як об’єм ЛП відбиває кумулятивні ефекти коливань тисків наповнення протягом певного часу.
Важливим є спостереження на базі обсерваційних досліджень, що включали 6,657 пацієнтів без попереднього анамнезу фібриляції передсердь (ФП) та клінічно значущої клапанної патології, що індекс об’єму ЛП ≥34 мл/м2 є незалежним предиктором смертності, розвитку маніфестної СН, ФП та ішемічного інсульту [12]. Втім, треба пам’ятати, що дилатація ЛП може спостерігатися у хворих з брадикардією та збільшенням всіх чотирьох камер, анемією та іншими станами, що супроводжуються збільшенням серцевого викиду, тріпотінням та ФП, клінічно значущою патологією мітрального клапана навіть при відсутності діастолічної дисфункції. Крім того, дилатація ЛП досить часто наявна у професійних спортсменів взагалі при відсутності кардіальної патології (Рис. 2). Таким чином, важливо співвідносити об’єм ЛП із загальним клінічним статусом пацієнта, розмірами інших порожнин, та допплерівськими параметрами розслаблення ЛШ.
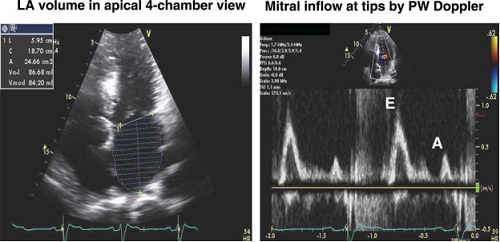
Рис 2. (Зліва) Кінцево-систолічний (максимальний) об’єм ЛП у професійного спортсмена з індексом об’єму ЛП 33 мл/м2. (Справа) Нормальна графіка трансмітрального кровопотоку, отримана за допомогою імульсно-хвильового (ІХ) допплера (ІХД) у того ж самого суб’єкта. Швидкість раннього діастолічного потоку Е складала 100 см/с, а потоку в систолу передсердь А – 38 см/с. У цього атлета мала місце фізіологічна МР, що видно на допплерівському спектрі. Зауважте наявність збільшеного об’єму ЛП не зважаючи на нормальну міокардіальну функцію.
C. Функція ЛП
Передсердя модулює наповнення шлуночка через свою резервуарну, провідникову та насосну функції [13]. Підчас систоли шлуночків та їх ізоволюмічної релаксації, коли атріо-вентрикулярні (АВ) клапани зачинені, камери передсердь працюють у якості розтяжних резервуарів, що накопичують кров, що потрапляє в них з венозної циркуляції (резервуарний об’їм визначається як об’єм пасивного випорожнення ЛП мінус об’єм зворотного потоку у легеневих венах підчас систоли передсердь). Передсердя також є насосною камерою, що додає певну долю до адекватного кінцево-діастолічного об’єму (КДО) ЛШ за рахунок активного скорочення наприкінці діастоли (ударний об’єм (УО) ЛП визначається як об’єм ЛП на початку ЕКГ хвилі Р мінус мінімальний об’єм ЛП). Врешті решт, передсердя також виступає як кондуїт (провідник), що функціонує від відкриття АК та припиняє функціонування перед скороченням передсердя, та може бути визначений як УО ЛШ мінус суму пасивного та активного об’ємів ЛП, що випорожнюються. Резервуарний, кондуїтний та ударний об’єми ЛП можуть бути розраховані та виражені у відсотках від УО ЛШ [13].
Порушення релаксації ЛШ асоціюється з нижчим діастолічним раннім АВ- градієнтом та зниженням кондуїтного об’єму ЛП, у той час як збільшується роль резервуарно-насосного комплексу з метою підтримання оптимального кінцево-діастолічного об’єму ЛШ та нормального УО ЛШ. При більш прогресивних ступенях діастолічної дисфункції та зниженні скоротливості ЛШ збільшується вклад ЛП у наповнення ЛШ.
Окрім УО ЛП, систолічна функція ЛП може бути оцінена за допомогою 2D та допплерівських вимірів [14,15] як сила викиду ЛП (залежить від переднавантаження, розраховується як 0,5 х 1,06 х площа мітрального кільця х [швидкість піку А]2) та кінетична енергія (0,5 х 1,06 х УО ЛП х [швидкість піку А]2). Крім ого, нещодавно опубліковані роботи, що оцінювали деформацію (strain) та швидкість деформації (strain rate) ЛП та їх клінічний взаємозв’язок у пацієнтів з ФП [16,17]. Потрібні додаткові дослідження для кращого вивчення та визначення ролі цих клінічних характеристик.
D. Систолічний та діастолічний тиск у легеневій артерії
Маніфестні пацієнти з діастолічної дисфункцією звичайно спостерігається підвищення тиску в легеневій артерії (ЛА). Тому, при відсутності легеневої патології підвищення тиску у ЛА може використовуватись як свідоцтво підвищення таску наповнення ЛШ. І насправді між систолічним тиском у ЛА та неінвазивно оціненим тиском наповнення ЛШ була виявлена значуща кореляція [18]. Для розрахунку систолічного тиску у ЛА (СТЛА) використовується постійно-хвильова (ПХ) допплерограма трикуспідальної регургітації (ТР) з якої розраховується максимальний градієнт тиску за максимальною швидкістю регургітації та систолічний тиск у правому передсерді (ПП) (Рис. 3) [19]. У пацієнтів з важкою ТР та низькими систолічними градієнтами між правим шлуночком (ПШ) та ПП точність розрахунку СТЛА залежить від надійного визначення систолічного тиску у ПП, що є еквівалентним центральному венозному тиску (ЦВТ).
Аналогічно, кінцево-діастолічна швидкість потоку регургітації на клапані ЛА (ЛР) (Рис. 4) може використовуватись для розрахунку діастолічного тиску у ЛА (ДТЛА) [19]. За необхідності, обидва ПХ-сигнали можуть бути підсилені за допомогою збовтаного фізіологічного розчину або офіцинального внутрішньовенного ультразвукового контрасту (потрібна обережність в оцінці, бо існує вірогідність переоцінки надлишкових шумів сигналів). Оцінка тиску в ПП потрібна для обох розрахунків, та може бути визначена за допомогою оцінки діаметру нижньої порожнистої вени (НПВ) та його коливань підчас дихання, а також за допомогою співвідношення систолічної та діастолічної швидкостей кровотоку в печінкових венах [19].
ДТЛА, визначений за допомогою допплерографії, звичайно добре корелює з інвазивно виміряним тиском заклинювання у легеневих капілярах (ТЗЛК), та може бути використаний в рутинній практиці, як сурогат ТЗЛК [20]. Обмеженням використання ДТЛА є відносно низка доступність адекватних допплерівських сигналів ЛР (<60%), особливо у пацієнтів блоків інтенсивної терапії та без використання контрастних агентів. Крім того, точність визначення дуже сильно залежить від акуратного визначення середнього тиску у ПП, що також може викликати забруднення в деяких випадках. Припущення, що споріднює ДТЛА до тиску у ЛП, має достатню точність у пацієнтів без вираженої (помірної чи важкої) легеневої гіпертензії. Втім, у пацієнтів з легеневим судинним опором, що перевищує 200 дін х с х см -5 або середнім тиском у ЛА >40 мм Hg, ДТЛА звичайно декілька вище (на 5 мм Hg), ніж середній ТЗЛК [21].
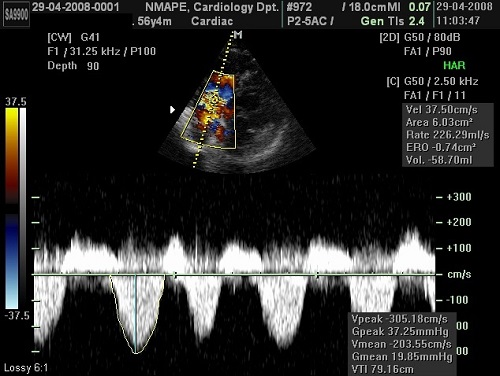
Рис 3. Визначення систолічного тиску у ЛА з використанням ПХ-спектру ТР. У даного пацієнта пікова швидкість ТР складає 3,05 м/с (піковий градієнт дорівнює 37 мм Hg), а тиск у ПП дорівнював 20 мм Hg. СТЛА дорівнює 37+20=57 мм Hg).
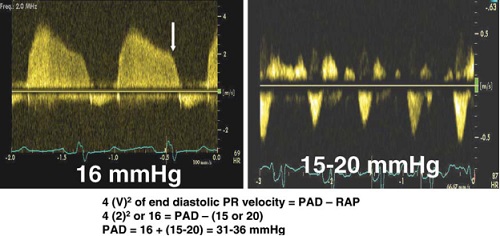
Рис 4. Визначення діастолічного тиску у ЛА з використанням ПХ-спектру ЛР (зліва) та ІХ-спектру кровотоку в печінкових венах (справа). У даного пацієнта кінцево-діастолічна швидкість потоку ЛР складала 2 м/с (градієнт тиску 16 мм Hg), а тиск у ПП дорівнював від 15 до 20 мм Hg, таким чином ДТЛА = 16+ (15-20) = 31-36 мм Hg (див. Quinones et al. [19] для подробиць з визначення середнього тиску у ПП).
III. Трансмітральний кровоток
A. Отримання та відтворюваність
Імпульсно-хвильова (ІХ) допплерографія (ІХД) виконується в апікальній 4-камерній (А4С) позиції для отримання трансмітрального приносного антероградного діастолічного потоку та його швидкостей для оцінки наповнення ЛШ [22]. Кольорове допплерівське картування (КДК) може бути корисним для оптимального встановлення курсору допплерівського променя, особливо при наявності дилатації ЛШ. Заохочується виконання ПВВ для оцінки швидкостей піків Е (ранній діастолічний поток) та А (пізній поток в систолу передсердь) перед використанням ІХД для більшої впевненості у тому, що отримано максимальні швидкості. Після цього пробний об’єм від 1 до 3 мм встановлюється між кінчиками стулок підчас діастоли для запису чіткого профілю швидкостей (Рис. 2). Оптимізація підсилення спектру та фільтрів необхідні для чіткого відображення початку та припинення токів діастолічного наповнення ЛШ. Майже у всіх пацієнтів можливий запис хвиль діастолічних потоків наповнення ЛШ бездоганної якості. Записи спектрів трансмітральних швидкостей повинні отримуватись на швидкостях розгортки 25 чи 50 мм/с для оцінки респіраторних коливань швидкостей кровотоку, які бувають досить вираженими у пацієнтів з легеневою чи перикардіальною патологією (див. далі). Якщо варіації відсутні, швидкість розгортки збільшують до 100 мм/с, а значення виводять з усереднення вимірів 3 послідовних циклів.
B. Виміри
Первинні (обов’язкові) виміри трансмітрального діастолічного кровотоку включають швидкості піку раннього наповнення (хвиля Е) та пізнього діастолічного наповнення в систолу передсердь (хвиля А), співвідношення швидкостей Е/А, час сповільнення раннього діастолічного наповнення (DT), та IVRT, що розраховується після розміщення курсору ПВД на межі виносного та приносного трактів ЛШ так, щоб водночас відобразити систолічний кровотоку викиду у ВТЛШ та початок діастолічного трансмітрального кровотоку. Вторинні (факультативні) виміри включають тривалість хвилі А (розраховується з позиції курсору на рівні мітрального кільця), загальний час (тривалість) діастолічного наповнення, інтеграл лінійної швидкості (VTI) хвилі А, та загальний VTI діастолічного трансмітрального кровотоку (за яким можна визначити фракцію наповнення ЛП) при розташуванні пробного об’єму на рівні мітрального кільця [22]. Важливо розпізнавати середньодіастолічний потік. У здорових суб’єктів може реєструватися низькошвидкісні потоки в діастазу (проміжок між піками Е та А підчас прикриття стулок клапану, коли потік майже припиняється внаслідок вирівнювання тиску між ЛП та ЛШ). Але при збільшенні швидкості середньо-діастолічного потоку (≥20 см/с), вони можуть бути ознакою значно сповільненої релаксації ЛШ та підвищеного тиску наповнення ЛШ [23].
C. Нормальні значення
При визначенні нормальних значень швидкостей та часових інтервалів трансмітрального діастолічного потоку в першу чергу треба орієнтуватись на вік. По мірі зростання віку знижується пікова швидкість раннього діастолічного потоку Е та співвідношення Е/А, в той час як DT та пікова швидкість пізнього потоку в систолу передсердь A зростають. Нормальні значення наведені в Таб. 1 [24].
Окрім діастолічної функції ЛШ та тиску наповнення на трансмітральний діастолічний потік впливає ряд інших факторів, включаючи частоту серцебиття та ритм, інтервал PQ, серцевий викид, розмір мітрального кільця та функція ЛП. Зміни діастолічної функції, пов’язані з віком, можуть відбивати сповільнення розслаблення міокарду, що є одним з факторів розвитку діастолічної СН у літніх суб’єктів.
D. Типи кровотоку та гемодинаміка
Типи трансмітрального кровотоку визначаються за співвідношенням Е/А та DT. Вони включають нормальну графіку, графіку порушення релаксації ЛШ, псевдонормальне наповнення (ПНН) ЛШ, та рестриктивное наповнення ЛШ. Визначення ПНН тільки за швидкостями трансмітрального потоку може бути важким (див. далі). Крім того, інколи спостерігаються нетипові профілі наповнення, наприклад, трьохфазний профіль діастолічного трансмітрального потоку. Найбільш виражені аномалії фізіології діастоли та профілю трансмітрального кровотоку часто спостерігаються у літніх пацієнтів з важкою та тривалою гіпертензією чи у пацієнтів з гіпертрофічною кардіоміопатією (ГКМП).
Таб. 1. Нормальні значення допплерівських діастолічних вимірів.
|
Показник
|
Вікова група (років)
|
|
16-20
|
21-40
|
41-60
|
>60
|
|
IVRT (мс)
|
50±9 (32–68)
|
67±8 (51–83)
|
74±7 (60–88)
|
87±7 (73–101)
|
|
E/A
|
1,88±0,45 (0,98–2.78)
|
1,53±0,40 (0,73–2.33)
|
1,28±0,25 (0,78–1,78)
|
0,96±0,18 (0,6–1,32)
|
|
DT (мс)
|
142±19 (104–180)
|
166±14 (138–194)
|
181±19 (143–219)
|
200±29 (142–258)
|
|
Adur (мс)
|
113±17 (79–147)
|
127±13 (101–153)
|
133±13 (107–159)
|
138±19 (100–176)
|
|
S/DЛВ
|
0,82±0,18 (0,46–1,18)
|
0,98±0,32 (0,34–1,62)
|
1,21±0,2 (0,81–1,61)
|
1,39±0,47 (0,45–2,33)
|
|
ЛВ AR (см/с)
|
16±10 (1–36)
|
21±8 (5–37)
|
23±3 (17–29)
|
25±9 (11–39)
|
|
ЛВ ARdur (мс)
|
66±39 (1–144)
|
96±33 (30–162)
|
112±15 (82–142)
|
113±30 (53–173)
|
|
Септальний Е’ (см/с)
|
14,9±2,4 (10,1–19,7)
|
15,5±2,7 (10,1–20,9)
|
12,2±2,3 (7.6–16.8)
|
10,4±2,1 (6,2–14,6)
|
|
Септальне Е’/А’
|
2,4*
|
1,6±0,5 (0,6–2,6)
|
1,1±0,3 (0,5–1,7)
|
0,85±0,2 (0,45–1,25)
|
|
Латеральний Е’ (см/с)
|
20,6±3,8 (13–28,2)
|
19,8±2,9 (14–25,6)
|
16,1±2,3 (11,5–20,7)
|
12,9±3,5 (5,9–19,9)
|
|
Латеральне Е’/А’
|
3,1*
|
1,9±0,6 (0,7–3,1)
|
1,5±0,5 (0,5–2,5)
|
0,9±0,4 (0,1–1,7)
|
Дані представлені як середнє ± SD (95% довірчий інтервал). Зауважте, що швидкість мітрального кільця Е’ у суб’єктів 16-20 років перехрещується зі значеннями у суб’єктів 21-40 років. Це тому, що швидкість руху мітрального кільця Е’ у дітей та підлітків з віком прогресивно зростає. Таким чином, швидкість Е’ у здорового 20-річної людини вище за нормальну швидкість у 16 років, що призводить до дещо нижчого середнього значення Е’ у суб’єктів вікової групи 16-20 років.
*Стандартні відхилення не включені, бо ці дані були розраховані, а не безпосередньо забезпечені клінічними спостереженнями згідно оригінальних статей, що були джерелами.
Добре визначено, що швидкість піку Е переважно відбиває градієнт тиску між ЛП та ЛШ (Рис. 5) підчас ранньої діастоли, і, таким чином, на нього впливає переднавантаження та порушення релаксації ЛШ [25]. Швидкість піку А відбиває градієнт тиску між ЛП та ЛШ підчас пізньої систоли, та на неї впливає податливість (compliance) ЛШ та скоротлива функція ЛП. На час сповільнення хвилі Е DT впливає релаксація ЛШ, діастолічний тиск в ЛШ після відкриття мітрального клапану та податливість (compliance) ЛШ (тобто, взаємозв’язок між тиском та об’ємом ЛШ). Зміни кінцево-систолічного та/чи кінцево-діастолічного об’ємів ЛШ, пружної віддачі ЛШ та/чи діастолічного тиску у ЛШ безпосередньо впливає на швидкості трансмітральних пікових швидкостей (тобто, переважно швидкість Е) та часові інтервали (тобто, DT та IVRT).
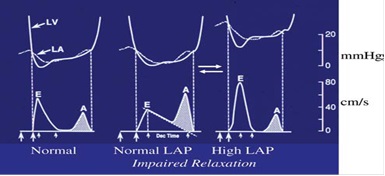
Рис. 5. Схематична діаграма змін профілю трансмітрального діастолічного потоку у відповідь на зміни трансмітральних градієнтів тиску (Normal – норма; Normal LAP – нормальний тиск у ЛП; High LAP – високий тиск у ЛП).
E. Клінічне застосування у пацієнтів зі зниженою та збереженою ФВ
У пацієнтів з дилатаційною кардіоміопатією (ДКМП) незалежно від етіології, показники ІХ-спектрів трансмітральних швидкостей та профілів трансмітрального наповнення ЛШ краще корелюють з тисками наповнення ЛШ, функціональним класом СН та прогнозом, ніж ФВ ЛШ [26-47]. Пацієнти з порушенням релаксації ЛШ мають менш виражену симптоматику, у той час як скорочення IVRT, DT, та прогресивне збільшення співвідношення Е/А є характеристиками більш прогресивної діастолічної дисфункції, збільшення тиску у ЛП та гірший функціональний клас СН. Рестриктивна графіка наповнення ЛШ також асоціюється з поганим прогнозом, особливо, якщо вона залишається після зниження переднавантаження (т.з., незворотне рестриктивное наповнення). Також псевдонормальна або рестриктивна графіка наповнення, асоційована з гострим інфарктом міокарда, вказує на підвищений ризик СН, несприятливого ремоделювання ЛШ та підвищення серцево-судинної смертності незалежно від ФВ ЛШ.
У пацієнтів з ішемічною хворобою серця (ІХС) [48] чи ГКМП [49, 50], у яких ФВ ЛШ ≥50%, показники трансмітрального діастолічного кровотоку погано корелюють з гемодинамікою. Це може бути пов’язаним із значною варіабельністю ступеня затримки релаксації ЛШ, що спостерігається у цих пацієнтів, що може призводити до різноманітних варіабельних трансмітральних градієнтів тиску при подібних вихідних значеннях тиску в ЛП. Рестриктивна графіка наповнення ЛШ та збільшення ЛП у пацієнтів зі збереженою ФВ ЛШ (≥50%) асоціюється з поганим прогнозом подібно до такої у хворих з ДКМП. Така ситуація досить розповсюджена при рестриктивних кардіоміопатіях (РКМП), особливо при амілоїдозі [51,52] та у реципієнтів після трансплантації серця [53].
F. Обмеження
Графіка (профіль) наповнення ЛШ має U-контурний взаємозв’язок з діастолічної функцією ЛШ, з подібними значеннями у здорових нормальних суб’єктів та у хворих з кардіальної патологією. Хоча ця відмінність не є проблемою при зниженій систолічній функції ЛШ, але проблема розпізнання ПНН та діастолічної СН у пацієнтів із збереженою ФВ ЛШ була основним імпульсом для розвитку множинних допоміжних методик оцінки діастолічної функції, що обговорюються у послідуючих розділах. Іншими факторами, що ускладнюють інтерпретацію показників трансмітрального потоку є синусова тахікардія [54], патологія провідності та аритмії.
Синусова тахікардія та АВ-блокада першого ступеня можуть призводити до часткового або повного злиття піків Е та А. Якщо швидкість мітрального потоку на початку систоли передсердь не перевищує 0,20 см/с, швидкість хвилі А може зростати, що зменшує співвідношення Е/А. При частковому злитті хвиль Е та А може бути неможливим виміряти DT, хоча на вимір IVRT це впливати не має. При ФП на наповнення ЛШ кардинально впливають швидкі передсерді скорочення, таки чином вимірювання швидкості піку Е, співвідношення Е/А чи DT не можливе. При наявності АВ-блокади 3:1 або 4:1, наявні множинні передсерді скорочення з діастолічною мітральною регургітацією (МР), що перемежається з непроведеними передсердними скороченнями [55]. У цих випадках тиски в ЛА, розраховані за допомогою швидкостей ТР та ЛА можуть бути найкращими індикаторами підвищеного тиску наповнення ЛШ (при відсутності значущої легеневої патології).
Ключові моменти
(1) ІХД виконується в А4С позиції для отримання швидкостей трансмітрального діастолічного потоку для оцінки наповнення ЛШ.
(2) Пробний об’єм шириною 1-3 мм встановлюється рівно між стулками мітрального клапану підчас систоли для запису чітких швидкісних спектрів.
(3) Основні (первинні) виміри включають пікові швидкості Е і А, співвідношення Е/А, DT та IVRT.
(4) Профілі діастолічного мітрального кровотоку включають нормальне наповнення, порушення релаксації ЛШ, ПНН та рестриктивне наповнення ЛШ.
(5) У пацієнтів з ДКМП різної етіології профілі трансмітрального діастолічного кровотоку наповнення краще корелюють з тиском наповнення ЛШ, функціональним класом СН та прогнозом, ніж ФВ ЛШ.
(6) У хворих з ІХС та ГКМП з ФВ ЛШ ≥50% швидкості трансмітрального діастолічного кровотоку слабо корелюють з гемодинамікою.
IV. Проба Вальсальви
A. Отримання та відтворюваність
Проба Вальсальви виконується шляхом сильного напружування (близько 40 мм Hg) без видоху через ніс чи рот, що призводить до складного гемодинамічного процесу, що включає 4 фази [56]. Підчас фази напружування (фаза ІІ) відбувається зменшення переднавантаження ЛШ, при чому спостерігаються певні зміни трансмітрального кровотоку, що дозволяють відрізнити профілі нормального та ПНН ЛШ. Пацієнт повинен генерувати достатнє зусилля для нарощування внутрішньогрудного тиску, у той час як виконавець ЕхоКГ має утримати правильну локалізацію пробного об’єму між кінчиками стулок мітрального клапану підчас проби. Зниження пікової швидкості ранньодіастолічного потоку Е на 20 см/с звичайно є критерієм адекватного зусилля пацієнта (за відсутності рестриктивного типу наповнення ЛШ).
B. Клінічне застосування
Псевдонормальна графіка трансмітрального потоку викликається легким чи помірним підвищенням тиску в ЛП в умовах порушеної релаксації ЛШ. З тієї причини, що проба Вальсальви зменшує переднавантаження підчас фази напруження, профіль ПНН ЛШ змінюється на графіку порушення релаксації ЛШ. Отже, пікова швидкість раннього потоку Е зменшується із пролонгацією DT, в той час як швидкість піку А залишається незмінною або зростає. Таким чином, співвідношення E/A знижується [57]. З іншого боку, при наявності нормального наповнення ЛШ обидві пікові швикості Е та А знижуються пропорційно, а співвідношення Е/А, відповідно, не змінюється. При розрахунку співвідношення Е/А підчас проби Вальсальви повинна використовуватись абсолютна швидкість А (пікова швидкість А мінус швидкість Е перед початком хвилі А). У хворих з кардіальною патологією зниження співвідношення Е/А ≥50% є високо специфічним для підвищення тиску наповнення ЛШ [57], хоча менший відсоток зменшення також не завжди вказує на нормальну діастолічну функцію.
Крім того, відсутність зворотних змін при ПНН чи рестрикції (зворотна рестрикція при пробі Вальсальви трансформується у ПНН) є індикатором незворотної графіки наповнення.
C. Обмеження
Головним обмеженням проби Вальсальви є те, що не всі здатні виконати цю пробу адекватно. Крім того, проба не є стандартизованою. Її клінічне значення у розрізненні нормального та псевдонормального трансмітрального кровотоку знизилася із введенням в клінічну практику запису швидкостей рухів мітрального кільця за допомогою тканинної допплерографії для більш кількісних та простих методик оцінки стану розслаблення ЛШ та визначення тиску наповнення ЛШ. В клінічних закладах з великим потоком хворих проба Вальсальви використовується, як резервний діагностичний інструмент у випадках, коли визначення діастолічної функції лишається неясним після оцінки трансмітрального кровотоку та вимірів швидкостей кільця.
Ключові моменти
(1) Проба Вальсальви виконується шляхом сильного напружування (близько 40 мм Hg) без видоху через ніс чи рот, що призводить до складного гемодинамічного процесу, що включає 4 фази.
(2) У хворих з кардіальною патологією зниження співвідношення Е/А ≥50% є високо специфічним для підвищення тиску наповнення ЛШ [57], хоча менший відсоток зменшення також не завжди вказує на нормальну діастолічну функцію.
V. Кровоток в легеневих венах
A. Отримання та відтворюваність
ІХД кровотоку в легеневих венах виконується в А4С позиції та допомагає в оцінці діастолічної функції ЛШ [22]. Для правильної локалізації пробного об’єму є корисним використання КДК в області впадіння правої верхньої легеневої вени. У більшості пацієнтів найкращі допплерівські профілі отримуються при нахилі датчика ближче до апікальної 5-камерної позиції, коли візуалізується аортальний клапан. Пробний об’єм розміром 2-3 мм розташовується на глибину 0,5 см від війстя у порожнину легеневої вени для оптимального запису допплерівських спектрів. Фільтр сигналу повинен стояти на досить низькому рівні для адекватної реєстрації початку та припинення зворотного потоку в легеневих венах в систолу передсердь (AR). Запис кровотоку в легеневих венах може бути записаний у приблизно 80% амбулаторних пацієнтів [58], хоча у хворих в умовах блоку інтенсивної терапії відтворюваність реєстрації значно нижча. Найбільшою технічною проблемою є артефакти рухів стінки ЛП, викликані скороченням передсердь, що перешкоджає точному відображенню швидкості AR. Рекомендується, щоб запис спектрів отримувався на швидкості розгортки кадрів від 50 до 100 мм/с наприкінці видиху, і щоб виміри були результатом усереднення не менше 3 послідовних циклів.
B. Виміри
Виміри хвиль кровотоку у легеневих венах включають швидкість систолічного потоку (S), пікова швидкість антероградного діастолічного потоку (D), співвідношення S/D, систолічна фракція наповнення (Інтеграл лінійної швидкості потоку (VTI) S/ [VTIS + VTID]), та пікова швидкість зворотного кровотоку в систолу передсердь AR наприкінці діастоли. Інші виміри включають: тривалість хвилі ARdur, різниця тривалості ARdur та тривалості хвилі трансмітрального кровотоку А (Ar – A), та час сповільнення DT хвилі D. Часто реєструється дві систолічних швидкості (S1 і S2), частіше помітних при подовженому інтервалі PQ, тому що S1 відноситься до релаксації передсердя. Для розрахунку швидкості S та співвідношення S/D треба використовувати хвилю S2.
C. Гемодинамічні детермінанти
На швидкість S1 переважно впливають зміни у тиску в ЛП та скорочення і релаксація ЛП [59,60], у той час як хвиля S2 безпосередньо пов’язана з ударним об’ємом та розповсюдженням пульсової хвилі в судинному древі ЛА [59,60]. На швидкість хвилі D впливають зміни в наповненні ЛШ та його податливості, а також паралельні зміни швидкості хвилі Е [61]. На швидкість та тривалість зворотного потоку в систолу передсердь AR впливає кінцево-діастолічний тиск в ЛШ, його переднавантаження та скоротливість ЛП [62]. Зниження податливості (compliance) ЛП та підвищення тиску у ЛП призводить до зменшення швидкості хвилі S та підвищення швидкості хвилі D, що призводить до зниження співвідношення S/D <1, фракції систолічного наповнення <40% [63], та скорочення часу сповільнення DT хвилі D звичайно <150 мс [64]. При підвищенні КДТ ЛШ зростають швидкість та тривалість AR (Рис. 6), так само як і часова різниця між ARdur і тривалістю трансмітральної хвилі А в систолу передсердь Adur [48,65,66]. ФП призводить до притуплення (пологої) хвилі S та відсутності хвилі AR.
D. Нормальні значення
На швидкості кровотоку у ЛВ впливає вік (Таб. 1). У здорових молодих суб’єктів молодше 40 років звичайно спостерігаються виражені хвилі D, які відбивають паралельні у часі трансмітральні хвилі Е. По мірі збільшення віку співвідношення S/D зростає. У здорових суб’єктів швидкості AR можуть зростати з віком, але звичайно не перевищують 35 см/с. Вищі значення свідчать про збільшений КДТ ЛШ [67].
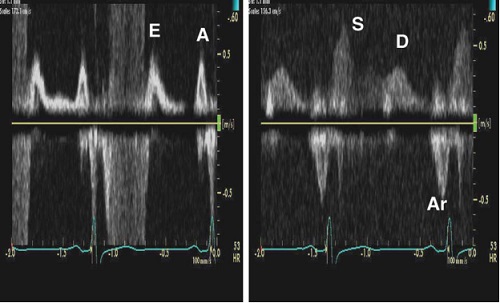
Рис. 6. Запис мітрального діастолічного антероградного кровотоку на рівні кільця мітрального клапана (зліва) та кровотоку в легеневих венах (справа) у пацієнта з підвищеним КДТ ЛШ. Зауважте значно підвищену швидкість зворотного потоку в систолу передсердь AR, що сягає 50 см/с, та її подовжену тривалість ARdur >200 мс порівняно з піздньодіастолічною трансмітральною швидкістю A. Тривалість трансмітральної хвилі А краще всього визначати на рівні мітрального кільця [22].
E. Клінічне застосування у пацієнтів зі зниженою та збереженою ФВ
У пацієнтів із зниженою ФВ ЛШ зниження систолічної фракції антероградного кровотоку <40% пов’язана із зниженням податливості ЛП та збільшенням середнього тиску в ЛП. Це спостереження, втім, має обмежену акуратність у пацієнтів з ФВ ЛШ >50% [48], ФП [68], ураженням мітрального клапану [69], та ГКМП [50]. З іншого боку, різниця ARdur – Adur є особливо корисною, оскільки це є єдиною вік-незалежною ознакою підвищення тиску в ЛШ підчас трансмітральної хвилі А [67], та може допомагати стратифікувати пацієнтів з порушеним розслабленням ЛШ на групи з нормальним тиском наповнення та з підвищенням КДТ ЛШ, але нормальним середнім тиском у ЛП. Таке ізольоване підвищення КДТ ЛШ є першою гемодинамічною аномалією, що відбувається при діастолічний дисфункції. Інші допплерівські ЕхоКГ ознаки, такі як максимальний розмір ЛП, час сповільнення трансмітральної хвилі Е DT, та псевдонормальна графіка наповнення ЛШ можуть вказувати на підвищення середнього тиску у ЛП та більш розвинуту стадію діастолічної дисфункції. Крім того різниця ARdur – Adur лишається точною ознакою у пацієнтів з нормальною ФВ ЛШ [48], патологією мітрального клапану [70], та ГКМП [50]. У підсумок, зауважте, що значення різниці ARdur – Adur >30 мс вказує на підвищення КДТ ЛШ. На відміну від трансмітральних діастолічних швидкостей, не має великої кількості досліджень, що вказували б на якусь прогностичну роль хвиль потоку у ЛВ [71-73].
F. Обмеження
Одне з важливих обмежень в інтерпретації потоків в ЛВ є важкість отримання високоякісного запису, гідного для вимірів. Це особливо стосується швидкості AR, підчас якої скорочення передсердя може створювати низькошвидкісні артефакти, що затьмарюють слабий сигнал швидкості зворотного потоку. Синусова тахікардія та АВ-блокада першого ступеня часто призводять до початку скорочення передсердя, що відбувається до того, як діастолічні трансмітральний та потік у ЛВ повернуться до нульової лінії. Це збільшує ширину трансмітральної хвилі А та зменшує таку зворотного потоку у ЛВ, що робить важкою інтерпретацію різниці ARdur – Adur щодо оцінки підвищення КДТ ЛШ. При ФП втрата скорочення передсердь та погіршення релаксації знижує систолічний потік в ЛВ незалежно від тиску наповнення. При АВ-блокаді першого ступеня з затримкою ≥300 мс потік в ЛВ в ЛП підчас його релаксації (S1) не може бути відокремлений від пізнішого систолічного потоку (S2), або навіть може відбуватися у діастолу.
Ключові моменти
(1) ІХД потоку в ЛВ виконується в А4С позиції та допомагає оцінити діастолічну функцію ЛШ.
(2) Пробний об’єм розміром 2 – 3 мм розташовується на глибіні >0.5 см в порожнині ЛВ для оптимального запису спектральних хвиль потоків.
(3) Вимірювання включають піки швидкостей S і D, співвідношення S/D, систолічну фракцію наповнення та пікову швидкість AR в пізню діастолу. Іншими вимірами є різниця часу між тривалістю хвилі AR та тривалістю трансмітральної хвилі А (ARdur – Adur ).
(4) При зростанні КДТ ЛШ, швидкість та тривалість AR зростає, так само, як і ARdur – Adur.
(5) У пацієнтів із зниженою ФВ ЛЖ зниження систолічної фракції наповнення (<40%) асоціюється зі зниженням податливості ЛП та збільшенням середнього тиску в ЛП.
VI. Швидкість розповсюдження діастолічного кровотоку в ЛШ за даними кольорового М-режиму
A. Отримання, доступність та виміри
Найбільш розповсюдженим підходом для виміру мітрально-апікального розповсюдження потоку є метод нахилу [74,75]. Метод нахилу (Рис. 7) , здається, має найменшу варіабельність [76]. Отримання даних виконується в А4С позиції з використанням КДК у вузькому кольоровому пробному об’ємі з таким налаштуванням підсилення, щоб запобігти шуму. Курсор М-режиму встановлюється по центру стовпа кровотоку від мітрального клапану до верхівки ЛШ. Далі, нульова лінія шкали КДК пересувається до найнижчого ліміту Найквіста так, щоб середня частина кольорового спектру в М-режимі стала синьою. Швидкість розповсюдження потоку (Vp) вимірюється як нахил першої швидкості розвороту спектру підчас раннього наповнення від площини мітрального клапану на відстань 4 см в глибину порожнини ЛШ [75]. Або, в якості альтернативи вимірюється нахил межі появлення кольорового спектру [74]. Vp >50 см/с вважається нормальною [75, 77]. Також за допомогою КДК можливо неінвазивно визначити градієнт тиску від мітрального кільця до верхівки шляхом урахування інерційних сил [78,79], але цей підхід є ускладненим і не придатним для рутинного клінічного застосування.
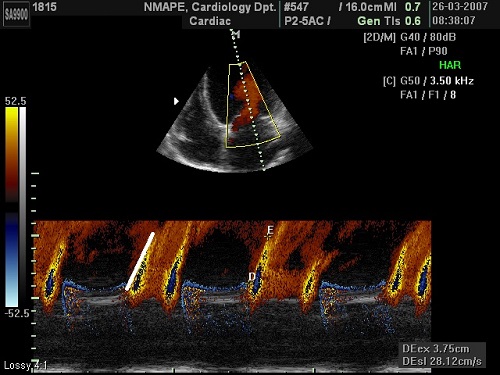
Рис 7. Визначення Vp методом КДК в М-режимі у пацієнта зі зниженою ФВ та порушеною релаксацією ЛШ. Швидкість відповідає нахилу (біла лінія) та становить 28 см/с.
B. Гемодинамічні детермінанти.
Подібно до трансмітрального наповнення, на нормальне внутрішньопорожнинне наповнення ЛШ LV впливає рання хвиля та хвиля наповнення внаслідок скорочення передсердя. Більшість уваги завжди приділялася ранній діастолічній хвилі наповнення, бо вона суттєво змінюється при порушенні релаксації при ішемії та зниженні функції міокарду ЛШ. В нормальному шлуночку рання хвиля наповнення швидко розповсюджується в напрямку верхівки за рахунок градієнту тиску, що існує між базальним відділом та верхівкою ЛШ [80]. Цей градієнт представляє собою насосну силу, що є атрибутом сил відновлення та релаксації ЛШ. При СН та при ішемії міокарду має місце гальмування мітрально-апікального розповсюдження потоку відповідно зниженню всмоктуючого ефекту з боку верхівки [74,81,82]. Втім, оцінка та інтерпретація внутрішньошлуночкового наповнення в клінічній практиці є ускладненою множинністю детермінант, що визначають внутрішньшлуночковий потік. Важливу роль відіграють не тільки градієнт тиску, сили інерції та віскозне тертя, але й геометрія, систолічна функція та скоротлива діссинхронія [83,84]. Більше того, потік відбувається в множинних та швидко змінюючихся напрямах, що формують складну вихрову модель. Уповільнення розповсюдження мітрально-апікального потоку у шлуночку у стані недостатності часткового відбувається завдяки повільно рушаючих в напрямку верхівки кільцевих вихорів [79]. В цих умовах визначення взаємозв’язку між мітрально-аортальним Vp та внутрішньошлуночковим градієнтом тиску є більш складним. Складність внутрішньошлуночкового потоку та обмеження, притаманні сучасним методам візуалізації ускладнюють кількісну оцінку взаємозв’язку профілю внутрішньошлуночкового потоку з міокардіальною функцією ЛШ.
C. Клінічне застосування
Сповільнення швидкості мітрально-апікального розповсюдження діастолічного потоку, визначене за допомогою КДК в М-режимі є добре визначеним напівкількісний маркером діастолічної дисфункції ЛШ. Крім того, можливо використування Vp у поєднанні з хвилею Е трансмітрального наповнення для визначення тиску наповнення ЛШ. Дослідження у пацієнтів показали, що співвідношення пікової швидкості Е до Vp є прямо пропорційним до тиску в ЛП, що, таким чином, означає, що E/Vp може бути використане для визначення тиску наповнення ЛШ саме по собі [75] та у комбінації з IVRT [85]. У більшості пацієнтів зі зниженою ФВ ЛШ наявні множинні ЕхоКГ ознак порушення діастолічної функції ЛШ, та Vp у більшості випадків є надлишковим для визначення діастолічної дисфункції. Втім, у випадках, коли інші допплерівські показники виявляються недостатніми для остаточного рішення, Vp може забезпечити корисну інформацію для визначення тиску наповнення ЛШ, а E/Vp >2,5 говорить про ТЗЛК >15 мм Hg з високою долею точності [86].
D. Обмеження
У пацієнтів з нормальною ФВ ЛШ співвідношення E/Vp має використовуватись з обережністю [86]. Зокрема, у пацієнтів з нормальними порожнинами ЛШ та збереженою ФВ ЛШ при підвищеному тиску наповнення Vp може бути оманливо нормальною [83,84,86]. Крім того, існують літературні дані, що вказують на позитивний вплив переднавантаження на Vp у пацієнтів як з нормальною [87], так і зниженою ФВ ЛШ [88].
Ключові моменти
(1) Отримання виконується в А4С позиції з використанням КДК в М-режимі.
(2) Курсор М-режиму встановлюється по центру стовпа кровотоку від мітрального клапану до верхівки ЛШ зі зсуванням нульової лінії шкали КДК пересувається до найнижчого ліміту Найквіста так, щоб середня частина кольорового спектру в М-режимі стала синьою.
(3) Швидкість розповсюдження потоку (Vp) вимірюється як нахил першої швидкості розвороту спектру підчас раннього наповнення або як нахил межі появлення кольорового спектру від площини мітрального клапану на відстань 4 см в глибину порожнини ЛШ.
(4) Vp >50 см/с вважається нормальною.
(5) У більшості пацієнтів із зниженою ФВ ЛШ Vp є зниженою. У випадку недостатніх даних для висновків за іншими допплерівськими параметрами, співвідношення E/Vp ≥2,5 свідчить про підвищення ТЗЛК >15 мм Hg з достатньою вірогідністю.
(6) У пацієнтів з нормальними об’ємом та ФВ ЛШ, але підвищеним тиском наповнення Vp може бути хибно нормальним.
VII. Рання та пізня швидкості діастолічного руху мітрального кільця за даними тканинної допплерографії
A. Отримання та доступність
ІХ тканинна допплерография (ТД) виконується із апікального доступу для отримання швидкостей руху мітрального кільця [89]. Хоча швидкості руху кільця можуть бути отримані за допомогою кольорового ТД, але цей метод не є рекомендованим, тому що всі дослідження стосовно реферативних значень використовували ІХТД. Пробний об’єм повинен встановлюватись в септального та латерального сегментів мітрального кільця в межах 1 см від прикріплення стулок та налаштовується на покриття 5-10 мм повздовжньої екскурсії кільця як в систолу, так і діастолу. Особливу увагу слід приділити налаштуванням підсилення допплерівського сигналу, тому що сигнали швидкостей мають високу амплітуду.
Більшість сучасних ультразвукових систем мають вже готові налаштування допплерівського сигналу та шкали для правильного отримання швидкостей. Загалом, швидкісна шкала має бути налаштована приблизно на 20 см/с вище та нижче нульової лінії, хоча у хворих з важкою дисфункцією ЛШ швидкості можуть бути значно нижчими (шкала налаштовується для оптимальної візуалізації на 10-15 см/с). При цьому має бути мінімальна ануляція (кут між ультразвуковим променем та напрямом руху мітрального кільця не має перевищувати 200. Хвилі ТД руху мітрального кільця можуть бути отримані у майже всіх пацієнтів (>95%) незалежно від якості двохмірного зображення. Рекомендується запис швидкісних спектрів на швидкості розгортки сигналу 50-100 мм/с наприкінці видиху так, щоб на екрані відображалося в середньому ≥3 послідовних кардіальних циклів.
B. Виміри
Первинні виміри включають систолічну (S), ранню та пізню діастолічну швидкості [90]. Рання діастолічна швидкість мітрального кільця виражається як Ea, Em, E’, чи e’, відповідно, пізня діастолічна швидкість - як Aa, Am, A’, чи a’. Робоча група надає перевагу використанню Е’ та А’, тому що Еа часто також використовується для визначення еластичності артеріальної стінки. Вимірювання часу прискорення та DT сьогодні не представляється таким, що містить цінну клінічну інформацію саме по собі [91], та не потребує рутинного виконання. З іншого боку, при порушенні релаксації ЛШ у особливих популяціях пацієнтів (див. далі) важливу інформацію може забезпечувати часовий інтервал між початком комплексу QRS та початком хвилі Е’. Для оцінки глобальної діастолічної функції ЛШ рекомендовано отримувати та вимірювати швидкості руху мітрального кільця за даними ТД принаймні в септальному та латеральному сегментах мітрального кільця з розрахунком середніх арифметичних значень для урахування регіональних впливів на швидкості та часові інтервали [86,92]. Після отримання швидкостей трансмітрального потоку, швидкостей руху мітрального кільця та часових інтервалів можливий розрахунок додаткових часових інтервалів та співвідношень. До комбінованих показників відносяться співвідношення ранньої та пізньої діастолічної швидкості мітрального кільця Е’/А’ та співвідношення трансмітральної швидкості раннього діастолічного наповнення Е за даними ІХД до швидкості раннього діастолічного руху мітрального кільця Е’ за даними ТД (E/Е’) [90]. Останнє співвідношення відіграє важливу роль у визначенні тиску наповнення ЛШ. Крім того, використовують часовий інтервал TE-Е’, що отримують шляхом різниці між інтервалом від початку комплексу QRS до початку трансмітральної хвилі Е інтервалом від початку комплексу QRS до початку раннього діастолічного руху мітрального кільця(TE-e’), що може забезпечити важливу клінічну інформація додатково до E/Е’ в особливих популяціях, що обговорюються далі. Технічно важливо, щоб співпадали інтервали RR при вимірах обох інтервалів (до початку хвилі Е та початку раннього руху мітрального кільця Е’), та оптимізувати підсилення та налаштування фільтрів, оскільки надмірне підсилення сигналу може завадити коректній ідентифікації початку раннього діастолічного руху мітрального кільця Е'.
C. Гемодинамічні детермінанти
Гемодинамічні детермінанти хвилі Е' включають розслаблення ЛШ (Рис. 8), переднавантаження, систолічна функція та мінімальний тиск в порожнині ЛШ. Значний взаємозв’язок між швидкістю Е' та релаксацією ЛШ спостерігався в дослідженнях як на тваринних моделях [93,94], так і у людей [95–97]. Щодо переднавантаження, тиск наповнення ЛШ має мінімальний вплив на швидкість Е' при порушенні релаксації ЛШ [87,93,94].
З іншого боку, при нормальній або прискореній релаксації ЛШ переднавантаження зростає [93,94,98,99]. Таким чином, у пацієнтів з кардіальною патологією швидкість Е’ може використовуватись для корекції ефектів релаксації ЛШ на трансмітральну швидкість кровоточу Е, а співвідношення E/Е’ може бути використане для оцінки тиску наповнення ЛШ (Рис. 9). Головні гемодинамічні детермінанти хвилі А’ включають скоротливу функцію ЛП та КДТ ЛШ. Таким чином, підвищення скоротливості ЛП веде до підвищення швидкості пізньо-діастолічного руху А’, у той час як підвищення КДТ ЛШ призводить до її зниження [93]. При наявності порушення релаксації ЛШ та незалежно від тиску у ЛП швидкість хвилі Е’ сповільнюється та починається із затримкою, відбуваючись в точці перехресту тисків у ЛП та ЛШ [94,100]. З іншого боку, ранньо-діастолічна хвиля трансмітрального кровоточу Е починається раніше при ПНН або рестриктивного наповненні. Відповідно, часовий інтервал між початком трансмітрального кровопотоку Е та ранньо-діастолічним рухом мітрального кільця Е’ при діастолічній дисфункції подовжується. Дослідження на тваринних моделях [94,100] та у людей [100] показали, що показник TE-Е’) сильно залежить від часової константи релаксації ЛШ та мінімального тиску у ЛШ [100].
D. Нормальні значення
На нормальні значення (Таб. 1) швидкостей мітрального кільця за даними ТД впливає вік подібно до подібно до інших показників діастолічної функції ЛШ. З віком швидкість хвилі Е' знижується, у той час як хвиля А’ та співвідношення E/Е’ зростають [101].
E. Клінічне застосування
Швидкості руху мітрального кільця можуть використовуватись для висновків про стан релаксації ЛШ, а використання комбінованого показника, що залучає трансмітральну ранньо-діастолічну швидкість кровопотоку Е (співвідношення Е/Е’) дозволяє визначати тиск наповнення ЛШ [86,90,97,102–106]. Для досягнення надійних висновків важливо завважити вік конкретного пацієнта, клінічну наявність чи відсутність серцево-судинної патології, та наявність чи відсутність інших патологічних знахідок підчас ЕхоКГ. Таким чином, Е’ та співвідношення E/Е’ є важливими показниками. Але їх не слід використовувати, як єдині маркери діастолічної функції ЛШ.
Для визначення тиску наповнення ЛШ слід використовувати середнє значення швидкості Е’, отримане зі значень на септальному та латеральному сегментах мітрального кільця в А4С позиції. Оскільки септальна швидкість Е’ звичайно є нижчою за таку на латеральному сегменті мітрального кільця, співвідношення Е/Е’, отримане з септального сегменту кільця звичайно є вищим порівняно із співвідношенням, отриманим з латерального сегменту, тому для різних сегментів мають використовуватись різні нормативні значення. Хоча поодинокі виміри тільки латерального чи тільки септального сегменту мітрального кільця інколи використовуються у пацієнтів з нормальною або порушеною глобальною систолічною функцією ЛШ, при наявності порушень регіональної скоротливості обов’язково має використовуватися середнє арифметичне значень швидкостей Е’ з латерального та септального сегментів мітрального кільця (Рис. 10) [86]. Крім того, корисно враховувати ступінь співвідношення. При використанні септального співвідношення E/Е’ значення <8 звичайно асоціюється з нормальним тиском наповнення, у той час як значення >15 є асоційованим з чітко підвищеним тиском наповнення ЛШ [97]. При значенні співвідношення від 8 до 15 для точнішого висновку про тиск наповнення ЛШ повинні залучатися інші ехокардіографічні показники. Декілька недавніх досліджень показали, що у пацієнтів з нормальною ФВ ЛШ саме дані латерального сегменту мітрального кільця (E/Е’ та Е’/Е’) найкраще корелюють з тиском наповнення ЛШ та інвазивними показниками жорсткості ЛШ [86,106].
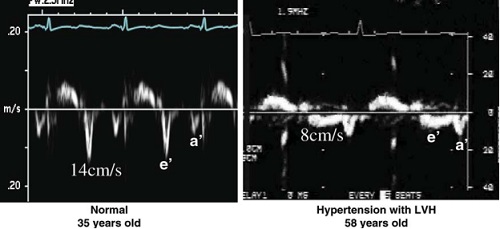
Рис. 8. Тканинна допплерографія (ТД) рухів латерального сегменту мітрального кільця у здорового суб’єкту 35 років (зліва) (Е’=14 см/с) та у пацієнта 58 років з артеріальною гіпертензією, гіпертрофією ЛШ та порушення релаксації ЛШ (справа) (Е’=8 см/с).
Ці дослідження схиляються в бік використання ТД сигналів руху саме латерального сегменту мітрального кільця в цій популяції.
Показник часового інтервалу TE-Е’ є особливо корисним в ситуаціях, в яких використання піку Е’ обмежене, при чому для визначення цього показника середнє арифметичне значень чотирьох сегментів мітрального кільця з А4С та А2С позицій є більш точним порівняно з поодиноким виміром [100]. В клінічних умовах визначення цього показника включає пацієнтів з нормальною скоротливою функцією [100] та суб’єктів з патологією мітрального клапану [69], а також у випадках, коли значення співвідношення Е/Е’ знаходиться у межах від 8 до 15 [107]. Зокрема, співвідношення IVRT/TE-Е’ <2 має достатню точність у визначенні пацієнтів з підвищеним тиском наповнення ЛШ [100].
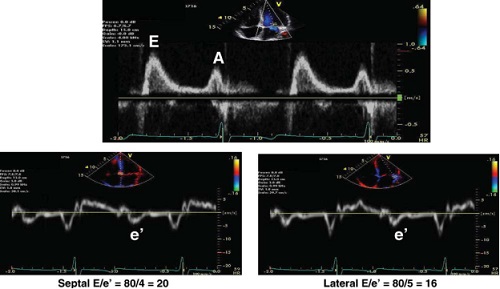
Рис. 9. Трансмітральний кровоток (зверху), ТД сигнали рухів септального (внизу зліва) та латерального (внизу справа) сегментів мітрального кільця у 60-річного пацієнта з СН та нормальною ФВ ЛШ. Співвідношення E/Е’ було суттєво підвищеним при використанні швидкостей Е’ обох сегментів мітрального кільця.
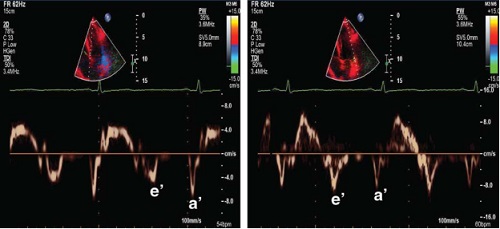
Рис. 10. ТД рухів септального (зліва) та латерального (справа) сегментів мітрального кільця у пацієнта з передньо-перегородковим інфарктом міокарду. Зауважте різницю між септальною (5 см/с) та латеральною (10 см/с) швидкостями ранньо-діастолічного руху Е’. У таких пацієнтів обов'язково треба використовувати середнє арифметичне значення септальної та латеральної швидкостей Е’ для найбільш точної оцінки діастолічної функції ЛШ та тиску його наповнення.
F. Обмеження
Існують як технічні, так і клінічні обмеження. Технічних обмежень стосуються необхідність певної уваги до правильної локалізації пробного об’єму, а також адекватних підсилення сигналу, налаштування фільтрів та досягнення мінімального кута між променем та напрямком руху мітрального кільця. У досвідчених операторів показники звичайно мають високу відтворюваність з невеликою варіабельністю. Оскільки визначення часових інтервалів виконується в різни кардіальні цикли, це вносить додаткову варіабельність. Це у певній мірі обмежує їх використання в вибраних клінічних обставинах, у яких допплерівські кількісні показники можуть бути ненадійними.
Є декілька клінічних обставин, в яких визначення швидкостей руху мітрального кільця та співвідношення Е/Е’ не повинно використовуватись. У здорових суб’єктів швидкість хвилі Е’ позитивно пов'язана з переднавантаженням [98], та співвідношення Е/Е’ може не давати надійної інформації щодо тиску наповнення. Цих індивідів можна розпізнати по анамнезу, нормальними структурними та функціональними кардіальними показниками, та більш раннім (або одночасним) початком ранньо-діастолічного руху мітрального кільця Е’ порівняно з трансмітральною хвилею кровопотоку Е [100]. Крім того, швидкість хвилі Е’ звичайно знижується у пацієнтів зі значним звапненням мітрального кільця, при наявності вшитих кілець після хірургічної пластики мітрального кільця, при мі тральному стенозі, та наявності протезу мітрального клапану.
Хвиля Е’ збільшується у пацієнтів з помірною та важкою первинною МР при нормальній релаксації ЛШ завдяки збільшенню кровопотоку через регургітуючий мітральний клапан. У цих пацієнтів співвідношення E/Е’ не повинне використовуватись, а натомість може використовуватись співвідношення IVRT/TE-Е’ [69].
У пацієнтів з конструктивним перикардитом септальна швидкість Е’ звичайно підвищена, в основному завдяки збереженій повздовжній експансії ЛШ, що компенсує обмежену латеральну та передньо-задню діастолічну екскурсію. У цій ситуації швидкість Е’ латерального кільця може бути меншою за таку септального сегмента, а співвідношення Е/Е’ може зворотньо співвідноситися до тиску наповнення ЛШ, що отримало назву анулярного парадоксу [108].
Ключові моменти
(1) ІХТД виконується з апікальних доступів для отримання швидкостей рухів мітрального кільця.
(2) Пробний об’єм має встановлюватися в діапазоні 1 см в межах септального та латерального сегментів (точок прикріплення мітральних стулок).
(3) Рекомендовано, щоб записи спектрів отримувалися на швидкості розгортки від 50 до 100 мм/с наприкінці видоху, та щоб виміри відбивали середнє арифметичне трьох послідовник циклів.
(4) Первинні виміри включають систолічну, та ранню (Е’) і пізню (А’) діастолічні швидкості.
(5) Для оцінки глобальної діастолічної функції ЛШ рекомендується отримувати та проводити виміри сигналів за даними ТД принаймні на латеральному та септальному сегментах мітрального кільця з розрахунком середнього арифметичного значення.
(6) У пацієнтів з кардіальною патологією Е’ може використовуватись для корекції впливу релаксації ЛШ на трансмітральну швидкість Е у вигляді комбінованого співвідношення E/Е’ для оцінки тиску наповнення ЛШ.
(7) Співвідношення E/Е’ не є точним показником тиску наповнення ЛШ у здорових суб’єктів або у пацієнтів з важким звапненням мітрального кільця, вадами мітрального клапану та констриктивним перикардитом
VIII. Виміри деформації
Strain означає деформацію, та може бути розрахована з використанням різних формул. В клінічній кардіології strain часто виражається, як відсоток, або фракційний strain (strain Лагранжа). Систолічна деформація представляє собою відсоток скорочення, коли вимір виконується по довгій вісі, та відсоток радіального потовщення – по короткій. Систолічна деформація представляє собою швидкість скорочення чи потовщення міокарду, відповідно. Міокардіальна деформація та швидкість деформації (strain rate) є прекрасними параметрами для кількісної оцінки регіональної скоротливості, та можуть також забезпечувати важливу інформацію для оцінки діастолічної функції. Підчас кардіального циклу міокард ЛШ проходить через складну 3-вимірну деформацію, що веде до множинних локальних зрушень (зсувів, деформацій), коли ділянки міокарду зсуваються одна відносно другої. Втім, сьогодні такий складний аналіз за допомогою ЕхоКГ ще не є доступним. Традиційно деформаціям при подовженні та потовщенні присвоюють позитивні значення, а деформаціям при скороченні та потоншенні – негативні. До недавнього часу єдиним клінічним методом кількісної оцінки деформації міокарду була магніто-резонансна візуалізація з тканинними позначками, але складність та висока вартість цієї методики обмежує її використання до меж клінічних досліджень. Оцінка деформації міокарду за допомогою ТД була введена в клініку як рутинний клінічний метод та ретельно вивчалася на предмет оцінки регіональної систолічної функції [109,110]. Деформація також може бути оцінена за допомогою методики «speckle-tracking» в В-режимі, нової методики, що вимірює деформацію, відстежуючи гіперехогенні сигнали (speckles) в сірій шкалі ехокардіографічного зображення міокарду [111,112]. Ці сигнали «speckles» відіграють роль натуральних акустичних маркерів, що можна відстежити від кадру до кадру, а швидкість їх зміщення та деформація розраховуються автоматично по відстаням між окремими сингалами. Ця методика не залежить від кута між променем ультразвуку та напрямом руху. Тому виміри можуть отримуватися одномоментно з різних ділянок в межах сектора сканування. Треба зауважити, що цим фактом методика позитивно відрізняється від оцінки деформації допплером, що є дуже чутливим до кута між ультразвуковим променем та напрямом руху міокарду. Крім того, проблеми з тканинним допплером та його використанням в оцінці деформації є значні фонові шуми та дрейф сигналу.
Ехокардіографія з використанням техніки «спекл-трекінг» має обмеження у відносно низькій частоті обновлення зображення. Декілька досліджень дозволили припустити, що деформація та швидкість деформації міокарду (strain та strain rate) можуть надати унікальну інформацію щодо діастолічної функції. До такої інформації відноситься кількісна оцінка постсистолічної деформації міокарду, а саме вимірювання скорочення ішемізованного міокарду після викиду [113] та регіональна діастолічна швидкість деформації, що може використовуватись для оцінки діастолічної жорсткості підчас оглушення та інфаркту [114,115]. Є свідоцтва з тваринних моделей, що сегментарна швидкість деформації міокарду підчас ранньої діастоли корелює з ступенем інтерстиціального фіброзу [115]. Подібно до цієї тези, регіональні Рекомендації з оцінки діастолічної функції ЛШ за даними ЕхоКГ [177] свідчать, що різниця в часі від скорочення до релаксації міокарда, визначена за допомогою strain rate може ідентифікувати ішемізовані сегменти [116]. Певні дослідження показали значний взаємозв’язок між сегментарною [117] та глобальною [118] ранньою діастолічною швидкістю деформації та часовою константою релаксації ЛШ. Більш того, недавнє дослідження, в якому комбіновано оцінювалася глобальна швидкість деформації міокарду підчас періоду ізоволюмічної релаксації за технікою спекл-трекінг та трансмітральні швидкості кровотоку, показало, що співвідношення ранньої трансмітральної хвилі Е до глобальної швидкості деформації міокарду було добрим предиктором тиску наповнення ЛШ у пацієнтів, у яких співвідношення E/Е’ не дозволяло зробити чіткі висновки, та було більш точним порівняно з E/Е’ у пацієнтів з нормальною ФВ ЛШ та пацієнтів з регіональними порушеннями міокардіальної функції [118]. Таким чином, оцінка діастолічної функції шляхом візуалізації деформації міокарду є багатообіцяючою перспективою, але потребує більше досліджень своєї потенційної клінічної ролі. Сьогодні імпульсно-хвильова допплерографія кровотоку та руху міокарду є переважними початковими ехокардіографічними методиками для оцінки діастолічної функції ЛШ.
IX. Розкручування лівого шлуночка
Обертальний рух (кручення) ЛШ відбувається завдяки косо розташованим фібрилам субепікардіального шару міокарда, що пролягає в напрямку верхівки по часовій стрілці. Субепікардіальні волокна домінують над субендокардіальними, що формують спіраль в протилежному напрямку. Таким чином, при погляді на ЛШ з верхівки в напрямку базальних відділів верхівка виконує систолічну ротацію проти часової стрілки, а базальний відділ ЛШ обертається по часовій стрілці.
Розкручування починається в пізню систолу, але основний його етап відбувається підчас ізоволюмічного розслаблення та в більшій степені закінчується в момент відкриття мітрального клапану [119]. Діастолічне розкручення представляє собою пружну віддачу завдяки вивільненню відновлюваних сил, що генерувалися підчас попередньої систоли. Швидкість розкручення часто позначається як швидкість віддачі. Такий поворот ЛШ, здається, відіграє важливу роль у нормальній систолічній функції ЛШ, у той час як розкручення допомагає ефективнішому наповненню ЛШ за рахунок створення додаткових всмоктувальних сил [119,120]. Було припущено, що зменшення розкручування ЛШ з ослабленням або втратою діастолічного всмоктування посилює діастолічну дисфункцію при кардіальній патології [120–123]. Хоча діастолічна дисфункція і асоціюється з нормальними віковими змінами (старінням), але при вікових змінах не спостерігається зменшення діастолічного розкручування [124].
A. Клінічне застосування
До сьогодні наше розуміння щодо кількісного визначення скручення та розкручення ЛШ та його ротації було дуже обмеженим та слабо могло втілитися в рутинну клінічну практику, тому що вимірювання скручення ЛШ можливе тільки за допомогою міченої магнитно-резонансної томографії та інших складних методик [120–126]. Але, зважаючи на недавнє впровадження ехокардіографічної методики «спекл-трекінг», сьогодні стало можливим кількісно визначати ротацію, скручування та розкручування ЛШ в щоденній клінічній практиці [127,128]. Скручування ЛШ розраховується як різниця між базальною та апікальною ротацією, що визначається по короткій вісі ЛШ. Для виміру базальної ротації площина зрізу встановлюється трохи дистальніше мітрального кільця, а для апікальної ротації – трохи проксимальніше рівня кінцево-систолічного перекриття просвіту апікальної частини порожнини ЛШ. Клінічне значення оцінки розкручення ЛШ досі не визначене. При оцінці скручування та розкручення ЛШ у пацієнтів з діастолічною дисфункцію або діастолічною серцевою недостатністю, швидкість як скручування, так і розкручення були збереженими [129,130], та не було виявлено достовірного зв’язку з часовою константою розслаблення ЛШ [129]. З іншого боку, у пацієнтів зі зниженою ФВ ЛШ ці значення були значно знижені. На тваринних моделях, та в обох групах з серцевою недостатністю, найсильніша асоціація спостерігалася з кінцево-систолічним об’ємом ЛШ та скручуванням [129], натякаючи, що швидкість розкручування ЛШ найкраще відбиває взаємозв’язок між систолічною компресією та ранньою діастолічної віддачею. В заключення слід зауважити, що виміри швидкостей скручування та розкручення ЛШ можуть стати важливою частиною оцінки діастолічної функції в майбутньому, хоча сьогодні вони ще не можуть бути рекомендовані для рутинного клінічного ви користування, та потрібні додаткові дослідження для визначення їх потенційного місця у клінічному застосуванні.
B. Обмеження
Складність представляє вибір площини зображення, тому потрібне подальше клінічне тестування ЕхоКГ з використанням «спекл-трекінг» для визначення відтворюваності вимірів, що отримуються з шлуночків з різною геометрією. Якість «спекл-трекінг» може бути субоптимальною в базальних відділах ЛШ, що вносить значну варіабельність в виміри [128].
X. Оцінка розслаблення лівого шлуночка
A. Пряме визначення
1. IVRT
При порушенні розслаблення міокарду, тиск в ЛШ підчас періоду ізоволюмічної релаксації падає повільніше, що призводить до збільшення часу до моменту падіння тиску в ЛШ нижче рівня в ЛП. Таким чино, затримується відкриття мітральног клапану, що призводить до пролонгації IVRT. IVRT легко вимірюється за допомогою допплерівської ЕхоКГ, як обговорювалося в попередніх розділах. Втім, сам по собі IVRT має обмежену точність, зважаючи на змішаний вплив на нього переднавантаження, що діє у напрямку, протилежному порушенню релаксації ЛШ. Можливо комбінувати IVRT з неінвазівними індексами кінцево-систолічного тиску в ЛШ та тиску в ЛП для розрахунку τ (IVRT/[ln кінцево-систолічний тиск в ЛШ – ln тиск в ЛП]). Цей підхід був виправданий [131] та може використовуватися для кількісного розрахунку τ замість якісної оцінки релаксації ЛШ.
2. Постійно-хвильовий спектр аортальної регургітації
Миттєвий градієнт тиску між аортою та ЛШ підчас діастоли може бути розрахований за допомогою постійно-хвильової допплерографії (ПХД) спектру аортальної регургітації. Оскільки флуктуації тиску в аорті підчас IVRT є настільки малими, що їх можна зневажити, а також тому, що мінімальний тиск в ЛШ звичайно низький, тиск в ЛШ підчас IVRT може бути розрахований з ПХД спектру потоку аортальної регургітації, а саме: середній градієнт між аортою та ЛШ та градієнт КДТ ЛШ, dP/dtmin (4V2 x 1,000/20, де V швидкість аортальної регургітації у м/с через 20 мс після початку потоку регургітації, а t (часовий інтервал між початком аортальної регургітації та досягненням швидкості регургітації, що віповідає значенню [1 -1/e]1/2 від максимальної швидкості). Розрахунок τ перевірявся у дослідженні на тваринах [132], але клінічний досвід на людях є обмеженим лише невеликою кількістю пацієнтів [133].
3. Постійно-хвильовий сигнал мітральної регургітації
Використовуючи модифіковане рівняння Бернуллі, за допомогою ПХД мжна визначити максимальний та середній градієнти тиску між ЛШ та ЛП у хворих з наявною МР, що добре корелює з такими, що отримані підчас катетеризації серця [134]. Рівняння для розрахунку dP/dtmin: dP/dtmin (мм Hg/с) = [4(VMR2)2 – 4(VMR1)2] x 1,000/20, де VMR1 та VMR2 є швидкостями МР (м/с) з інтервалом 20 мс. Спрощений підхід для розрахунку τ з потоку МР є таким: τ = часовий інтервал між точкою –dP/dtmin до точки, в якій швидкість МР дорівнює значенню (1/e)1/2 від швидкості МР в точці –dP/dtmin. Зважаючи на наявність простіших методів оцінки релаксації міокарду, як аортальна, так і мітральна регургітація в рутинній клінічній практиці використовуються рідко.
Окрім вище описаних розрахунків, певну цінність має оцінка профілю (морфології) допплерівського спектру в ПХД. Наприклад, для МР, круте наростання швидкості з послідовним пологим сповільненням кровотоку після досягнення пікової швидкості є характерним для явної «V»-подібної кривої тиску та підвищеного середнього тиску в ЛП. З іншого боку, округлений рівнобедрений спектр з повільним наростанням та зменшенням швидкості скоріше свідчень про систолічну дисфункцію ЛШ та порушення його релаксації. Для аортальної регургітації при відсутності значної структурної патології аортального клапану (у хворих з помірною аортальною недостатністю), швидке сповільнення пікової швидкості та короткий час напівзниження тиску звичайно вказують на швидке зростання діастолічного тиску в ЛШ завдяки його підвищеній жорсткості.
B. Сурогатні виміри
1. Швидкості трансмітрального кровотоку
Коли релаксація міокарда є значно сповільненою, спостерігається зниження співвідношення Е/А<1 та пролонгація DT >220 мс. Крім того, при наявності брадікардії можна побачити характерний середньо-діастолічний кровопотоку, що спостерігається після кровопотоку раннього наповнення Е, завдяки прогресивному падінню діастолічного тиску в ЛШ, пов’язаному з сповільненим розслабленням ЛШ. Втім, підвищений тиск наповнення може маскувати ці зміни швидкостей трансмітрального кровопотоку. Таким чином, співвідношення E/A<1 та DT >240 мс мають високу специфічність для виявлення порушення релаксації ЛШ, але можуть спостерігатися при нормальному або підвищеному тиску наповнення ЛШ, залежно від того, наскільки сповільненою є релаксація ЛШ. Зважаючи на те, що порушення релаксації є самою ранньою патологічною ознакою при більшості серцевих хвороб, її наявність слід передбачати у більшості, якщо навіть не у всіх пацієнтів з діастолічної дисфункцією.
2. Спектри руху мітрального кільця за даними тканинного допплера
Тканинний допплерівський пік Е’ є набагато чутливішим параметром, що вказує на аномальну релаксацію міокарда порівняно з даними трансмітрального кровопотоку. Декілька досліджень на тваринних моделях та у людей продемонстрували значущий кореляційний взаємозв’язок між Е’ та τ (див. попереднє обговорення). У більшості пацієнтів із зниженням швидкості Е’ латерального сегменту мітрального кільця <8.5 см/с або септального сегменту мітрального кільця <8 см/с наявне порушення релаксації ЛШ. Втім, для більш надійного заключення важливо визначати, чи Е’ є меншим, ніж середнє значення мінус 2 стандартних відхилення для даної вікової групи конкретного пацієнта (див. Таб. 1).
При наявності порушення релаксації міокарду інтервал TE-e’ подовжується та добре корелює з τ та мінімальним тиском в ЛШ. Втім, цей підхід демонструє більшу варіабельність порівняно з ізольованим вимірюванням швидкості E’, та буває потрібним тільки в нечастих клінічних випадках (див. попереднє обговорення).
3. Vp у кольоровому М-режимі
Нормальне значення Vp складає ≥50 см/с та корелює з швидкістю міокардіальної релаксації. Втім, Vp може збільшуватись у пацієнтів нормальними об’ємами ЛШ та ФВ ЛШ, незважаючи на порушену релаксацію.
Таким чином, Vp є набагато надійнішим у якості показника релаксації ЛШ у пацієнтів із зниженою ФВ ЛШ та дилатацією ЛШ. У інших груп пацієнтів бажано використовувати інші показники.
Ключові моменти
(1) IVRT само по собі має обмежену акуратність, зважаючи на перехресний вплив на нього переднавантаження, що перекриває ефект порушеної релаксації ЛШ.
(2) У більшості пацієнтів із зниженням швидкості ранньо-діастолічного руху мітрального кільця Е’ в латеральному сегменті <8,5 см/с чи в септальному сегменті <8 см/с наявне порушення релаксації ЛШ.
(3) Vp є найбільш надійним показником релаксації ЛШ у пацієнтів із зниженною ФВ та дилатацією ЛШ. В інших групах пацієнтів слід користуватися іншими показниками.
(4) Для дослідницьких цілей для розрахунку τ можна використовувати ПХД сигнали мітральної та аортальної регургітації.
XI. Визначення жорсткості лівого шлуночка
A. Пряме визначення
Діастолічні криві тиску-об’єму можуть бути отримані з одночасних високоякісного запису тиску та допплерографії трансмітрального кровопотоку, при цьому отримані швидкості наповнення (за рахунок множення допплерівської кривої на діастолічну площу мітрального отвору) інтегруються для отримання кумулятивних об’ємів наповнення та нормалізуються до ударного об’єму за даними двомірної ЕхоКГ [135,136]. З використанням цієї техніки можна розрахувати константу жорсткості камери ЛШ. Визначення кінцево-діастолічної податливості (комплаєнсу), що є реципрокною до жорсткості ЛШ, також можливо з однієї координати кривої тиску та об’єму наприкінці діастоли, використовуючи ЕхоКГ для КДО ЛШ та визначення КДТ ЛШ, але цей метод може призводити до значної помилки у пацієнтів з великим ступенем діастолічної функції.
B. Сурогатні виміри
1. DT раннього трансмітрального кровотоку Е
Пацієнти із станами, асоційованими з підвищеною жорсткістю ЛШ мають більш швидкі рівні сповільнення раннього наповнення ЛШ та коротші значення DT [137]. Теоретичний аналіз передбачає, що при відносно постійному тиску в ЛП підчас раннього наповнення ЛШ DT є пропорціональним зворотному квадратному кореню індекса жорсткості ЛШ [138]. Це припущення підтверджується недавніми дослідженнями, що показали, що жорсткість ЛП не змінюється підчас періоду сповільнення раннього наповнення ЛШ [139]. Експериментальні спостереження та обмежені даних спостережень у людей підтвердили теоретичні розрахунки (жорсткість [мм Hg / мм], розраховується як KLV = [70 мс/(DT – 20 мс)]2 [140,141]. Для досягнення більшої точності потрібне також урахування віскозної еластичності та релаксації ЛШ [142]. У підсумку, мітральний час DT є важливим параметром, що повинен враховуватись при винесенні висновку про жорсткість ЛШ, особливо у хворих із значним сповільненням ЛШ.
2. Тривалість хвилі А
Скорочення ЛП створює хвилю тиску-швидкості, що входить в ЛШ. Хвиля рухається через приносний тракт шлуночка та відбивається від верхівки у напрямку аортального клапану. Час, потрібний на розповсюдження хвилі тиску-швидкості через шлуночок, визначається як транзитний час хвилі А, та може бути визначений з використанням імпульсно-хвильвової допплерографії (ІХД) [143]. Цей часовий інтервал добре корелює з пізньою жорсткістю та КДТ ЛШ, виміряними високоточним катетером при катетерізації [143,144]. Обмеження цього підходу включає його залежність від місця встановлення пробного об’єму при допплерографії та геометрії ЛШ.
XII. Діастолічний стрес-тест
У багатьох пацієнтів з діастолічної дисфункцією з'являються симптоми, переважно при навантаженні, в наслідок підйому тиску наповнення ЛШ, потрібного для підтримання адекватного наповнення ЛШ та ударного об’єму. Таким чином, корисно оцінювати також тиск наповнення ЛШ підчас навантаження, подібно до того, як використовують проби з навантаженням у хворих з ішемічною хворобою серця або патологією мітрального клапана. Для цієї мети використовують E/Е’ (Рис. 11). У суб’єктів з нормальним розслабленням ЛШ, швидкості Е та Е’ збільшуються пропорційно (Таб. 2), а співвідношення E/Е’ лишається незмінним чи зменшується [145]. Втім, у пацієнтів з порушенням розслаблення міокарду, збільшення швидкості Е’ при навантаженні відбувається в меншій ступені, ніж швидкості раннього трансмітрального потоку Е, що призводить до збільшення співвідношення Е/Е’ [146]. У зв’язку з цим було показано, що співвідношення E/Е’ достовірно корелює з тиском наповнення ЛШ підчас навантаження при одночасному проведенні допплерівської ЕхоКГ та катетеризації серця [147]. Крім того, час сповільнення раннього трансмітрального кровопотоку DT у здорових суб’єктів підчас навантаження зменшується незначно, у той час, як у пацієнтів з підвищеним тиском наповнення ЛШ DT зменшується більше, ніж на 50 мс. У кардіологічних хворих підчас навантаження швидкість раннього трансмітрального кровопотоку Е зростає та лишається підвищеною ще декілька хвилин після припинення вправи, у той час як швидкість Е’ лишається зниженою як до навантаження, так і підчас навантаження та реституції. Таким чином, швидкості Е та Е’ можуть бути записані після навантаження після аналізу регіональної скоротливості стінок в В-режимі. Далі, відстрочений запис допплерівських швидкостей дозволяє запобігти зливання швидкостей Е та А, що часто відбувається при підвищенні частоти серцевих скорочень. Навантаження звичайно виконується за допомогою протоколу з лежачим велоергометром, при цьому також записують спектр ТР для оцінки систолічного тиску в ЛА в спокої, підчас навантаження та реституції. Також для оцінки діастолічної функції виконувалася стрес-ехокардіографія з добутаміном, підчас якої появлення рестриктивного наповнення ЛШ асоціювалося з негативною прогностичною інформацією [148].
Проба з навантаженням є найбільш корисною у пацієнтів з нез'ясованою одишкою при навантаженні з легкою діастолічною дисфункцією та нормальним тиском наповнення в спокої. Втім, брак клінічних даних та потенційні обмеження у пацієнтів з регіональною дисфункцією ЛШ, патологією мітрального клапана та фібриляцією передсердь сьогодні поки що не дозволяють рекомендувати стрес-ехокардіографію для рутинного застосування.
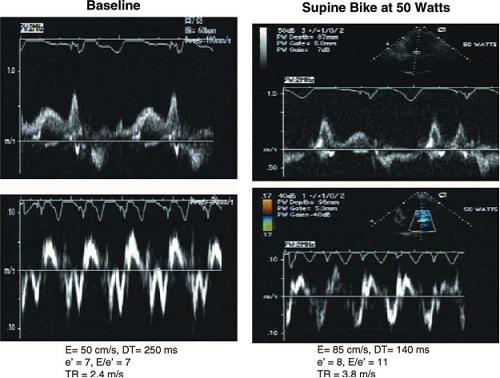
Рис. 11. Запис допплерографії підчас навантаження у пацієнта із зниженим діастолічним резервом. На виході допплерограма трансмітрального кровопотоку вказує на порушення релаксації ЛШ із співвідношенням E/Е’=7, та піковою швидкістю потоку ТР 2,4 м/с (Систолічний тиск у легеневій артерії =28 мм Hg). Підчас проби з фізичним навантаженням з лежачим велоергометром відбулося зростання швидкості Е та співвідношення Е/А із одночасним скороченням DT. Співвідношення E/Е’ при навантаженні складає 11, а систолічний тиск в ЛА збільшився до ≥60 мм Hg (Пікова швидкість потоку ТР = 3,8 м/с).
Таб. 2. Зміни швидкостей трансмітрального кровопотоку та рухів мітрального кільця за даними ТД у здорових суб’єктів підчас фізичного навантаження (середній вік 59±14 років) [145].
|
Показник
|
Базальний рівень
|
Фізичне навантаження
|
|
E (см/с)
|
73±19
|
90±25
|
|
A (см/с)
|
69±17
|
87±22
|
|
DT (мс)
|
192±40
|
176±42
|
|
Е’ (см/с)
|
12±4
|
15±5
|
|
E/Е’
|
6,7±2.2
|
6,6+2,5
|
XIII. Інші причини симптомів серцевої недостатності у пацієнтів з нормальною фракцією викиду
A. Хвороби перикарду
Підчас обстеження хворих з клінічним діагнозом СН із збереженою ФВ ЛШ важливо пам’ятати про можливість констриктивного перикардиту, тому що цей стан в більшості випадків є цілком виліковним. Оскільки тиск наповнення ЛШ при констриктивному перикардиті є підвищеним, графіка трансмітрального кровопотоку відбиває псевдонормальне або рестриктивне наповнення з Е/А>1 та нормальним або скороченим DT, хоча у деяких хворих швидкість піку Е може бути нижче швидкості А, особливо підчас вдиху. Крім того, типово, у пацієнтів з конструктивним перикардитом спостерігаються респіраторні варіації швидкості трансмітрального кровопотоку Е: зростання швидкості ≥25% підчас видихання [149]. Втім, до 50% пацієнтів з констриктивним перикардитом дихальні варіації швидкості Е складають <25%. З іншого боку, у пацієнтів з респіраторним дистресом, що спостерігається при астмі, синдромі ночного апное, хронічних обструктивних захворюваннях легень та ожирінні, можуть спостерігатися підвищені респіраторні коливання трансмітральної швидкості Е завдяки збільшеним коливанням внутрішньо грудного тиску.
Для диференційного діагнозу при встановленні констриктивного перикардиту необхідним є запис кровопотоку в печінкових венах [150]. У пацієнтів з констриктивним перикардитом печінкові вени звичайно розширені, та в них спостерігається виражений діастолічний зворотний потік підчас видиху. У пацієнтів з рестриктивною кардіоміопатією навпаки діастолічний зворотний потік більш виражений підчас вдиху, у той час як у пацієнтів з легеневою патологією перенаповнення правих відділів серця відбувається підчас вдиху, що видно по великому збільшенню швидкостей потоку в нижній та верхній порожнистих венах. У пацієнтів з констриктивним перикардитом, ускладненим фібриляцією передсердь, все ж таки лишаються типові ЕхоКГ ознаки в В-режимі, але для виявлення коливань швидкостей підчас допплерографії може потребувати більше часу [151].
Також важливо отримати та аналізувати швидкості мітрального кільця за допомогою тканинної допплерографії. У пацієнтів з рестриктивною кардіоміопатією має місце порушення релаксації та загальної міокардіальної функції, що призводить до зниження швидкостей S’ та Е’, та збільшення часового інтервалу TE-Е’ [152–154]. Навпаки, у пацієнтів з констриктивним перикардитом повздовжня екскурсія атріо-вентрикулярного кільця є звичайно збереженою (Рис. 12). Швидкість септального сегменту мітрального кільця Е’≥7 см/с є високо точною диференційно-діагностичною межею для диференціації констриктивного перикардиту від рестриктивної кардіоміопатії. Обмеження використання Е’ з'являються у пацієнтів із значним звапненням атріо-вентрикулярних кілець та у хворих із супутньою патологією міокарду, коли швидкість руху зменшена за рахунок патології міокарда незалежно від наявності перикардіальної констрикції. Недавні літературні дані показали, що у деяких пацієнтів також можливі дихальні коливання швидкості Е’, але ці коливання носять зворотний характер відносно швидкостей трансмітрального кровопотоку [155]. Крім того, у пацієнтів з патологією міокарда звичайно зменшена систолічна деформація, в той час як у пацієнтів з конструкцією вона звичайно є збереженою (Таб. 3).
Таб. 3. Диференціальна діагностика констриктивного перикардиту та рекстриктивної кардіоміопатії.
|
Показник
|
Рестрикція
|
Констрикція
|
|
Септальний рух
|
Нормальний
|
Респіраторні коливання
|
|
Трансмітральний кровоток E/A
|
>1,5
|
>1,5
|
|
Трансмітральний DT (см)
|
<160
|
<160
|
|
Респіраторні варіації трансмітрального кровотоку
|
Відсутні
|
Звичайно присутні
|
|
Допплер печінкових вен
|
Інспіраторна реверсія діастолічного потоку
|
Експіраторна реверсія діастолічного потоку
|
|
Септальна швидкість Е’
|
Звичайно <7 см/с
|
Звичайно >7 см/с
|
|
Латеральна швидкість Е’
|
Вище септальної швидкості Е’
|
Нижче септальної швидкості Е’
|
|
Септальна шлуночкова деформація (strain)
|
Знижена
|
Звичайно нормальна
|
Ключові моменти. У пацієнтів з клінічними симптомами серцевої недостатності при нормальній ФВ ЛШ рестриктивне наповнення ЛШ, значний діастолічний зворотний потік в печінкових венах підчас видиху, та нормальні або збільшені швидкості мітрального кільця за даними тканинного допплера повинні навести на підозри на констриктивний перикардит, навіть коли респіраторні коливання трансмітрального кровопотоку відсутні або не є чіткими.
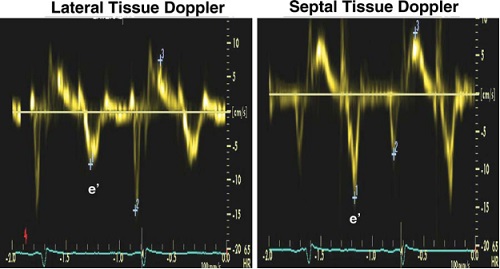
Рис. 12. Тканинна допплерографія швидкостей руху латерального (зліва) та септального (справа) сегментів мітрального кільця у пацієнта з констриктивним перикардитом. Зазначте вищу ранньо-діастолічну швидкість септального сегменту (14 см/с) порівняно з латеральним сегментом (8 см/с) 1 = Е’, 2 = А’, 3 = систолічна швидкість (S).
B. Мітральний стеноз
Типово, у пацієнтів з мітральним стенозом діастолічний тиск в ЛШ є нормальним або зниженим за винятком нечастих випадків співіснуючої міокардіальної патології. Такі самі гемодинамічні знахідки присутні й у хворих з обструкцією приносного тракту ЛШ іншої етіології, таких як пухлини ЛП, трьохпередсердне серце та вроджений мітральний стеноз. На трансмітральний градієнт впливає ступінь важкості стенозу, серцевий викид та тривалість діастолічного наповнення. При розвитку фібриляції передсердь тиск в ЛП значно зростає для підтримання адекватного наповнення ЛШ. Хоча основним фокусом при клінічному обстеженні та веденні пацієнта з мітральним стенозом є ступінь його важкості, вираженість клінічних симптомів та вторинної легеневої гіпертензії, миттєве напівкількісне визначення миттєвого тиску наповнення ЛШ (тиску в ЛП) також може бути забезпечене підчас ранньої та пізньої систоли за допомогою допплерівських показників. Чим коротшим є IVRT (аускультативно відповідає тону відкриття мітрального клапану) та вищим є швидкість піку Е (за модифікованим рівнянням Бернуллі P = 4V2), тім вищим є ранньо-діастолічний тиск в ЛП. Тиск в ЛП є значно підвищеним наприкінці діастоли, якщо в цей момент мітральна швидкість залишається підвищеною >1,5 м/с. Крім того, співвідношення IVRT/(TE – TЕ’) корелює з середнім ТЗЛК та тиском в ЛП (значення співвідношення <4,2 є досить акуратним для виявлення пацієнтів з тиском наповнення >15 мм Hg). Втім, співвідношення E/Е’ при мітральному стенозі не є корисним [69].
Ключові моменти. Мітральний стеноз робить оцінку діастолічної функції ЛШ більш складною, але використання IVRT, TE-e’, та пікової швидкості трансмітрального кровопотоку в ранню та пізню діастолу можуть бути цінними у напівкількісному визначення середнього тиску в ЛП.
C. Мітральна регургітація
Первинна МР призводить до збільшення ЛП та ЛШ та зростання податливості обох камер, що сповільнює зростання тиску в ЛП. Якщо ЛП не може повністю компенсувати ситуацію, поступово зростає середній тиск у ЛП та у правих камерах серця, що пов’язане не з дисфункцією ЛШ, а з додатковим регургітуючим об’ємом, що закидається в ЛП та легеневі вени. При наявності діастолічної дисфункції ЛШ з часом додається міокардіальний компонент збільшення тиску наповнення. Таким чином, послідовність порівняно з тою, що спостерігається при первинній патології міокарда, такій, як дилатаційна кардіоміопатія, є зворотною, що веде до більш раннього зростання тиску наповнення та пізніше до прогресування функціональної МР. Таким чином, у пацієнтів із вторинною МР, ехокардіографічні знахідки показники підвищення тиску наповнення відбивають комбінацію як міокардіальної, так і клапанної патології.
Помірна та важка МР звичайно веде до зростання піку Е та зменшенню систолічного потоку в легеневих венах із зниженням співвідношення S/D. При важкій МР може також спостерігатися пізньо-систолічний зворотний поток в легеневій вені. Таким чином, МР сама по собі може приводити до змін графіки трансмітрального кровопотоку та потоку в легеневих венах, нагадуючи графіку при важкій дисфункції ЛШ з можливим винятком у різниці АR-A [70]. Крім того, запис спектру МР в ПХД може забезпечити високоспецифічні, хоча й не чутливі ознаки збільшеного тиску в ЛП (див. обговорення вище).
Здатність параметрів тканинної допплерографії (E/Е’) визначати тиск наповнення ЛШ у умовах помірної чи важкої МР залежить від систолічної функції [69,156,157]. У пацієнтів зі зниженою ФВ ЛШ підвищення співвідношення E/Е’ добре корелює з тиском наповнення та є предиктором ризику госпіталізації та смертності. У пацієнтів з нормальною ФВ ЛШ ці показники не корелюють з тиском наповнення. Навпаки, IVRT та співвідношення IVRT/TE-e’ досить добре корелюють з середнім ТЗЛК незалежно від ФВ ЛШ [69]. В особливості значення співвідношення IVRT/TE-e’<3 є однозначним предиктором ТЗЛК>15 мм Hg в даній підгрупі пацієнтів [69]. У пацієнтів з фібриляцією передсердь та МР для підрахунку співвідношення IVRT/TE-e’ можливо використовувати, співпадаючі інтервали RR, що, однак потребує отримання та аналізу великої кількості циклів (≥20).
Ключові моменти. Часові інтервали Ar – A, IVRT, та IVRT/TE-e’ можуть використовуватися для визначення тиску наповнення ЛШ у хворих з МР та нормальною ФВ ЛШ, у той час як співвідношення E/Е’ може бути використаним тільки при наявності зниженої ФВ ЛШ.
XIV. Оцінка тиску наповнення лівого шлуночка в особливих популяціях (Таб. 4)
A. Фібриляція передсердь
Оцінка тиску наповнення ЛШ з використанням допплерографії при фібриляції передсердь є обмеженою варіабельністю довжин кардіальних циклів, відсутністю чіткої передсердної активності та частим розвитком дилатації порожнини ЛП. Взагалі, коли ФВ ЛШ є зниженою, для визначення підвищення тиску наповнення ЛШ та прогнозування несприятливого клінічного прогнозу досить точним є зниження часу сповільнення ранньо-діастолічного кровотоку DT ≤150 мс [68,158]. Інші допплерівські виміри, що можна використовувати, включають пікове прискорення швидкості ранньо-діастолічного потоку Е (≥1,900 см/с2), IVRT (≤65 мс), DT діастолічної швидкості потоку в легеневих венах [159] (≤220 мс), співвідношення E/Vp (≥1,4), та співвідношення E/Е’ (≥11). В одному з досліджень [104] швидкість септального сегменту мітрального кільця Е’ <8 см/с показало досить високу точність у виявлені пацієнтів з τ ≥50 мс. Також значення співвідношення E/Е’ на септальному сегменті мітрального кільця ≥11 також свідчило про підвищення КДТ ЛШ ≥15 мм Hg. При цьому слід відмічати варіабельність швидкостей трансмітрального потоку, спів ставляючи її з довжиною інтервалів RR, хоча у пацієнтів з підвищеним тиском наповнення ЛШ варіабельність від удару до удару буває звичайно меншою [68]. Таким чином, допплерографія є корисною в оцінці тиску наповнення ЛШ у пацієнтів з фібриляцією передсердь. Вимірювання 10 кардіальних циклів є найбільш точним, хоча визначення швидкостей та часових інтервалів з розрахунком середнього арифметичного з даних 3 непослідовних кардіальних циклів в межах 10-20% середньої ЧСС та виміри одного кардіального циклу при використанні відповідного інтервалу RR в межах 70-80 уд./хв. теж досі полізні [68].
Table 4. Оцінка тиску наповнення ЛШ в спеціальних популяціях*.
|
Патологія
|
ЕхоКГ виміри та порогові значення
|
|
Фібриляція передсердь [68,104,159]
|
Пікове прискорення ранньо-діастолічного потоку Е (≥1,900 см/с2), IVRT (≤65 мс), DT діастолічного потоку в легеневих венах (≤220 мс), E/Vp (≥1,4), та септальне E/Е’ (≥11)
|
|
Синусова тахікардія [102,105]
|
Графіка трансмітрального потоку з домінуванням раннього наповнення ЛШ у пацієнтів з ФВ ЛШ <50%, IVRT ≤70 мс є специфічним (79%), систолічна фракція наповнення ≤40% є специфічною (88%), латеральне E/Е’>10 (значення >12 має найвищу специфічність 96%)
|
|
Гіпертрофічна кардіоміопатія [50]
|
Латеральне E/Е’(≥10), Ar – A (≥30 мс), систолічний тиск в ЛА (>35 мм Hg), та індекс об’єму ЛП (≥34 мл/м2)
|
|
Рестриктивна кардіоміопатія [51,52,160]
|
DT (<140 мс), мітральне E/A (>2,5), IVRT (<50 мс має високу специфічність), та септальне E/Е’(>15)
|
|
Некардіальна легенева гіпертензія [163]
|
Латеральне E/Е’ може бути використане для відповіді, чи є саме кардіогенна етіологія причиною підвищення тиску в малому колі (кардіальна етіологія: E/Е’>10; некардіальна етіологія: E/Е’<8)
|
|
Мітральний стеноз [69]
|
IVRT (<60 мс має високу специфічність), IVRT/TE-e’ (<4.2), трансмітральний пік A (>1,5 м/с)
|
|
МР [69,70,157]
|
Ar – A (≤30 мс), IVRT (<60 мс має високу специфічність), та IVRT/TE-e’ (<3) можуть використовуватись для визначення тиску наповнення ЛШ у хворих з МР та нормальною ФВ ЛШ, у той час як середнє значення E/Е’(>15) може застосовуватись тільки при зниженій ФВ ЛШ
|
*У всіх вищенаведених ситуаціях рекомендований комплексний підхід, а заключення не повинне робитися, базуючись тільки на одному вимірі. Коментарії щодо специфічності стосуються виявлення тиску наповнення >15 мм Hg.
B. Синусова тахікардія
Традиційні показники трансмітрального потоку та кровопотоку в легеневих венах при синусовій тахікардії >100 уд./хв. у пацієнтів з нормальною ФВ ЛШ є поганими індикаторами тиску наповнення ЛШ. Втім, співвідношення E/Е’ з використанням латерального сегменту мітрального кільця >10 свідчить про середній ТЗЛК >12 мм Hg з чутливістю 78% та специфічністю 95%. Важливо, що ця взаємозалежність залишається міцною незалежно від графіки трансмітрального кровопотоку та ФВ ЛШ, так само, як і від наявності тільки одного піку швидкості внаслідок злиття як трансмітральних швидкостей Е і А, так і піків руху мітрального кільця Е’ та А’ [102,105].
C. Рестриктивна кардіоміопатія
Незалежно від етіології (ідіопатичної чи інфільтративної), показники трансмітрального кровопотоку, потоків в легеневих венах та тканинні допплерівські індекси є добрими індикаторами значного збільшення тиску наповнення у пацієнтів з рестриктивною кардіоміопатією. Скорочення (<140 мс) ранньо-діастолічного DT [51,52,160] та збільшення чи трансмітрального E/A (>2,5) чи E/Е’ (>15) вказують на значно підвищений тиск наповнення ЛШ. Вкорочення IVRT <50 мс внаслідок раннього відкриття МК також вказує на високий тиск у ЛП [160].
D. Гіпертрофічна кардіоміопатія
На відміну від рестриктивних кардіоміопатій, трансмітральні швидкості та їх співвідношення E/A, та DT слабо або взагалі не корелюють з тиском наповнення ЛШ у пацієнтів з гіпертрофічною кардіоміопатією [49,50]. Значна варіабельність фенотипу, м’язової маси, кількості хаотично розташованих міофібріл та наявність чи відсутність обструкції призводять до дуже різноманітних комбінацій порушення релаксації та комплаєнсу та великим варіаціям графік трансмітрального кровопотоку. В одному
дослідженні співвідношення E/Е’ (≥10 на латеральному сегменті мітрального кільця) добре корелювало з тиском в ЛШ перед хвилею А [50], у той час як в іншому джерелі при неінвазивному визначенні середнього тиску в ЛП спостерігалися великі розбіжності даних [161]. Подібно до інших груп хворих, різниця тривалості хвиль Ar - A (≥30 мс) в цій популяції пацієнтів може бути використана для визначення КДТ ЛШ [50]. При визначенні тиску наповнення ЛШ у хворих з гіпертрофічною кардіоміопатією рекомендований комплексний підхід, з урахуванням всіх ехокардіографічних даних, включаючи тиски в малому колі кровообігу та об’єм ЛП (особливо при відсутності гемодинамічно значущої МР).
E. Легенева гіпертензія
У пацієнтів з легеневою гіпертензією ЕхоКГ відіграє дуже важливу роль у визначенні тисків в малому колі кровообігу, оцінці розмірів та функції ПШ та визначенні підлеглої етіології легеневої гіпертензії та диференційній діагностиці у сенсі кардіального гіпертензія походження чи ні. Якщо етіологія пов'язана з паренхіматозною чи судинною легеневою патологією, тиск наповнення ЛШ звичайно нормальний чи низький, а на мітральному клапані звичайно спостерігається графіка порушення релаксації [162] внаслідок не діастолічної дисфункції per se, а зниження наповнення ЛШ. Типово в цих пацієнтів спостерігають нормальні швидкості ранньо-діастолічного руху мітрального кільця Е’ (Рис. 13) та співвідношення E/Е’ на латеральному сегменті мітрального кільця <8 [163]. І навпаки, у пацієнтів із вторинною легеневою гіпертензією внаслідок діастолічної дисфункції ЛШ звичайно спостерігаються збільшені значення співвідношення E/Е’, тому що швидкість трансмітрального піку Е збільшуються внаслідок підвищеного тиску в ЛП, а швидкість латерального сегменту мітрального кільця Е’ знижується внаслідок патології міокарда. Використання ранньо-діастолічної швидкості руху Е’ септального мітрального кільця у пацієнтів з некардіальною етіологією легеневої гіпертензії є обмеженим, тому що септальна швидкість Е’ знижується за рахунок вкладу ПШ в рух міжшлуночкової перегородки [163]. При успішному зниженні легеневого судинного опору серцевий викид зростає, графіка діастолічного наповнення ЛШ змінюється в напрямку нормалізації, а співвідношення E/Е’ на латеральному сегменті мітрального кільця зростає [163]. Ці зміни можуть бути корисними при динамічному спостереженні відповіді на медикаментозне чи хірургічне лікування легеневої гіпертензії.
XV. Прогноз
Діастолічна дисфункції розвивається раніше інших змін при більшості серцевих захворювань, призводячи до зростання тиску наповнення ЛШ. Тому ехокардіографічні виміри показників діастолічної функції забезпечують важливу прогностичну інформацію (Таб. 5). Клінічні дослідження показали асоціацію скорочення часу скорочення ранньо-діастолічного потоку DT з розвитком серцевої недостатності, смертності та частотою госпіталізацій у пацієнтів з гострим інфарктом міокарда [30–46]. Показники діастолічної функції додають багато інформації до звичайної оцінки сегментарної скоротливості, включаючи розрахунок індексу локальної скоротливості. Нещодавно ці спостереження були підтверджені в мета-аналізі 12 клінічних досліджень у 1286 хворих після гострого інфаркту міокарда [47]. Подібні ж знахідки були докладені також у хворих з ішемічною чи ідіопатичною дилатаційною кардіоміопатією, включаючи пацієнтів з фібриляцією передсердь [34]. Швидкості кровопотоку в легеневих венах [71–73] та Vp [88,164–166] досліджені не так ретельно, але все ж є доведеними предикторами клінічних подій. Зважаючи на варіабельність в вимірах DT, Vp, та тривалості кровопотоків в легеневих венах, недавні дослідження вивчали прогностичну значимість співвідношення E/Е’ (Таб. 5). Декілька досліджень [88,167–178] показали, що E/Е’ є точним предиктором небажаних клінічних подій після гострого інфаркту міокарда та при гіпертензивному серця, важкій вторинній МР, термінальних стадіях захворюваннях нирок, фібриляції передсердь та кардіоміопатіях.
Співвідношення E/Е’ є серед найбільш відтворюваних ехокардіографічних параметрів для визначення ТЗЛК, та йому віддається перевага у багатьох патологічних ситуаціях при серцевій патології.
XVI. Рекомендації для клінічних закладів
Коли технічна якість дослідження є адекватною, а знахідки виявляються непогодженими одна з другою і т.д., заключення має включати оцінку як тиску наповнення ЛШ, так і типу діастолічної дисфункції.
A. Оцінка тиску наповнення ЛШ у хворих із зниженою ФВ
В даній популяції графіка трансмітрального потоку сама по собі може використовуватися для визначення тиску наповнення з досить доброю точністю в популяції. Крім того, зміни профілю графіки трансмітрального кровопотоку можуть використовуватися для оцінки змін тиску наповнення у відповідь на лікування в динаміці. У пацієнтів з графікою порушення релаксації та швидкістю піку Е<50 см/с тиск наповнення ЛШ звичайно нормальний. При рестриктивному наповненні середній тиск в ЛП підвищений (Рис. 14). Використання додаткових допплерівських показників рекомендується у пацієнтів з E/A від 1 до 2. Зміни значення співвідношення E/A при проведенні проби Вальсальви на більше, ніж 50%, зниження співвідношення систолічного піку кровопотоку в легеневих венах до діастолічного S/D<1, Ar – A ≥30 мс, E/Vp≥2,5, E/Е’ (з використанням середнього значення швидкостей Е’ на латеральному та септальному сегментах мітрального кільця) ≥15, IVRT/TE-e’<2, та систолічного тиску в ЛА ≥35 мм Hg (за відсутності легеневої патології) можуть використовуватися для визначення підвищеного тиску наповнення ЛШ. І навпаки, зміни співвідношення E/A при проведенні проби Вальсальви менше, ніж на 50%, співвідношення піків потоків в легеневих венах S/D>1, Ar – A <0 мс, E/Vp <1,4, E/Е’ (з використанням середнього значення швидкостей Е’ на латеральному та септальному сегментах мітрального кільця) <8, IVRT/TE-e’ >2, та систолічний тиск в ЛА <30 ммHg вказують на нормальний тиск наповнення ЛШ. У пацієнтів з псевдонормальним наповненням висновок має робитися на основі не менше двох, а краще більшої кількості допплерівських показників, з відданням переваги записам сигналів кращої якості. В цій популяції хворих частою знахідкою є дилатація ЛП, навіть при нормальному тиску наповнення ЛШ, тому в таких випадках розмір ЛП не повинен використовуватися, як ознака останньої інстанції.
B. Оцінка тиску наповнення ЛШ у хворих з нормальною ФВ
Оцінка тиску наповнення ЛШ у пацієнтів з нормальною ФВ ЛШ є більш складною порівняно з хворими з систолічною дисфункцією. В цій групі пацієнтів слід розраховувати співвідношення E/Е’. Середнє значення ≤8 визначає хворих з нормальним тиском наповнення ЛШ, у той час як середнє E/Е’≥13 говорить про його підвищення [86]. При значенні E/Е’=8-13 слід вдаватися до інших допоміжних показників (Рис. 15).
Різниця Ar - A ≥30 мс, зміни співвідношення E/A при пробі Вальсальви більше, ніж на 50%, IVRT/TE-e’<2, систолічний тиск в ЛА ≥35 мм Hg (при відсутності легеневої патології), та максимальний індекс об’єму ЛП ≥34 мл/м2 всі вказують на підвищення тиску наповнення ЛШ. Відтворюваність аномальних результатів ≥2 разів збільшує вірогідність заключення. Хоча E/Vp >1,9 спостерігається при середньому ТЗЛК >15 мм Hg, у певної частини пацієнтів з діастолічною дисфункцією та нормальною ФВ ЛШ Vp може бути нормальним, або навіть підвищеним, призводячи до значення E/Vp<1,9 навіть при підвищеному тиску наповнення ЛШ.
Таб. 5. Дослідження прогностичного значення допплерівських показників діастолічної функції ЛШ.
|
Дослідження
|
n
|
Популяція
|
Спостереження
|
Події
|
Показники
|
Результати
|
|
Xie, et al. [30]
|
100
|
СН, ФВ <40%
|
16±8 міс.
|
Смертність
|
E/A, DT
|
Смертність через 1 р. 19% vs 5%; через 2 р. 51% vs 5%
|
|
Rihal, et al. [31]
|
102
|
ДКМП
|
36 міс.
|
Смертність
|
E/A, DT
|
EF <25% + DT <130 ms мали рівень виживання 35% через 2 р., EF
<25% + DT > 130 ms мали рівень виживання 72% через 2 р., EF >25% мали рівень виживання >95% незалежно від DT
|
|
Giannuzzi, et al. [33]
|
508
|
ФВ≤35%
|
29±11 міс.
|
Смертність + госпіталізації
|
DT
|
Виживання без подій 77% при DT > 125 ms, виживання без подій 18% при DT < 125 ms; DT був додатковим предиктором до віку, функціонального класу, наявності третього серцевого тону, ФВ та площі ЛП
|
|
Pozzoli, et al. [40]
|
173
|
СН, ФВ<35%
|
17±9 міс.
|
Кардіальна смерть та ургентна трансплантація серця
|
Зміни мітрального кровопотоку при навантаженні
|
Частота подій 51% при незворотному рестриктивному наповненні, 19% - при зворотному рестриктивному наповненні, 33% - при нестабільному нерестрективному, та 6% - при стабільному нерестрективному наповненні
|
|
Pinamonti, et al. [41]
|
110
|
ДКМП
|
41±20 міс.
|
Смертність + кардіо-трансплантація
|
Зміни трансмітрального потоку через 3 місяців лікування
|
Через 1, 2, та 4 р., виживання пацієнтів з персистуючим рестриктивним наповненням (65%, 46%, та 13%, відповідно) був значно нижчим порівняно із пацієнтами зі зворотно рестриктивним наповненням (100% через 1 та 2 р., та 96% через 4 р.), та пацієнтами з нерестрективним наповненням (100% через 1 та 2 р., та 97% через 4 р.)
|
|
Traversi, et al. [32]
|
98
|
ІКМП + ДКМП
|
12±7 міс.
|
Кардіальна смертність + кардіо-трансплантація
|
Зміни трансмітрального потоку через 6 місяців лікування
|
Частота подій 35% при персистуючому рестриктивному наповненні, 5% - при зворотному рестриктивному наповненні, та 4% - при персистуючому нерестриктивному наповненні
|
|
Temporelli, et al. [42]
|
144
|
СН + DT ≤125 ms
|
26±7 міс.
|
Кардіальна смертність
|
Зміни DT через 6 місяців лікування
|
Частота подій: 37% при персистуючому рестриктивному наповненні vs 11% при зворотній рестрикції; подовження вихідного вкороченого DT був єдиним та найкращим предиктором виживання
|
|
Hurrell, et al. [34]
|
367
|
Рестриктивне наповнення:
DT ≤130ms
|
2,2 р.
|
Смертність
|
DT
|
Виживання 42% при синусовому ритмі та DT <130 мс та 39% при фібриляції передсердь та DT <130 мс
|
|
Hansen, et al. [35]
|
311
|
ІКМП + ДКМП
|
512±314 днів
|
Смертність + кардіо-трансплантація
|
Графіка трансмітрального потоку
|
2-річна виживаність 52% при рестриктивному наповненні vs 80% при нерестриктивному; тип трансмітрального наповнення був додатковим предиктором до пікового споживання кисню
|
|
Faris, et al. 36
|
337
|
ДКМП
|
43±25 міс.
|
Смертність
|
Графіка трансмітрального потоку
|
1,3, та 5-річна виживаність пацієнтів з рестриктивним наповненням (88%, 77%, та 61%) була значно нижчою порівняно з пацієнтами з нерестриктивним наповненням (96%, 92%, та 80%)
|
|
Whalley, et al. [37]
|
115
|
ІКМП + ДКМП
|
0,87±0,28 р.
|
Смертність + госпіталізації
|
Графіка трансмітрального потоку
|
Частота подій 62.9% при рестриктивному наповненні vs 26.1% у пацієнтів з порушенням релаксації
|
|
Bella, et al. [39]
|
3008
|
Американські індіанці
|
3р.
|
Загальна та кардіальна смертність
|
E/A
|
Загальна смертність була вищою при E/A<0,6 або
E/A>1.5 (12% та 13%), як і кардіальна смертність (4.5% та 6.5%) vs 6% та 1.6% при нормальному співвідношенні E/A
|
|
Rossi, et al. [38]
|
106
|
ДКМП
|
524±138 днів
|
Смертність
|
Графіка трансмітрального потоку
|
Рівень виживання 38% при рестриктивному наповненні vs 90% при нерестриктивному через 600 днів спостереження
|
|
Dini, et al. [72]
|
145
|
ІКМП + ДКМП
|
15±8 міс.
|
Смертність + госпіталізації
|
DT + Ar - A
|
Кардіальна виживаність без подій через 24-міс. була найвищою (86.3%) при DT > 130 мс + Ar - A <30 ms; помірною (37.9%) при DT > 130 мс + Ar - A ≥30 ms; та найгіршою (22.9%) при DT < 130 мс + Ar - A ≥30 ms
|
|
Dini, et al. [73]
|
115
|
ІКМП + ДКМП
|
12 міс.
|
Кардіальна смертність
|
S/D піків потоку в легеневих венах
|
Смертність складала 23% при S/D<1 та значно вищою порівняно з пацієнтами з S/D>1 (7%)
|
|
Yamamoto, et al.1 68
|
96
|
ІКМП + ДКМП, ФВ
≤40%
|
29±10 міс.
|
Кардіальна смертність та госпіталізації з приводу СН
|
Трансмітральний потік, E/Е’ (задній сегмент)
|
Виживаність через 40 міс. була ~72% при А’>5 cm/s та ~22% при А’≤5 cm/s; при множинній регресії A’≤5 cm/s, E/Е’>15, та DT<140 мс були незалежними предикторами подій
|
|
Hillis, et al. [170]
|
250
|
Гострий ІМ
|
13 міс.
|
Смертність
|
DT, E/Е’ (септальний сегмент)
|
Смертність 26% with E/Е’>15 та 5.6% при E/Е’≤15; E/Е’ >15 був додатковим предиктором до клінічних симптомів, ФВ ЛШ та DT <140 мс
|
|
Wang, et al. [171]
|
182
|
Кардіальні пацієнти з ФВ<50%
|
48 міс.
|
Кардіальна смертність
|
Трансмітральний потік, кодований в кольорі Е’ (середнє значення з септального, латерального, переднього та нижнього сегментів), Vp
|
Рівень кардіальної смертності був 32% при E’<3 см/с та 12% при E’>3 см/с; E’ був додатковим предиктором до DT <140 мс та E/Е’
>15
|
|
Wang, et al. [173]
|
252
|
Артеріальна гіпертензія, середня ФВ = 51%
|
~19 міс.
|
Кардіальна смертність
|
Трансмітральний потік, кодований в кольорі Е’ (середнє значення з септального, латерального, переднього та нижнього сегментів), Vp
|
Кардіальна смерть у 19 пацієнтів (7,5%); при множинній регресії Е’<3,5 см/с був найпотужнішим незалежним предиктором подій
|
|
Dokainish, et al. [172]
|
110
|
ІКМП + ДКМП
|
527±47 днів
|
Кардіальна смертність та госпіталізації з приводу СН
|
DT, ІХД E/Е’ (середнє значення з латерального та септального сегментів)
|
Рівень НУП та E/Е’ перед випискою були додатковими предикторами подій (54/110, або частота подій 49%)
|
|
Troughton, et al. [88]
|
225
|
ІКМП + ДКМП (ФВ<35%)
|
~10 міс.
|
Смертність + кардіо-трансплантація + госпіталізації з приводу СН
|
DT, S/D, Vp, E/Е’ (септальний сегмент)
|
Частота подій 45% при E/Е’>16 та 13% при E/Е’<16; частота подій 37% при E/Vp >2,7 та 22% при E/Vp<2,7; частота подій 44% при DT<170 мс та 14% при DT>170 мс; частота подій 45% при S/D<1 та 10% при S/D>1; E/Е’ та S/D – незалежні пре диктори прогнозу
|
|
Okura, et al. [175]
|
230
|
Фібриляція передсердь неклапанного генезу
|
245±200 днів
|
Загальна смертність, кардіальна смертність, гостра СН
|
Трансмітральний DT, S/D, DT потоку D в легеневих венах, PW E/Е’ (септальний сегмент)
|
Загальна смертність була вищою (16,7%) при E/Е’>15, та 4,3% при E/Е’<15; кардіальна смертність складала 11,1% при E/Е’>15 vs 1,4% при E/Е’< 15; застійна СН розвивалася частіше при E/Е’>15(17,8%) vs 5,7% при E/Е’<15; E/Е’ та вік були незалежними предикторами смертності
|
|
Sharma, et al. [174]
|
125
|
Термінальна хвороба нирок, ФВ=66±14%
|
1,61±0,56 р.
|
Загальна смертність
|
Трансмітральний потік, легеневі вени, Vp, ІХД E/Е’ (середнє значення з латерального та септального сегментів)
|
Загальна смертність була 9,6% та значно вищою при E/Е’>15; не виявлено різниці в смертності у пацієнтів з чи без рестриктивного наповнення
|
|
Bruch, et al. [176]
|
370
|
СН + МР,
ЕРО>0.2cm2,
ІКМП + ДКМП, ФВ<50%
|
790±450 днів
|
Смертність та госпіталізації з приводу СН
|
DT, ІХД E/Е’ (середнє значення з латерального та септального сегментів)
|
Рівень смертності був вищий у пацієнтів при вираженій МР vs пацієнти без такої (33% vs 14%); у пацієнтів з МР рівень виживання без подій був 31% при E/Е’>13,5 та 64%
при E/Е’e ≤13,5
|
*НУП – натрій-уретичний пептид; СН – серцева недостатність; ДКМП – дилатаційна кардіоміопатія; ЕРО – ефективний регургітуючий отвір; ІСМП – ішемічна кардіоміопатія; ІМ – інфаркт міокарду.
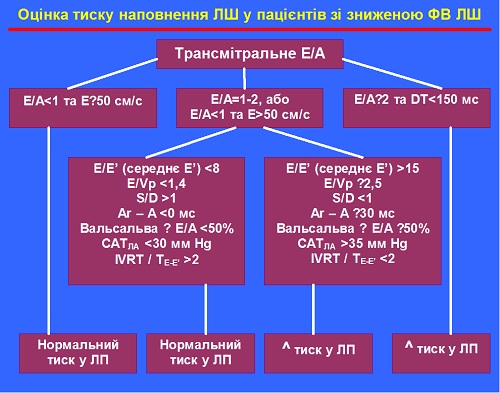
Рис. 14. Діагностичний алгоритм для визначення тиску наповнення ЛШ у пацієнтів із зниженою ФВ ЛШ.
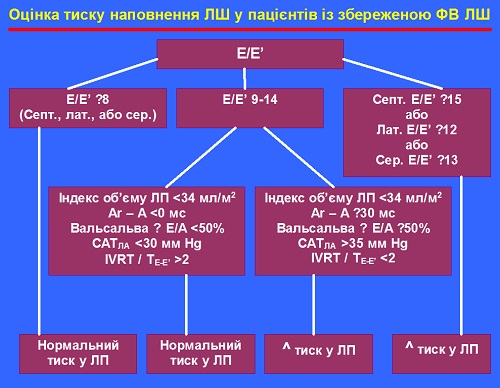
Рис. 15. Діагностичний алгоритм для визначення тиску наповнення ЛШ у пацієнтів з нормальною ФВ ЛШ.
C. Класифікація діастолічної дисфункції
Діастолічна дисфункція класифікується на легку, або І степеня (порушення релаксації), помірну, або ІІ ступеня (псевдо нормалізація) та важку, або ІІІ ступеня (рестриктивне наповнення) (Рис. 16). Ця схема є важливим предиктором загальної смертності згідно великому епідеміологічному дослідженню [169]. Важливо, що навіть у безсимптомних пацієнтів І ступінь діастолічної дисфункції (див. далі) асоціювався з 5-кратним підвищенням 3-5 річної смертності порівняно з суб’єктами з нормальною діастолічної функцією.
Підчас оцінки треба приймати до уваги вік пацієнта та частоту серцевих скорочень (трансмітральна швидкість Е, співвідношення Е/А та швидкість мітрального кільця Е’ знижуються при збільшенні ЧСС). Також специфічним є те, що у літніх індивідів без анамнезу серцево-судинних захворювань висновок про І ступінь діастолічної дисфункції слід робити з обережністю, оскільки у більшості суб’єктів старше 60 років без анамнезу серцево-судинної патології Е/А<1 та DT>200 мс. Тому такі значення у цих пацієнтів при відсутності інших ознак кардіальної патології (наприклад, гіпертрофії ЛШ, дилатації ЛП, тощо) можуть вважатися віковими змінами.
У пацієнтів з легкою діастолічною дисфункцією, співвідношення E/A<0,8, DT>200 мс, IVRT≥100 мс, домінує систолічний потік в легеневих венах (S > D), Е’ мітрального кільця>8 см/с, а співвідношення E/Е’<8 (середнє значення з септального та латерального сегментів мітрального кільця). У цих пацієнтів має місце знижений діастолічний резерв, що може бути виявлено підчас проб з навантаженням. Втім, зниження співвідношення Е/А при нормальних швидкостях мітрального кільця за даними тканинного допплера може спостерігатися у зневоднених здорових суб’єктів, тобто значення E/A<0,8 не повинно універсально приводити до висновку про діастолічну дисфункцію. У більшості ситуацій, коли Е/A<0,8, середній тиск в ЛП не підвищений, за винятком деяких пацієнтів з важким порушенням релаксації міокарду, наприклад при стійкій важкій артеріальній гіпертензії чи гіпертрофічній кардіоміопатії.
У пацієнтів з помірною діастолічною дисфункцією (ступінь II) співвідношення E/A дорівнює 0,8-1,5 (псевдонормалізація), та при проведенні проби Вальсальви знижується більше, ніж на 50%. Середнє значення Е/Е’ складає 9-12 при швидкості руху мітрального кільця Е’<8 см/с. Інші дані, що свідчать на користь помірної діастолічної дисфункції включають швидкість зворотного потоку в легеневій вені підчас систоли передсердь Ar>30 см/с та співвідношення S/D <1. У деяких пацієнтів з помірною діастолічною дисфункцією підвищеним є тільки КДТ ЛШ (тобто, середній тиск в ЛП може бути нормальним), що можна підтвердити при значенні різниці Ar - A ≥30 мс. Ступінь II дисфункції відповідає порушенню релаксації міокарда з легким чи помірним збільшенням тиску наповнення ЛШ.
При важкій діастолічній дисфункції (ступінь III) рестриктивне наповнення реєструється при E/A≥2, DT<160 мс, IVRT≤60 мс, фракції систолічного наповнення ≤40%, скороченні тривалості трансмітральної хвилі A до значення, меншого, ніж тривалість зворотного потоку в легеневій вені підчас систоли передсердя Ar, та середньому значенні E/Е’ >13 (або септальному E/Е’ ≥15 та латеральному E/Е’>12). У деяких пацієнтів графіка наповнення може зворотно змінюватися до порушення релаксації при ефективній терапії (ступінь IIIa), у той час як в інших вона залишається рестриктивною не зважаючи на лікування (ступінь IIIb). Остання є зловісною знахідкою, що є предиктором високого ризику кардіальної захворюваності та смертності. Втім, дисфункція IIIb ступеня не може бути визначена за одне дослідження, та потребує декількох досліджень до та після оптимізації лікування. При ІІ та ІІІ ступенях діастолічної дисфункції об’єм ЛП збільшений, але може бути в нормальних межах у пацієнтів з І ступенем та у пацієнтів з доклінічними змінами.
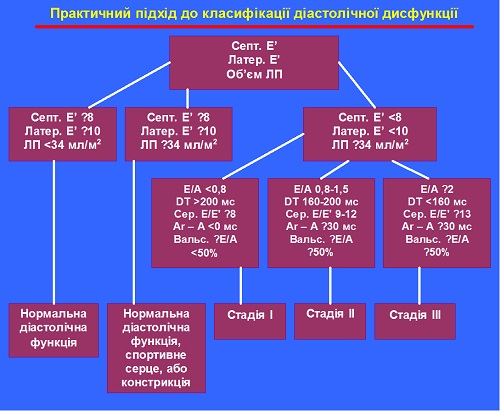
Рис. 16. Схема для класифікації діастолічної дисфункції. Сер. - середній; ЛП – ліве передсердя; Вал. – проба Вальсальви.
XVII. Рекомендації до застосування в наукових дослідженнях та клінічних випробуваннях
В ехокардіографічній лабораторії релаксація міокарда, жорсткість ЛШ та тиск наповнення можуть бути оцінені тільки непрямо, тому що оцінка гемодинамічних даних за допомогою ЕхоКГ часто включає спрощені припущення, що прийнятні для певної популяції пацієнтів, але можуть не підходити для всіх без винятку пацієнтів.
Допплерівські виміри показників діастолічної функції можуть демонструвати індивідуальну варіабельність та можуть коливатись від дня до дня у одного і того самого пацієнта залежно від змін переднавантаження, пост навантаження та симпатичного тонусу. Реферативні значення для диференціації здорових та патологічних суб’єктів повинні враховувати вікову групу, з якої обирається суб’єкт для дослідження. Також при з'ясуванні взаємозв’язків та кореляцій із створенням статистичних моделей бажано досліджувати залежність допплерівських показників від статі, маси тіла та артеріального тиску.
На базі чітко сформульованого питання дослідник має визначити необхідність визначення змін релаксації, жорсткості та/або тиску наповнення. Основними показниками порушеної релаксації є IVRT та ізоволюмічний або ранній діастолічний рух мітрального кільця або швидкість деформації міокарду ЛШ. Показниками зниженої податливості (комплаєнсу) є DT of трансмітральної хвилі Е, тривалість хвилі А, співвідношення КДТ ЛШ до КДО ЛШ, та сурогатні показники підвищення КДТ ЛШ, а саме вище вказана тривалість хвилі А, зниження швидкості пізньо-діастолічного руху А’, та подовження тривалості зворотного потоку в легеневій вені в систолу передсердь Ar. Маркерам раннього діастолічного тиску в ЛШ та тиску в ЛП є співвідношення E/Е’, DT трансмітральної хвилі E у пацієнтів зі зниженою ФВ ЛШ, та, до деякої міри, збільшення ЛП, що відбиває скоріше хронічне, ніж гостре підвищення тиску. Швидкість розкручування ЛШ може бути корисною для вивчення ефектів всмоктування на наповнення ЛШ та взаємозв’язку між систолічною та діастолічною функцією ЛШ. Для кожного експериментального питання повинен бути підібраний найбільш адекватний ехокардіографічний підхід для відповіді на це запитання, як підкреслено в цих рекомендаціях. Крім того, висновки щодо змін стану релаксації ЛШ мають робитися з обережністю, тому що зміни показників можуть бути наслідком змін навантаження per se, а не швидким покращенням міокардіальної функції.
При виборі ехокардіографічної методики для дослідження та вирішення поставлених задач, пов’язаних з діастолічною функцією, можливо використовувати як загальноприйняті прості підходи, що є легко доступними та високо відтворюваними, так і більш індивідуальні та складні. Хоча вже давно відомі підходи влаштовують клінічно орієнтовані дослідження, більш нові методики можуть дати більше відповідей на питання внутрішньосерцевої механіки. Прикладом традиційних підходів є ехокардіографічне субдослідження в рамках «Ірбесартан при серцевій недостатності із збереженою систолічною функцією» [179]. В цьому субдослідженні вивчалися розмір ЛП, розміри та функція ЛШ, індекс маси міокарду ЛШ та співвідношення E/Е’. З іншого боку, дослідження деформації міокарду за технологією «спекл-трекінг» показало добру відтворюваність, та може бути застосоване для вивчення сегментарної деформації і питань міокардіальної механіки.
Література
1. Paulus W.J., Tschope C., Sanderson J.E., et al. How to diagnose diastolic heart failure: a consensus statement on the diagnosis of heart failure with normal left ventricular ejection fraction by the Heart Failure and Echocardiography Associations of the European Society of Cardiology // Eur. Heart J. - 2007. - Vol. 28. - p. 2539–50.
2. Brutsaert D.L., Sys S.U., Gillebert T.C. Diastolic failure: pathophysiology and therapeutic implications // J. Am. Coll. Cardiol. - 1993. - Vol. 22. - p. 318–25.
3. Yip G.W., Zhang Y., Tan P.Y., Wang M., Ho P.Y., Brodin L.A. et al. Left ventricular long-axis changes in early diastole and systole: impact of systolic function on diastole // Clin. Sci. (Lond). - 2002. - Vol. 102. - p. 515–22.
4. Leite-Moreira A.F., Correia-Pinto J., Gillebert T.C. Afterload induced changes in ьyocardial relaxation: a mechanism for diastolic dysfunction // Cardiovasc. Res. - 1999. - Vol. 43. - p. 344–53.
5. Leite-Moreira A.F. Current perspectives in diastolic dysfunction and diastolic heart failure // Heart. - 2006. - Vol. 92:712–8.
6. Gillebert T.C, Lew W.Y. Nonuniformity and volume loading independently influence isovolumic relaxation rates // Am. J. Physiol. - 1989. - Vol. 257. - p. H1927–35.
7. Westermann D., Kasner M., Steendijk P., et al. Role of left ventricular stiffness in heart failure with normal ejection fraction // Circulation. - 2008. - Vol. 117. - p. 2051–60.
8. Torrent-Guasp F., Ballester M., Buckberg G.D., et al. Spatial orientation of the ventricular muscle band: physiologic contribution and surgical implications // J. Thorac. Cardiovasc. Surg. - 2001. - Vol. 122. - p. 389–92.
9. Hung J., Lang R., Flachskampf F., et al. 3D echocardiography: a review of the current status and future directions // J. Am. Soc. Echocardiogr. - 2007. - Vol. 20. - p. 213–33.
10. Lang R.M., Bierig M., Devereux R.B., et al. American Society of Echocardiography’s Nomenclature and Standards Coммittee; Task Force on Chamber Quantification; American College of Cardiology Echocardiography Coммittee; American Heart Association; European Association of Echocardiography, European Society of Cardiology recoммendations for chamber quantification // Eur. J. Echocardiogr. - 2006. - Vol. 7. - p. 79–108.
11. Tsang T.S., Barnes M.E., Gersh B.J., et al. Left atrial volume as a morphophysiologic expression of left ventricular diastolic dysfunction and relation to cardiovascular risk burden // Am. J. Cardiol. - 2002. - Vol. 90. - p. 1284–9.
12. Abhayaratna W.P., Seward J.B., Appleton C.P., et al. Left atrial size: physiologic determinants and clinical applications // J. Am. Coll. Cardiol. - 2006. - Vol. 47. - p. 2357–63.
13. Prioli A., Marino P., Lanzoni L., Zardini P. Increasing de.g.rees of left ventricular filling impairment modulate left atrial function in humans // Am. J. Cardiol. - 1998. - Vol. 82. - p. 756–61.
14. Manning W.J., Silverman D.I., Katz S.E., Douglas P.S. Atrial ejection force: a noninvasive assessment of atrial systolic function // J. Am. Coll. Cardiol. - 1993. - Vol. 22. - p. 221–5.
15. Stefanadis C., Dernellis J., Lambrou S., Toutouzas P. Left atrial energy in normal subjects, in patients with symptomatic mitral stenosis, and in patients with advanced heart failure // Am. J. Cardiol. - 1998. - Vol. 82. - p. 1220–3.
16. Inaba Y., Yuda S., Kobayashi N., et al. Strain rate imaging for noninvasive functional quantification of the left atrium: comparative studies in controls and patients with atrial fibrillation // J. Am. Soc. Echocardiogr. - 2005. - Vol. 18. - p. 729–36.
17. Di Salvo G., Caso P., Lo Piccolo R., Fusco et al. Atrial myocardial deformation properties predict maintenance of sinus rhythm after external cardioversion of recent-onset lone atrial fibrillation // Circulation. - 2005. - Vol. 112. - p. 387–95.
18. Bouchard J.L., Aurigeммa G.P., Hill J.C., et al. Usefulness of the pulmonary arterial systolic pressure to predict pulmonary arterial wedge pressure in patients with normal left ventricular systolic function // Am. J. Cardiol. - 2008. - Vol. 101. - p. 1673–6.
19. Quinones M.A., Otto C.M., Stoddard M., et al. Recoммendations for quantification of Doppler echocardiography: a report from the Doppler Quantification Task Force of the Nomenclature and Standards Coммittee of the American Society of Echocardiography // J. Am. Soc. Echocardiogr. - 2002. - Vol. 15. - p. 167–84.
20. Lee R.T., Lord C.P., Plappert T., Sutton M.S. Prospective Doppler echocardiographic evaluation of pulmonary artery diastolic pressure in the medical intensive care unit // Am. J. Cardiol. - 1989. - Vol. 64. - p. 1366–70.
21. Rapp A.H., Lange R.A., Cigarroa J.E., et al. Relation of pulmonary arterial diastolic and mean pulmonary arterial wedge pressures in patients with and without pulmonary hypertension // Am. J. Cardiol. - 2001. - Vol. 88. - p. 823–4.
22. Appleton C.P., Jensen J.L., Hatle L.K., Oh J.K. Doppler evaluation of left and right ventricular diastolic function: a technical guide for obtaining optimal flow velocity recordings // J. Am. Soc. Echocardiogr. - 1997. - Vol. 10. - p. 271–91.
23. Ha J.W., Oh J.K., Redfield M.M., et al. Triphasic mitral inflow velocity with middiastolic filling: clinical implications and associated echocardiographic findings // J. Am. Soc. Echocardiogr. - 2004. - Vol. 17. - p. 428–31.
24. Klein A.L., Burstow D.J., Tajik A.J., et al. Effects of age on left ventricular dimensions and filling dynamics in 117 normal persons // Mayo Clin. Proc. - 1994. - Vol. 69. - p. 212–24.
25. Appleton C.P., Hatle L.K., Popp R.L. Relation of transmitral flow velocity patterns to left ventricular diastolic function: new insights from a combined hemodynamic and Doppler echocardiographic study // J. Am. Coll. Cardiol. - 1988. - Vol. 12. - p. 426–40.
26. Vanoverschelde J.L., Raphael D.A., Robert A.R., Cosyns J.R. Left ventricular filling in dilated cardiomyopathy: relation to functional class and hemodynamics // J. Am. Coll. Cardiol. - 1990. - Vol. 15. - p. 1288–95.
27. Pinamonti B., Di Lenarda A., Sinagra G., Camerini F. Heart Muscle Disease Study Group. Restrictive left ventricular filling pattern in dilated cardiomyopathy assessed by Doppler echocardiography: clinical, echocardiographic and hemodynamic correlations and prognostic implications // J. Am. Coll. Cardiol. - 1993. - Vol. 22. - p. 808–15.
28. Giannuzzi P., Imparato A., Temporelli P.L., et al. Doppler-derived mitral deceleration time of early filling as a strong predictor of pulmonary wedge pressure in postinfarction patients with left ventricular dysfunction // J. Am. Coll. Cardiol. - 1994. - Vol. 23. - p. 1630–7.
29. Pozzoli M., Capomolla S., Pinna G., et al. Doppler echocardiography reliably predicts pulmonary artery wedge pressure in patients with chronic heart failure with and without mitral re.g.urgitation // J. Am. Coll. Cardiol. - 1996. - Vol. 27. - p. 883–93.
30. Xie G.Y., Berk M.R., Smith M.D., et al. Prognostic value of Doppler transmitral flow patterns in patients with congestive heart failure // J. Am. Coll. Cardiol. - 1994. - Vol. 24. - p. 132–9.
31. Rihal C.S., Nishimura R.A., Hatle L.K., et al. Systolic and diastolic dysfunction in patients with clinical diagnosis of dilated cardiomyopathy. Relation to symptoms and prognosis // Circulation. - 1994. - Vol. 90. - p. 2772–2779.
32. Traversi E., Pozzoli M., Cioffi G., et al. Mitral flow velocity changes after 6 months of optimized therapy provide important hemodynamic and prognostic information in patients with chronic heart failure // Am. Heart J. - 1996. - Vol. 132. - p. 809–19.
33. Giannuzzi P., Temporelli P.L., Bosmini E., et al. Independent and incremental prognostic value of Doppler-derived mitral deceleration time of early filling in both symptomatic and asymptomatic patients with left ventricular dysfunction // J. Am. Coll. Cardiol. - 1996. - Vol. 28. - p. 383–90.
34. Hurrell D.G., Oh J.K., Mahoney D.W., et al. Short deceleration time of mitral inflow E velocity: prognostic implication with atrial fibrillation versus sinus rhythm // J. Am. Soc. Echocardiogr. - 1998. - Vol. 11. - p. 450–7.
35. Hansen A., Haass M., Zugck C., et al. Prognostic value of Doppler echocardiographic mitral inflow patterns: implications for risk stratification in patients with congestive heart failure // J. Am. Coll. Cardiol. - 2001. - Vol. 37. - p. 1049–55.
36. Faris R., Coats A., Henein M. Echocardiography-derived variables predict outcome in patients with non-ischemic dilated cardiomyopathy with or without a restrictive filling pattern // Am. Heart J. - 2002. - Vol. 144. - p. 343–50.
37. Whalley G.A., Doughty R.N., Gamble G.D., et al. Pseudonormal mitral filling pattern predicts hospital re-admission in patients with congestive heart failure // J. Am. Coll. Cardiol. - 2002. - Vol. 39. - p. 1787–95.
38. Rossi A., Cicoira M., Golia G., Zanolla L., et al. Amino-terminal propeptide of type III procollagen is associated with restrictive mitral filling pattern in patients with dilated cardiomyopathy: a possible link between diastolic dysfunction and prognosis // Heart. - 2004. - Vol. 90. - p. 650–4.
39. Bella J.N., Palmieri V., Roman M.J., et al. Mitral ratio of peak early to late diastolic filling velocity as a predictor of mortality in middle-aged and elderly adults: the Strong Heart Study // Circulation. - 2002. - Vol. 105. - p. 1928–33.
40. Pozzoli M., Traversi E., Cioffi G., et al. Loading manipulations improve the prognostic value of Doppler evaluation of mitral flow in patients with chronic heart failure // Circulation. - 1997. - Vol. 95. - p. 1222–30.
41. Pinamonti B., Zecchin M., Di Lenarda A., et al. Persistence of restrictive left ventricular filling pattern in dilated cardiomyopathy: an ominous prognostic sign // J. Am. Coll. Cardiol. - 1997. - Vol. 29. - p. 604–12.
42. Temporelli P.L., Corra U., Imparato A., et al. Reversible restrictive left ventricular diastolic filling with optimized oral therapy predicts a more favorable prognosis in patients with chronic heart failure // J. Am. Coll. Cardiol. - 1998. - Vol. 31. - p. 1591–7.
43. Oh J.K., Ding Z.P., Gersh B.J., et al. Restrictive left ventricular diastolic filling identifies patients with heart failure after acute myocardial infarction // J. Am. Soc. Echocardiogr. – 1992. – Vol. 5. – p. 497–503.
44. Pozzoli M., Capomolla S., Sanarico M., et al. Doppler evaluations of left ventricular diastolic filling and pulmonary wedge pressure provide similar prognostic information in patients with systolic dysfunction after myocardial infarction // Am. Heart J. - 1995. - Vol. 129. - p. 716–25.
45. Nijland F., Kamp O., Karreman A.J., et al. Prognostic implications of restrictive left ventricular filling in acute myocardial infarction: a serial Doppler echocardiographic study // J. Am. Coll. Cardiol. - 1997. - Vol. 30. - p. 1618–24.
46. Sakata K., Kashiro S., Hirata S., et al. Prognostic value of Doppler transmitral flow velocity patterns in acute myocardial infarction // Am. J. Cardiol. - 1997. - Vol. 79. - p. 1165–9.
47. Somaratne J.B., Whalley G.A., Gamble G.D., Doughty R.N. Restrictive filling pattern is a powerful predictor of heart failure events post acute myocardial infarction and in established heart failure: a literature-based meta-analysis // J. Card. Fail. - 2007. - Vol. 13. - p. 346–52.
48. Yamamoto K., Nishimura R.A., Chaliki H.P., et al. Determination of left ventricular filling pressure by Doppler echocardiography in patients with coronary artery disease: critical role of left ventricular systolic function // J. Am. Coll. Cardiol. - 1997. - Vol. 30. - p. 1819–26.
49. Nishimura R.A., Appleton C.P., Redfield M.M., et al. Noninvasive Doppler echocardiographic evaluation of left ventricular filling pressures in patients with cardiomyopathies: a simultaneous Doppler echocardiographic and cardiac catheterization study // J. Am. Coll. Cardiol. - 1996. - Vol. 28. - p. 1226–33.
50. Nagueh S.F., Lakkis N.M., Middleton K.J., et al. Doppler estimation of left ventricular filling pressures in patients with hypertrophic cardiomyopathy // Circulation. - 1999. - Vol. 99. - p. 254–61.
51. Klein A.L., Hatle L.K., Taliercio C.P., et al. Serial Doppler echocardiographic follow-up of left ventricular diastolic function in cardiac amyloidosis // J. Am. Coll. Cardiol. - 1990. - Vol. 16. - p. 1135–41.
52. Klein A.L., Hatle L.K., Taliercio C.P., et al. Prognostic significance of Doppler measures of diastolic function in cardiac amyloidosis. A Doppler echocardiography study // Circulation. - 1991. - Vol. 83. - p. 808–16.
53. Valantine H.A., Appleton C.P., Hatle L.K., et al. A hemodynamic and Doppler echocardiographic study of ventricular function in long-term cardiac allograft recipients. Etiology and prognosis of restrictive-constrictive physiology // Circulation. - 1989. - Vol. 79. - p. 66–75.
54. Appleton C.P. Influence of incremental changes in heart rate on mitral flow velocity: assessment in lightly sedated, conscious dogs // J. Am. Coll. Cardiol. - 1991. - Vol. 17. - p. 227–36.
55. Schnittger I., Appleton C.P., Hatle L.K., Popp R.L. Diastolic mitral and tricuspid regurgitation by Doppler echocardiography in patients with atrioventricular block: new insight into the mechanism of atrioventricular valve closure // J. Am. Coll. Cardiol. - 1988. - Vol. 11. - p. 83–8.
56. Nishimura R.A., Tajik A.J. The Valsalva maneuver – 3 centuries later // Mayo Clin. Proc. - 2004. - Vol. 79. - p. 577–8.
57. Hurrell D., Nishimura R.A., Ilstrup D.M., Appleton C.P. Utility of preload alteration in assessment of left ventricular filling pressure by Doppler echocardiography: a simultaneous catheterization and Doppler echocardiographic study // J. Am. Coll. Cardiol. - 1997. - Vol. 30. - p. 459–67.
58. Jensen J.L., Williams F.E., Beilby B.J., et al. Feasibility of obtaining pulmonary venous flow velocity in cardiac patients using transthoracic pulsed wave Doppler technique // J. Am. Soc. Echocardiogr. - 1997. - Vol. 10. - p. 60–6.
59. Appleton C.P. Hemodynamic determinants of Doppler pulmonary venous flow velocity components: new insights from studies in lightly sedated normal dogs // J. Am. Coll. Cardiol. - 1997. - Vol. 30. - p. 1562–74.
60. Smiseth O.A., Thompson C.R., Lohavanichbutr K., et al. The pulmonary venous systolic flow pulse – its origin and relationship to left atrial pressure // J. Am. Coll. Cardiol. - 1999. - Vol. 34. - p. 802–9.
61. Nishimura R.A., Abel M.D., Hatle L.K., Tajik A.J. Relation of pulmonary vein to mitral flow velocities by transesophageal Doppler echocardiography. Effect of different loading conditions // Circulation. - 1990. - Vol. 81. - p. 1488–97.
62. Keren G., Bier A., Sherez J., Miura D., et al. Atrial contraction is an important determinant of pulmonary venous flow // J. Am. Coll. Cardiol. - 1986. - Vol. 7. - p. 693–5.
63. Kuecherer H.F., Muhiudeen I.A., Kusumoto F.M., et al. Estimation of mean left atrial pressure from transesophagealpulsed Doppler echocardiography of pulmonary venous flow // Circulation. - 1990. - Vol. 82. - p. 1127–39.
64. Yamamuro A., Yoshida K., Hozumi T., et al. Noninvasive evaluation of pulmonary capillary wedge pressure in patients with acute myocardial infarction by deceleration time of pulmonary venous flow velocity in diastole // J. Am. Coll. Cardiol. - 1999. - Vol. 34. - p. 90–4.
65. Rossvoll O., Hatle L.K. Pulmonary venous flow velocities recorded by transthoracic Doppler ultrasound: relation to left ventricular diastolic pressures // J. Am. Coll. Cardiol. - 1993. - Vol. 21. - p. 1687–96.
66. Appleton C.P., Galloway J.M., Gonzalez M.S., et al. Estimation of left ventricular filling pressures using two-dimensional and Doppler echocardiography in adult patients with cardiac disease. Additional value of analyzing left atrial size, left atrial ejection fraction and the difference in duration of pulmonary venous and mitral flow velocity at atrial contraction // J. Am. Coll. Cardiol. - 1993. - Vol. 22. - p. 1972–82.
67. Klein A.L., Tajik A.J. Doppler assessment of pulmonary venous flow in healthy subjects and in patients with heart disease // J. Am. Soc. Echocardiogr. - 1991. - Vol. 4. - p. 379–92.
68. Nagueh S.F., Kopelen H.A., Quinones M.A. Assessment of left ventricular filling pressures by Doppler in the presence of atrial fibrillation // Circulation. - 1996. - Vol. 94. - p. 2138–45.
69. Diwan A., McCulloch M., Lawrie G.M., et al. Doppler estimation of left ventricular filling pressures in patients with mitral valve disease // Circulation. - 2005. - Vol. 111. - p. 3281–9.
70. Rossi A., Cicoira M., Golia G., et al. Mitral regurgitation and left ventricular diastolic dysfunction similarly affect mitral and pulmonary vein flow Doppler parameters: the advantage of end-diastolic markers // J. Am. Soc. Echocardiogr. - 2001. - Vol. 14. - p. 562–8.
71. Poulsen S.H., Jensen S.E., Gotzsche O., Egstrup K. Evaluation and prognostic significance of left ventricular diastolic function assessed by Doppler echocardiography in the early phase of a first acute myocardial infarction // Eur. Heart. J. - 1997. - Vol. 18. - p. 1882–9.
72. Dini F., Michelassi C., Micheli G., Rovai D. Prognostic value of pulmonary venous flow Doppler signal in left ventricular dysfunction: contribution of the difference in duration of pulmonary venous and mitral flow at atrial contraction // J. Am. Coll. Cardiol. - 2000. - Vol. 36. - p. 1295–302.
73. Dini F.L., Dell’Anna R., Micheli A., et al. Impact of blunted pulmonary venous flow on the outcome of patients with left ventricular systolic dysfunction secondary to either ischemic or idiopathic dilated cardiomyopathy // Am. J. Cardiol. - 2000. - Vol. 85. - p. 1455–60.
74. Brun P., Tribouilloy C., Duval A.M., et al. Left ventricular flow propagation during early filling is related to wall relaxation: a color M-mode Doppler analysis // J. Am. Coll. Cardiol. - 1992. - Vol. 20. - p. 420–32.
75. Garcia M.J., Ares M.A., Asher C., et al. An index of early left ventricular filling that combined with pulsed Doppler peak E velocity may estimate capillary wedge pressure // J. Am. Coll. Cardiol. - 1997. - Vol. 29. - p. 448–54.
76. Sessoms M.W., Lisauskas J., Kovacs S.J. The left ventricular color M-mode Doppler flow propagation velocity V(p): in vivo comparison of alternative methods including physiologic implications // J. Am. Soc. Echocardiogr. - 2002. - Vol. 15. - p. 339–48.
77. Takatsuji H., Mikami T., Urasawa K., et al. A new approach for evaluation of left ventricular diastolic function: spatial and temporal analysis of left ventricular filling flow propagation by color M-mode Doppler echocardiography // J. Am. Coll. Cardiol. - 1996. - Vol. 27. - p. 365–71.
78. Greenberg N.L., Vandervoort P.M., Firstenberg M.S., et al. Estimation of diastolic intraventricular pressure gradients by Doppler M-mode echocardiography // Am. J. Physiol. - Heart Circ Physiol 2001. - Vol. 280. - p. H2507–15.
79. Yotti R., Bermejo J., Antoranz J.C., et al. A noninvasive method for assessing impaired diastolic suction in patients with dilated cardiomyopathy // Circulation. - 2005. - Vol. 112. - p. 2921–9.
80. Courtois M., Kovacs S.J. Jr., Ludbrook P.A. Physiological early diastolic intraventricular pressure gradient is lost during acute myocardial ischemia // Circulation. - 1990. - Vol. 81. - p. 1688–96.
81. Stugaard M., Smiseth O.A., Risoe C., Ihlen H. Intraventricular early diastolic filling during acute myocardial ischemia. Assessment by multigated color M-mode Doppler echocardiography // Circulation. - 1993. - Vol. 88. - p. 2705–13.
82. Steine K., Stugaard M., Smiseth O.A. Mechanisms of retarded apical filling in acute ischemic left ventricular failure // Circulation. - 1999. - Vol. 99. - p. 2048–54.
83. Ohte N., Narita H., Akita S., et al. Striking effect of left ventricular systolic performance on propagation velocity of left ventricular early diastolic filling flow // J. Am. Soc. Echocardiogr. - 2001. - Vol. 14. - p. 1070–4.
84. Rovner A., de las Fuentes L., Waggoner A.D., et al. Characterization of left ventricular diastolic function in hypertension by use of Doppler tissue imaging and color M-mode techniques // J. Am. Soc. Echocardiogr. - 2006. - Vol. 19. - p. 872–9.
85. Gonzalez-Vilchez F., Ares M., Ayuela J., Alonso L. Combined use of pulsed and color M-mode Doppler echocardiography for the estimation of pulmonary capillary wedge pressure: an empirical approach based on an analytical relation // J. Am. Coll. Cardiol. - 1999. - Vol. 34. - p. 515–23.
86. Rivas-Gotz C., Manolios M., Thohan V., Nagueh S.F. Impact of left ventricular ejection fraction on estimation of left ventricular filling pressures using tissue Doppler and flow propagation velocity // Am. J. Cardiol. - 2003. - Vol. 91. - p. 780–4.
87. Graham R.J., Gelman J.S., Donelan L., et al. Effect of preload reduction by haemodialysis on new indices of diastolic function // Clin. Sci. (Lond). - 2003. - Vol. 105. - p. 499–506.
88. Troughton R.W., Prior D.L., Frampton C.M., et al. Usefulness of tissue Doppler and color M-mode indexes of left ventricular diastolic function in predicting outcomes in systolic left ventricular heart failure (from the ADEPT study) // Am. J. Cardiol. - 2005. - Vol. 96. - p. 257–62.
89. Waggoner A.D., Bierig S.M. Tissue Doppler imaging: a useful echocardiographic method for the cardiac sonographer to assess systolic and diastolic left ventricular function // J. Am. Soc. Echocardiogr. - 2001. - Vol. 14. - p. 1143–52.
90. Nagueh S.F., Middleton K.J., Kopelen H.A., et al. Doppler tissue imaging: a non-invasive technique for evaluation of left ventricular relaxation and estimation of filling pressures // J. Am. Coll. Cardiol. - 1997. - Vol. 30. - p. 1527–33.
91. Ruan Q., Rao L., Middleton K.J., et al. Assessment of left ventricular diastolic function by early diastolic mitral annulus peak acceleration rate. - p. experimental studies and clinical application // J. Appl. Physiol. - 2006. - Vol. 100. - p. 679–84.
92. Nagueh S.F., Rao L., Soto J., et al. Haemodynamic insights into the effects of ischaemia and cycle length on tissue Dopplerderived mitral annulus diastolic velocities // Clin. Sci. (Lond). - 2004. - Vol. 106. - p. 147–54.
93. Nagueh S.F., Sun H., Kopelen H.A., et al. Hemodynamic determinants of mitral annulus diastolic velocities by tissue Doppler // J. Am. Coll. Cardiol. - 2001. - Vol. 37. - p. 278–85.
94. Hasegawa H., Little W.C., Ohno M., et al. Diastolic mitral annular velocity during the development of heart failure // J. Am. Coll. Cardiol. - 2003. - Vol. 41. - p. 1590–7.
95. Oki T., Tabata T., Yamada H., et al. Clinical application of pulsed tissue Doppler imaging for assessing abnormal left ventricular relaxation // Am. J. Cardiol. - 1997. - Vol. 79. - p. 921–8.
96. Sohn D., Chai I., Lee D., et al. Assessment of mitral annulus velocity by Doppler tissue imaging in evaluation of left ventricular diastolic function // J. Am. Coll. Cardiol. - 1997. - Vol. 30. - p. 474–80.
97. Oммen S.R., Nishimura R.A., Appleton C.P., et al. Clinical utility of Doppler echocardiography and tissue Doppler imaging in the estimation of left ventricular filling pressures: a comparative simultaneous Doppler-catheterization study // Circulation. - 2000. - Vol. 102. - p. 1788–94.
98. Firstenberg M.S., Levine B.D., Garcia M.J., et al. Relationship of echocardiographic indices to pulmonary capillary wedge pressures in healthy volunteers // J. Am. Coll. Cardiol. - 2000. - Vol. 36. - p. 1664–9.
99. Caiani E.G., Weinert L., Takeuchi M., et al. Evaluation of alterations on mitral annulus velocities, strain, and strain rates due to abrupt changes in preload elicited by parabolic flight // J. Appl. Physiol. - 2007. - Vol. 103. - p. 80–7.
100. Rivas-Gotz C., Khoury D.S., Manolios M., et al. Time interval between onset of mitral inflow and onset of early diastolic velocity by tissue Doppler: a novel index of left ventricular relaxation: experimental studies and clinical application // J. Am. Coll. Cardiol. - 2003. - Vol. 42. - p. 1463–70.
101. De Sutter J., De Backer J., Van de Veire N., et al. Effects of age, gender, and left ventricular mass on septal mitral annulus velocity (E’) and the ratio of transmitral early peak velocity to E’ (E/Е’) // Am. J. Cardiol. - 2005. - Vol. 95. - p. 1020–3.
102. Nagueh S.F., Mikati I., Kopelen H.A., et al. Doppler estimation of left ventricular filling pressure in sinus tachycardia. A new application of tissue Doppler imaging // Circulation. - 1998. - Vol. 98. - p. 1644–50.
103. Kim Y.J., Sohn D.W. Mitral annulus velocity in the estimation of left ventricular filling pressure: prospective study in 200 patients // J. Am. Soc. Echocardiogr. - 2000. - Vol. 13. - p. 980–5.
104. Sohn D.W., Song J.M., Zo J.H., et al. Mitral annulus velocity in the evaluation of left ventricular diastolic function in atrial fibrillation // J. Am. Soc. Echocardiogr. - 1999. - Vol. 12. - p. 927–31.
105. Sohn D.W., Kim Y.J., Kim H.C., et al. Evaluation of left ventricular diastolic function when mitral E and A waves are completely fused: role of assessing mitral annulus velocity // J. Am. Soc. Echocardiogr. - 1999. - Vol. 12. - p. 203–8.
106. Kasner M., Westermann D., Steendijk P., et al. Utility of Doppler echocardiography and tissue Doppler imaging in the estimation of diastolic function in heart failure with normal ejection fraction: a comparative Doppler-conductance catheterization study // Circulation. - 2007. - Vol. 11. - p. 637–47.
107. Min P.K., Ha J.W., Jung J.H., et al. Incremental value of measuring the time difference between onset of mitral inflow and onset of early diastolic mitral annulus velocity for the evaluation of left ventricular diastolic pressures in patients with normal systolic function and an indeterminate E/Е’ // Am. J. Cardiol. - 2007. - Vol. 100. - p. 326–30.
108. Ha J.W., Oh J.K., Ling L.H., et al. Annulus paradoxus: transmitral flow velocity to mitral annular velocity ratio is inversely proportional to pulmonary capillary wedge pressure in patients with constrictive pericarditis // Circulation. - 2001. - Vol. 104. - p. 976–8.
109. Heimdal A., Stoylen A., Torp H., Skjaerpe T. Real-time strain rate imaging of the left ventricle by ultrasound // J. Am. Soc. Echocardiogr. - 1998. - Vol. 11. - p. 1013–9.
110. Urheim S., Edvardsen T., Torp H., et al. Myocardial strain by Doppler echocardiography. Validation of a new method to quantify re.g.ional myocardial function // Circulation. - 2000. - Vol. 102. - p. 1158–64.
111. Langeland S., D’hooge J., Wouters P.F., et al. Experimental validation of a new ultrasound method for the simultaneous assessment of radial and longitudinal myocardial deformation independent of insonation angle // Circulation. - 2005. - Vol. 112. - p. 2157–62.
112. Amundsen B.H., Helle-Valle T., Edvardsen T., et al. Noninvasive myocardial strain measurement by speckle tracking echocardiography: validation against sonomicrometry and tagged magnetic resonance imaging // J. Am. Coll. Cardiol. - 2006. - Vol. 47. - p. 789–93.
113. Voigt J.U., Exner B., Schmiedehausen K., et al. Strain-rate imaging during dobutamine stress echocardiography provides objective evidence of inducible ischemia // Circulation. - 2003. - Vol. 107. - p. 2120–6.
114. Pislaru C., Bruce C.J., Anagnostopoulos P.C., et al. Ultrasound strain imaging of altered myocardial stiffness: stunned versus infarcted reperfused myocardium // Circulation. - 2004. - Vol. 109. - p. 2905–10.
115. Park T.H., Nagueh S.F., Khoury D.S., et al. impact of myocardial structure and function postinfarction on diastolic strain measurements: implications for assessment of myocardial viability // Am. J. Physiol. - Heart Circ Physiol 2006. - Vol. 290. - p. H724–31.
116. Abraham T.P., Belohlavek M., Thomson H.L., et al. Time to onset of regional relaxation: feasibility, variability and utility of a novel index of regional myocardial function by strain rate imaging // J. Am. Coll. Cardiol. - 2002. - Vol. 39. - p. 1531–7.
117. Kato T., Noda A., Izawa H., et al. Myocardial velocity gradient as a noninvasively determined index of left ventricular diastolic dysfunction in patients with hypertrophic cardiomyopathy // J. Am. Coll. Cardiol. - 2003. - Vol. 42. - p. 278–85.
118. Wang J., Khoury D.S., Thohan V., et al. Global diastolic strain rate for the assessment of left ventricular relaxation and filling pressures // Circulation. - 2007. - Vol. 115. - p. 1376–83.
119. Rademakers F.E., Buchalter M.B., Rogers W.J., et al. Dissociation between left ventricular untwisting and filling. Accentuation by catecholamines // Circulation. - 1992. - Vol. 85. - p. 1572–81.
120. Bell S.P., Nyland L., Tischler M.D., et al. Alterations in the determinants of diastolic suction during pacing tachycardia // Circ. Res. - 2000. - Vol. 87. - p. 235–40.
121. DeAnda A. Jr., Komeda M., Nikolic S.D, et al. Left ventricular function, twist, and recoil after mitral valve replacement // Circulation. - 1995. - Vol. 92(suppl). - p. II58–66.
122. Gibbons Kroeker C.A., Tyberg J.V., Beyar R. Effects of ischemia on left ventricular apex rotation: an experimental study in anesthetized dogs // Circulation. - 1995. - Vol. 92. - p. 130–41.
123. Fuchs E., Muller M.F., Oswald H., et al. Cardiac rotation and relaxation in patients with chronic heart failure // Eur. J. Heart Fail. - 2004. - Vol. 6. - p. 715–22.
124. Hees P.S., Fleg J.L., Dong S.J., Shapiro E.P. MRI and echocardiographic assessment of the diastolic dysfunction of normal aging: altered LV pressure decline or load? // Am. J. Physiol. - Heart Circ. Physiol. 2004. - Vol. 286. - p. H782–8.
125. Notomi Y., Martin-Miklovic M.G., Oryszak S.J., et al. Enhanced ventricular untwisting during exercise. - p. a mechanistic manifestation of elastic recoil described by Doppler tissue imaging // Circulation. - 2006. - Vol. 113. - p. 2524–33.
126. Dong S.J., Hees P.S., Siu C.O., et al. MRI assessment of LV relaxation by untwisting rate. - p. a new isovolumic phase measure of tau // Am. J. Physiol. - Heart Circ Physiol 2001. - Vol. 281. - p. H2002–9.
127. Notomi Y., Lysyansky P., Setser R.M., et al. Measurement of ventricular torsion by twodimensional ultrasound speckle tracking imaging // J. Am. Coll. Cardiol. - 2005. - Vol. 45. - p. 2034–41.
128. Helle-Valle T., Crosby J., Edvardsen T., et al. New noninvasive method for assessment of left ventricular rotation. - p. speckle tracking echocardiography // Circulation. - 2005. - Vol. 112. - p. 3149–56.
129. Wang J., Khoury D.S., Yue Y., et al. Left ventricular untwisting rate by speckle tracking echocardiography // Circulation. - 2007. - Vol. 116. - p. 2580–6.
130. Park S.J., Miyazaki C., Bruce C.J., et al. Left ventricular torsion by two-dimensional speckle tracking echocardiography in patients with diastolic dysfunction and normal ejection fraction // J. Am. Soc. Echocardiogr. - 2008. - Vol. 21. - p. 1129–37.
131. Scalia G.M., Greenberg N.L., McCarthy P.M., et al. Noninvasive assessment of the ventricular relaxation time constant (tau) in humans by Doppler echocardiography // Circulation. - 1997. - Vol. 95. - p. 151–5.
132. Yamamoto K., Masuyama T., Doi Y., et al. Noninvasive assessment of LV relaxation using continuous wave Doppler aortic regurgitant velocity curve. - p. its comparative value to the mitral regurgitation method // Circulation. - 1995. - Vol. 91. - p. 192–200.
133. Honda Y., Yokota Y., Yokoyama M. Evaluation of left ventricular relaxation using the continuous-wave Doppler velocity profile of aortic regurgitation. - p. noninvasive measurement of left ventricular negative dP/dt and time constant // Clin. Cardiol. - 1996. - Vol. 19. - p. 709–15.
134. Nishimura R.A., Schwartz R.S., Tajik A.J., Holmes D.R. Jr. Noninvasive measurement of rate of left ventricular relaxation by Doppler echocardiography. - p. validation with simultaneous cardiac catheterization // Circulation. - 1993. - Vol. 88. - p. 146–55.
135. Zile M.R., Baicu C.F., Gaasch W.H. Diastolic heart failure—abnormalities in active relaxation and passive stiffness of the left ventricle // N. Engl. J. Med. - 2004. - Vol. 350. - p. 1953–9.
136. Gorcsan J. III, Gasior T.A., Mandarino W.A., et al. Assessment of the iммediate effects of cardiopulmonary bypass on left ventricular performance by on-line pressure-area relations // Circulation. - 1994. - Vol. 89. - p. 180–90.
137. Ohno M., Cheng C.P., Little W.C. Mechanism of altered patterns of left ventricular filling during the development of congestive heart failure // Circulation. - 1994. - Vol. 89. - p. 2241–50.
138. Little W.C., Ohno M., Kitzman D.W., et al. Determination of left ventricular chamber stiffness from the time for deceleration of early left ventricular filling // Circulation. - 1995. - Vol. 92. - p. 1933–9.
139. Marino P., Faggian G., Bertolini P., et al. Early mitral deceleration and left atrial stiffness // Am. J. Physiol. - Heart Circ Physiol 2004. - Vol. 287. - p. H1172–8.
140. Garcia M.J., Firstenberg M.S., Greenberg N.L., et al. Estimation of left ventricular operating stiffness from Doppler early filling deceleration time in humans // Am. J. Physiol. - Heart Circ. Physiol. – 2001. – Vol. 280. – p. H554–61.
141. Marino P., Little W.C., Rossi A., et al. Can left ventricular diastolic stiffness be measured noninvasively? // J. Am. Soc. Echocardiogr. - 2002. - Vol. 15. - p. 935–43.
142. Shmuylovich L., Kovacs S.J. E-wave deceleration time may not provide an accurate determination of LV chamber stiffness if LV relaxation/viscoelasticity is unknown // Am. J. Physiol. - Heart Circ. Physiol. – 2007. – Vol. 292. – p. H2712–20.
143. Pai R.G., Suzuki M., Heywood T., et al. Mitral A velocity wave transit time to the outflow tract as a measure of left ventricular diastolic stiffness. Hemodynamic correlations in patients with coronary artery disease // Circulation. - 1994. - Vol. 89. - p. 553–7.
144. Pai R.G., Varadarajan P. Relative duration of transmitted mitral A wave as a measure of left ventricular end-diastolic pressure and stiffness. Echocardiography 2004. - Vol. 21. - p. 27–31.
145. Ha J.W., Lulic F., Bailey K.R., et al. Effects of treadmill exercise on mitral inflow and annular velocities in healthy adults // Am. J. Cardiol. - 2003. - Vol. 91. - p. 114–5.
146. Ha J.W., Oh J.K., Pellikka P.A., et al. Diastolic stress echocardiography. - p. a novel noninvasive diagnostic test for diastolic dysfunction using supine bicycle exercise Doppler echocardiography // J. Am. Soc. Echocardiogr. - 2005. - Vol. 18. - p. 63–8.
147. Burgess M.I., Jenkins C., Sharman J.E.,. Diastolic stress echocardiography. - p. hemodynamic validation and clinical significance of estimation of ventricular filling pressure with exercise // J. Am. Coll. Cardiol. - 2006. - Vol. 47. - p. 1891–900.
148. Duncan A.M., Lim E., Gibson D.G., Henein M.Y. Effect of dobutamine stress on left ventricular filling in ischemic dilated cardiomyopathy. - p. pathophysiology and prognostic implications // J. Am. Coll. Cardiol. - 2005. - Vol. 46. - p. 488–96.
149. Hatle L., Appleton C.P., Popp R. Differentiation of constrictive pericarditis and restrictive cardiomyopathy by Doppler echocardiography // Circulation. - 1989. - Vol. 79. - p. 357–70.
150. Oh J.K., Hatle L., Seward J.B., et al. Diagnostic role of Doppler echocardiography in constrictive pericarditis // J. Am. Coll. Cardiol. - 1994. - Vol. 23. - p. 154–62.
151. Tabata T., Kabbani S.S., Murray R.D., et al. Difference in the respiratory variation between pulmonary venous and mitral inflow Doppler velocities in patients with constrictive pericarditis with and without atrial fibrillation // J. Am. Coll. Cardiol. - 2001. - Vol. 37. - p. 1936–42.
152. Garcia M., Rodriguez L., Ares M., et al. Differentiation of constrictive pericarditis from restrictive cardiomyopathy. - p. assessment of left ventricular diastolic velocities in longitudinal axis by Doppler tissue imaging // J. Am. Coll. Cardiol. - 1996. - Vol. 27. - p. 108–14.
153. Ha J., Oммen S.R., Tajik A.J., et al. Differentiation of constrictive pericarditis from restrictive cardiomyopathy using mitral annular velocity by tissue Doppler echocardiography // Am. J. Cardiol. - 2004. - Vol. 94. - p. 316–9.
154. Choi E.Y., Ha J.W., Kim J.M., et al. Incremental value of combining systolic mitral annular velocity and time difference between mitral inflow and diastolic mitral annular velocity to early diastolic annular velocity for differentiating constrictive pericarditis from restrictive cardiomyopathy // J. Am. Soc. Echocardiogr. - 2007. - Vol. 20. - p. 738–43. 192 Nagueh et al.
155. Sohn D.W., Kim Y., Kim H.S., et al. Unique features of early diastolic mitral annulus velocity in constrictive pericarditis // J. Am. Soc. Echocardiogr. - 2004. - Vol. 17. - p. 222–6.
156. Olson J.J., Costa S.P, Young C.E., Palac R.T. Early mitral filling/diastolic mitral annular velocity ratio is not a reliable predictor of left ventricular filling pressure in the setting of severe mitral re.g.urgitation // J. Am. Soc. Echocardiogr. - 2006. - Vol. 19. - p. 83–7.
157. Bruch C., Stypmann J., Gradaus R., et al. Usefulness of tissue Doppler imaging for estimation of filling pressures in patients with primary or secondary pure mitral re.g.urgitation // Am. J. Cardiol. - 2004. - Vol. 93. - p. 324–8.
158. Temporelli P.L., Scapellato F., Corra U., et al. Estimation of pulmonary wedge pressure by transmitral Doppler in patients with chronic heart failure and atrial fibrillation // Am. J. Cardiol. - 1999. - Vol. 83. - p. 724–7.
159. Chirillo F., Brunazzi M.C., Barbiero M., et al. Estimating mean pulmonary wedge pressure in patients with chronic atrial fibrillation from transthoracic Doppler indexes of mitral and pulmonary venous flow velocity // J. Am. Coll. Cardiol. - 1997. - Vol. 30. - p. 19–26.
160. Appleton C.P., Hatle L.K., Popp R.L. Demonstration of restrictive ventricular physiology by Doppler echocardiography // J. Am. Coll. Cardiol. - 1988. - Vol. 11. - p. 757–68.
161. Geske J.B., Sorajja P., Nishimura R.A., Oммen S.R. Evaluation of left ventricular filling pressures by Doppler echocardiography in patients with hypertrophic cardiomyopathy. - p. correlation with direct left atrial pressure measurement at cardiac catheterization // Circulation. - 2007. - Vol. 116. - p. 2702–8.
162. Menzel T., Wagner S., Kraмм T., et al. Pathophysiology of impaired right and left ventricular function in chronic embolic pulmonary hypertension. - p. changes after pulmonary thromboendarterectomy // Chest. - 2000. - Vol. 118. - p. 897–903.
163. Ruan Q., Nagueh S.F. Clinical application of tissue Doppler imaging in patients with idiopathic pulmonary hypertension // Chest. - 2007. - Vol. 131. - p. 395–401.
164. Moller J.E., Sondergaard E., Seward J.B., et al. Ratio of left ventricular peak E-wave velocity to flow propagation velocity assessed by color M-mode Doppler echocardiography in first myocardial infarction. - p. prognostic and clinical implications // J. Am. Coll. Cardiol. - 2000. - Vol. 35. - p. 363–70.
165. Moller J.E., Sondergaard E., Poulsen S.H., Egstrup K. Pseudonormal and restrictive filling patterns predict left ventricular dilation and cardiac death after a first myocardial infarction. - p. a serial color M-mode Doppler echocardiographic study // J. Am. Coll. Cardiol. - 2000. - Vol. 36. - p. 1841–6.
166. Moller J.E., Sondergaard E., Poulsen S.H., et al. Color M-mode and pulsed wave tissue Doppler echocardiography. - p. powerful predictors of cardiac events after first myocardial infarction // J. Am. Soc. Echocardiogr. - 2001. - Vol. 14. - p. 757–63.
167. Wang M., Yip G.W., Wang A.Y., et al. Peak early diastolic mitral annulus velocity by tissue Doppler imaging adds independent and incremental prognostic value // J. Am. Coll. Cardiol. - 2003. - Vol. 41. - p. 820–6.
168. Yamamoto T., Oki T., Yamada H., et al. Prognostic value of the atrial systolic mitral annular motion velocity in patients with left ventricular systolic dysfunction // J. Am. Soc. Echocardiogr. - 2003. - Vol. 16. - p. 333–9.
169. Redfield M.M., Jacobsen S.J., Burnett J.C. Jr., et al. Burden of systolic and diastolic ventricular dysfunction in the coммunity. - p. appreciating the scope of the heart failure epidemic // JAMA. - 2003. - Vol. 289. - p. 194–202.
170. Hillis G.S., Moller J.E., Pellikka P.A., et al. Noninvasive estimation of left ventricular filling pressure by E/Е’ is a powerful predictor of survival after acute myocardial infarction // J. Am. Coll. Cardiol. - 2004. - Vol. 43. - p. 360–7.
171. Wang M., Yip G., Yu CM., et al. Independent and incremental prognostic value of early mitral annulus velocity in patients with impaired left ventricular systolic function // J. Am. Coll. Cardiol. - 2005. - Vol. 45. - p. 272–7.
172. Dokainish H., Zoghbi W.A., Lakkis N.M., et al. Incremental predictive power of B-type natriuretic peptide and tissue Doppler echocardiography in the prognosis of patients with congestive heart failure // J. Am. Coll. Cardiol. - 2005. - Vol. 45. - p. 1223–6.
173. Wang M., Yip G.W., Wang A.Y., et al. Tissue Doppler imaging provides incremental prognostic value in patients with systemic hypertension and left ventricular hypertrophy // J. Hypertens. - 2005. - Vol. 23. - p. 183–91.
174. Sharma R., Pellerin D., Gaze D.C., et al. Mitral peak Doppler E-wave to peak mitral annulus velocity ratio is an accurate estimate of left ventricular filling pressure and predicts mortality in end-stage renal disease // J. Am. Soc. Echocardiogr. - 2006. - Vol. 19. - p. 266–73.
175. Okura H., Takada Y., Kubo T., et al. Tissue Doppler-derived index of left ventricular filling pressure, E/Е’, predicts survival of patients with non-valvular atrial fibrillation // Heart. - 2006. - Vol. 92. - p. 1248–52.
176. Bruch C., Klem I., Breithardt G., et al. Diagnostic usefulness and prognostic implications of the mitral E/Е’ ratio in patients with heart failure and severe secondary mitral re.g.urgitation // Am. J. Cardiol. - 2007. - Vol. 100. - p. 860–5.
177. McMahon C.J., Nagueh S.F., Pignatelli R.H., et al. Characterization of left ventricular diastolic function by tissue Doppler imaging and clinical status in children with hypertrophic cardiomyopathy // Circulation. - 2004. - Vol. 109. - p. 1756–62.
178. McMahon C.J., Nagueh S.F., Eapen R.S., et al. Echocardiographic predictors of adverse clinical events in children with dilated cardiomyopathy. - p. a prospective clinical study // Heart. - 2004. - Vol. 90. - p. 908–15.
179. Carson P., Massie B.M., McKelvie .R, et al. for the I-PRESERVE Investigators. The Irbesartan in Heart Failure With Preserved Systolic Function (I-PRESERVE) trial. - p. rationale and design // J. Card. Fail. - 2005. - Vol. 11. - p. 576–85.