Рекомендації робочої групи з функціональної діагностики Асоціації кардіологів України та Всеукраїнської асоціації фахівців з ехокардіографії
Члени робочої групи з підготовки рекомендацій: акад. НАМН України, проф. В.М. Коваленко, проф. Сичов О.С., проф. М.М. Долженко, проф. Ю.А. Іванів, к.м.н. С.І. Деяк, к.м.н. С.В. Поташев
Кількісна оцінка порожнин серця, маси міокарду лівого шлуночка (ЛШ) та функції є однією з клінічно найважливіших та найбільш частих завдань ехокардіографії (ЕхоКГ). Стандартизація кількісної оцінки порожнин серця була однією з найбільш ранніх завдань, що вирішувала ЕхоКГ, а рекомендації з вимірів основних параметрів найбільш часто цитуються в даній області [1,2]. За останні десятиріччя ехокардіографічні методики та технології драматично покращились та виросли кількісно та якісно. Покращення візуалізації в останні роки було значним в результаті застосування високочастотних датчиків, візуалізації за допомогою «гармоніки», цифрової обробки зображення, застосування контрастних агентів, тощо.
Сьогодні ЕхоКГ є домінантною технологією візуалізації в кардіології, та, завдяки своїй компактності та портативності, сьогодні широко застосовується в реанімації та інтенсивній терапії, та інтраопераційно. До сьогодні не було чіткої та, порівняно з іншими техніками візуалізації, вдалої стандартизації вимірів в ЕхоКГ, в наслідок чого виміри в ЕхоКГ сьогодні часто сприймаються в медичному товаристві як менш надійні. Тому ми вважали за доцільне після вивчення відповідних літературних джерел, засновуючись на досвіді провідних товариств в ЕхоКГ, оновити та видати рекомендації з кількісної оцінки камер серця за даними ЕхоКГ. На жаль, не всі наведені нижче в статті виміри можуть бути виконані в усіх пацієнтів по причині технічних обмежень. Крім того, специфічні виміри можуть бути клінічно недоцільними у певних ситуаціях. Дана стаття розглядає технічні аспекти того, як виконувати кількісні виміри порожнин серця, та не спрямована на описання стандартів надання допомоги, в яких треба застосовувати ці виміри в окремих клінічних випадках. Втім, оцінка розмірів та функції камер серця має бути обов’язковим компонентом кожного повноцінного ЕхоКГ дослідження, а самі виміри мають впливати на прийняття певних клінічних рішень.
Загальний огляд
Покращення якості зображення було наслідком технологічних удосконалень, таких як застосування широкополосних датчиків, візуалізації в режимі «гармоніки» та контрастування лівих відділів серця. Втім, оптимізація зображення сьогодні все ще потребує значних зусиль та уваги до певних деталей, специфічних для окремих доступів (Таб. 1). В цілому, види, що використовуються для вимірів одної камери, можуть бути зовсім неоптимальними для візуалізації та вимірювання інших кардіальних структур. Важливим також є положення пацієнта підчас візуалізації. Найбільш оптимальні види кардіальних структур зазвичай отримують при положенні пацієнта в положенні лежачи на лівому боці з використанням вирізаного вікна в кушетці, що дозволяє візуалізувати істинну верхівку та запобіг нути штучного укорочення ЛШ. Ліва рука пацієнта повинна бути заведеною догори за голову для розширення міжреберних проміжків. Треба запобігати глибокого дихання пацієнта. Якщо зображення отримується наприкінці видиху, треба переконатися, що не виникає ефекту проби Вальсальви, що може суттєво зіпсувати якість зображення.
Таб. 1. Елементи отримання двомірного зображення та кількісних вимірів.
|
Мета
|
Метод
|
|
Мінімізація дихальних рухів
|
Неглибоке пригнічування дихання пацієнтом
|
|
Збільшення розрішення зображення
|
· Зображення на мінімальній глибині
· Найбільша можлива частота датчика
· Настройки підсилення, динамічного простору, бокового підсилення
· Частота кадру >30/с
· Використання «гармоніки»
· Псевдоколоризація в В-режимі
|
|
Запобігання штучного укорочення ЛШ («зрізання» верхівки.
|
· Положення пацієнта лежачи на лівому боці
· Кушетка з вирізаним вікном для апікального доступу
· Не використовувати пальпацію верхівкового поштовху для виведення апікальних позицій
|
|
Оптимізація границь ендокарду
|
Використання засобів контрастної оптимізації зображення
|
|
Визначення кінцево-діастолічної та кінцево-систолічної позицій
|
Орієнтація на рух мітрального клапану та розміри камери ЛШ та ЛП, а не на ЕКГ*
|
* - ЕКГ – електрокардіограма.
Цифровий захват та виведення зображення на екран в ехокардіографії чи робочій станції повинні відповідати оптимальній якості зображення з частотою щонайменш 30 кадрів/сек. В рутинній клінічній практиці будь який репрезентативний серцевий цикл може бути використаний для виконання вимірів, якщо у пацієнта синусовий ритм. При фібриляції передсердь, особливо у випадках, коли має місце велика варіабельність R-R, для вимірів треба використовувати декілька циклів. Усереднення вимірів з декількох серцевих циклів може бути особливо корисним при високому рівні нерегулярності R-R. У випадку суправентрикулярних або шлуночкових екстрасистол слід запобігати проведення вимірів в постектопічному циклі, тому що тривалість попереднього кардіального циклу може вплинути на об’єми порожнин та ступінь скорочення кардіальних волокон.
Візуалізація з використанням «гармоніки» сьогодні широко використовується в клінічній практиці для підсилення якості зображення, особливо у пацієнтів з неоптимальним акустичним вікном. Хоча ця техніка зменшує ефект випадіння ехо-сигналів від ендокардіальних границь, в літературі постійно з’являються повідомлення про системну тенденцію до завишення вимірів товщини стінок ЛШ та заниження вимірів внутрішніх розмірів та об’ємів підчас ЕхоКГ [3, 4]. При аналізі серійних ЕхоКГ досліджень на певних пацієнтах виявлялося, що різниця між вимірами камер серця завдяки змінам візуалізації від звичайного В-режиму до «гармоніки» була меншою, ніж різниця між вимірами різними дослідниками, та навіть між вимірами одного дослідника, що були проведені через певний час. Найкращим методом порівняння серійних змін в кількісних вимірах є сумісне виведення серійних знімків на екрані з виконанням одних і тих самих вимірів на двох суміжних зображеннях [5]. Важливо також відмітити, що більшість вимірів, наведених в цій статті, були отримані в звичайному В-режимі, оскільки нормативні величини при використанні «гармоніки» до сьогодні не були встановлені.
Використання контрастування лівих відділів серця для більш чіткої візуалізації ендокардіальних границь є дуже корисним, тому що суттєво поліпшує відтворюваність результатів вимірів при субоптимальній візуалізації та підвищує кореляцію ЕхоКГ з іншими методами візуалізації. Хоча використання ехо-контрастів детально описано в літературі [6], слід зауважити певні нюанси їх використання. Слід зменшувати механічний індекс для зниження акустичної сили ультразвукового променя, що дозволяє зменшити руйнування пухирців. Фокус повинен бути виставлений на структурі, що цікавить. Підчас начальної фази проходження пухирців повинно мати місце значне затінення, а найкращі кадри часто отримують через декілька кардіальних циклів від початкового появлення контрасту в ЛШ. Використання контрасту є дуже рекомендованим для визначення меж ендокарду у випадках, коли адекватно візуалізується менше, ніж 80% границь ендокарду [7]. При поліпшенні візуалізації верхівки зменшується проблема штучного укорочення ЛШ, та зростає кореляція ЕхоКГ з іншими методиками візуалізації. Підсилення зображення контрастом слід підкреслити особливо з тієї точки зору, що в Україні реєстрація ехо-контрастних агентів очікується найближчим часом, а попит на їх використання має бути достатньо високим.
Проведення кількісної оцінки порожнин серця підчас через стравохідної ЕхоКГ (ЧСЕхоКГ) у порівнянні з трансторакальною ЕхоКГ (ТТЕхоКГ) має свої переваги і недоліки. Хоча ЧСЕхоКГ дозволяє значно оптимізувати візуалізацію багатьох кардіальних структур, між ЧСЕхоКГ та ТТЕхоКГ були виявлені деякі розбіжності при проведенні вимірів. Ця різниця перш за все завдячуює неможливості отримати стандартні позиції, що використовують для проведення кількісних вимірів порожнин, при ЧСЕхоКГ так, як їх використовують при ТТЕхоКГ [8, 9]. Рекомендації зазначених вище робочих груп полягають у том, що застосовані нормальні межі значень для вимірів порожнин та об’ємів використовуються як у ТТЕхоКГ, так і у ЧСЕхоКГ, а рекомендації щодо кількісної оцінки підчас ЧСЕхоКГ переважно фокусуються на виведенні зображень, що дозволяють вимірювання кардіальних структур у доступах, аналогічних таким при ТТЕхоКГ.
Крім описання будь-якого параметра, як нормального чи аномального в кількісному вираженні відповідно до реферативних величин, ехокардіографісти частіше визначають ступінь відхилення від норми таким термінами як «легке» чи «незначне», «помірне», та «значне» чи «важке» відхилення від норми. Таке описання дозволяє клініцисту не тільки зрозуміти, що вимір є відхиленим від норми, але й визначити ступінь до якого виміри пацієнта відрізняються від норми. Окрім надання референтних нормальних значень також корисною була б стандартизація ступенів відхилень від референтних значень в усіх кабінетах ЕхоКГ, так щоб, наприклад, термін «помірне» відхилення однаково розумівся усіма спеціалістами. Втім, для визначення граничних значень існує багато статистичних методик, кожна з яких має значні обмеження [10].
Перший підхід полягає в емпіричному визначенні граничних значень для легкого, помірного та важкого чи вираженого відхилення від норми на основі наявного стандартного відхилення (SD) вище чи нижче граничного нормального значення у коридорі, що існує для здорових людей. Перевагою цього підходу є те, що ці данні вже існують для більшості ехокардіографічних параметрів. Втім, цей підхід має ряд недоліків. По-перше, не всі ехокардіографічні параметри нормально розподіляються (або по гауссіані) в природі, що робить застосування SD сумнівним. По-друге, навіть якщо певний параметр нормально розподіляється у контрольних суб’єктів, більшість ехокардіографічних показників, вимірюваних в загальній популяції, мають значну асиметричність розподілення в одному напрямку (аномально великі для розміру або аномально низькі для показників функції). Використання SD, отриманого на здорових людях, призводить до аномально низьких граничних значень, які не співпадають з клінічним досвідом, оскільки SD неадекватно представляє асиметричність (або розмах величин) у напрямку аномалії. У якості приклада можна навести фундаментальний показник фракції викиду (ФВ) ЛШ, коли при використанні чотирьох SD нижче середнього значення (64±6,5%) ми отримуємо верхню межу для важкого зниження 38%.
Альтернативним методом може бути визначення аномальних параметрів на основі процентних значень (напр., 95%, 99%) або значень, отриманих зі змішаної популяції здорових та хворих людей [11]. Хоча ці дані можуть теж не розподілятися по гауссіані, вони б враховували асиметричне розподілення, що спостерігається в загальній популяції. Головне обмеження цього підходу полягає у тому, що дані з достатньо великої популяції просто не є доступними для більшості ехокардіографічних показників.
В ідеалі найбільш привабливим є підхід, що міг би передбачати певні клінічні виходи чи прогноз. А саме, визначення помірного відхилення показника від норми означало би помірний ризик щодо певного клінічного виходу для пацієнта. Хоча існує досить велика база даних, що пов’язують ризики для пацієнтів з розмірами камер серця (напр., ФВ, розміри ЛШ, об’єм лівого передсердя (ЛП)), для багатьох інших параметрів це зв'язок досі не визначений. На жаль, цей підхід теж нараховує декілька обмежень застосування. Перше обмеження полягає у тому, як найкраще визначати ризик. Пропоновані граничні значення для одного параметра можуть значно відрізнятися для визначення ризику смертності, інфаркту міокарда (ІМ) чи фібриляції передсердь. Крім того, більшість доступних літературних даних стосуються специфічних популяції (напр., постінфарктних чи літніх пацієнтів). Нарешті, хоча наявність даних, що були б специфічно пов’язані з ризиками, представляється ідеальною, все ж не зовсім ясно, чи це необхідно. Скоріш за все, кардіальні ризики прогресивно збільшуються паралельно тому, як ехокардіографічні параметри стають більш аномальними. Це було показано для ряду ехокардіографічних параметрів (діаметр ЛП, товщина стінок, розмір ЛШ, маса ЛШ), які, при перенесенні на загальну популяцію, демонстрували чіткий поступовий взаємозв’язок з ризиком, який, втім, часто був нелінійним [11].
Нарешті, граничні значення повинні визначатися із залученням експертної думки. Хоча цей метод не є суворо науковим, він враховує колективний досвід вивчених і зроблених десятків тисяч ехокардіографічних досліджень.
Таким чином, для всіх існуючих параметрів не можна застосувати якусь єдину методологію. Звичайно, перелік граничних значень представляє собою консенсус експертів за типом «круглого стола», що використовував комбінацію вище описаних методів (Таб. 2.). Консенсусні значення є більш певними для одних параметрів порівняно з іншими, тому майбутні дослідження можуть перемінити граничні значення для певних параметрів. Не зважаючи на зазначені обмеження, існуючі значення параметрів демонструють суттєвий рух до стандартизації у клінічній ехокардіографії.
Таб. 2. Методи, що використовуються для визначення граничних величин різних ехокардіографічних параметрів.
|
|
SD
|
Відсотковий метод
|
Ризик
|
Експертна думка
|
|
Товщина МШП
|
+
|
|
|
+
|
|
Маса міокарду ЛШ
|
+
|
|
+
|
|
|
Розміри ЛШ
|
+
|
|
+
|
|
|
Об’єми ЛШ
|
+
|
|
|
|
|
Функція ЛШ, лінійний метод
|
+
|
|
|
|
|
Фракція викиду
|
|
|
+
|
+
|
|
Розміри ПШ
|
+
|
|
|
|
|
Діаметр ЛА
|
+
|
|
|
|
|
Площина ПШ
|
+
|
|
|
|
|
Функція ПШ
|
+
|
|
|
|
|
Розміри ЛП
|
+
|
|
|
|
|
Об'єми ЛП
|
+
|
|
+
|
+
|
|
Розміри ПП
|
+
|
|
|
|
* ЛА – легенева артерія, ЛП – ліве передсердя, ЛШ – лівий шлуночок, МШП – міжшлуночкова перегородка, ПП – праве передсердя, ПШ – правий шлуночок.
Кількісні виміри ЛШ
Розміри, об’єми та товщина стінок ЛШ – широко використовувані в клінічній практиці та наукових дослідженнях виміри [12,13]. Але до сьогодні розмір та скоротлива здатність ЛШ часто визначається візуально. Втім, якісна оцінка розміру та функції ЛШ може мати суттєву варіабельність між дослідниками, та суттєво залежить від досвіду виконавця. Тому її треба регулярно порівнювати з кількісними вимірами, особливо коли різні доступи та зрізи якісно пропонують різні ступені дисфункції ЛШ. З іншого боку, важливо перевіряти кількісні результати візуальним якісним контролем для запобігання переоцінки результатів процес-залежних вимірів, які часом залежать від якості зображення та структур, що візуалізуються на статичній картинці. На сьогодні визнаним є оцінка розмірів, маси та функції ЛШ в 2-мірній (2D чи В-режим) ЕхоКГ [14-17].
Є певні чіткі переваги та недоліки кожної з загально прийнятих кількісних методик (Таб. 3). Наприклад, лінійні виміри ЛШ, що широко визнані у лікуванні клапанних вад серця, можуть призводити до невірної інтерпретації дилатації чи дисфункції ЛШ у пацієнтів з регіональними порушеннями скоротливості в результаті ішемічної хвороби серця (ІХС). Таким чином, ехокардіографісти повинні бути знайомими та вміти використовувати всі відомі методики, адекватно до конкретного клінічного випадку.
Загальні принципи лінійних та волюмометрічних вимірювань ЛШ
Для отримання акуратного лінійного виміру товщини міжшлуночкової перегородки (МШП), товщини задньої стінки ЛШ (ЗСЛШ) та внутрішніх розмірів ЛШ, запис зображення треба провести з парастернальної позиції по довгій вісі ЛШ. Рекомендується, щоб внутрішні розміри ЛШ (КДР та КСР, відповідно) та товщина стінок вимірювалися у поперечній вісі ЛШ на рівні кінців стулок мітрального клапану. Ці лінійні виміри можуть проводитися безпосередньо в В-режимі, чи в М-режимі під В-режим-контролем.
Завдяки високій частоті оновлення кадру, запис в М-режимі має чудове часове розрішення, та може дати додаткову до В-режиму інформацію щодо розрізнення структур, таких як трабекули, що контактують з задньою стінкою, несправжні хорди з лівої сторони МШП, апарат трикуспідального клапану, чи модераторний пучок ПШ, що контактує з МШП з правого боку. Втім, треба пам’ятати, що навіть під контролем В-режиму, в М-режимі може бути неможливо виставити напрям променя перпендикулярно довгій вісі ЛШ, що є необхідним для отримання справжньої поперечної вісі ЛШ, в якій проводяться виміри. В такому випадку альтернативою може бути виведення та вимірювання розмірів камери ЛШ та товщини його стінок в парастернальній позиції по короткій вісі ЛШ безпосередньо в В-режимі чи в М-режимі під В-режим-контролем, коли курсор може напевно бути позиціонованим перпендикулярно МШП та ЗСЛШ.
Таб. 3. Методики кількісної оцінки лівого шлуночка: використання, переваги та обмеження.
|
Розміри / об’єми
|
Використання / переваги
|
Обмеження
|
|
Лінійні виміри
|
|
|
|
М-режим
|
- Відтворюваність
- Висока частота оновлення кадру
- Багато накопичених даних
- Найбільш репрезентативно при нормальній моделі ЛШ
|
- Рідко вдається досягнути перпендикулярності променя до довгої осі шлуночка
- Одне вимірювання може бути не репрезентативним при вираженій дилатації шлуночка
|
|
В-режим
|
- Забезпечує орієнтацію виміру перпендикуляро до довгої осі шлуночка
|
- Нижча частота оновлення кадру порівняно з М-режимом
|
|
Волюмометричні методи
|
|
|
|
Біплановий за Симпсоном
|
- Враховує локальні порушення контуру ендокарда
- Мінімізує вплив математичного припущення (формули)
|
- Часто зрізується верхівка
- Випадіння ехо-сигналів ендокарду
- Виміри тільки з двох площин
- Мало даних, накопичених зі здорової популяції
|
|
Площа-довжина
|
- Частково враховує локальні порушення контуру ендокарда
|
- Оснований на математичному припущенні (формулі)
- Мало накопичених даних
|
|
Масса
|
|
|
|
М- чи В-режим
|
- Багато накопичених даних
|
- Не є точним при порушеннях сегментарної скоротливості
- Неперпендикулярна орієнтація променя в М-режимі
- Маленька помилка виміру возводиться в куб (особливість формули)
- Переоцінка маси ЛШ
|
|
Площа-довжина
|
- Враховує вклад папілярних м'язів
|
- Нечутливий до порушень моделі ЛШ
|
|
Усічений еліпсоїд
|
- Більш чутливий до порушень моделі ЛШ
|
- Оснований на ряді математичних припущень (формул)
- Мінімум накопичених даних зі здорової популяції
|
Також запропонований метод у В-режимі, особливо корисний при дослідженні хворих з ІХС. При використанні цього методу рекомендується, щоб внутрішні розміри ЛШ (КДР та КСР, відповідно) та товщина стінок вимірювались на рівні поперечника ЛШ на рівні хорд мітрального клапану. Ці лінійні виміри також можуть бути виконані безпосередньо в В-режимі чи під його контролем в М-режимі. Пряме вимірювання в В-режимі на рівні хорд пересікає МШП нижче виносного тракту ЛШ (ВТЛШ) [2,5,18] і, таким чином, забезпечує загальну оцінку ЛШ, що скорочується симетрично, та дозволяє оцінити регіональну функцію базального відділу ЛШ при наявності порушень регіональної скоротливості.
Прямі поперечні розміри в В-режимі менші за такі у М-режимі з верхніми межами КДР ЛШ 5,2 та 5,5 см відповідно та нижніми межами фракційного скорочення (ФС) ЛШ 0,18 та 0,25, відповідно. Нормальні діастолічні та диастолічні виміри для КДР та КСР ЛШ скаладають, відповідно, 4,7±0,4 та 3,3±0,5 см [2,18].
Поперечні розміри ЛШ, товщина МШП та ЗСЛЖ вимірюються в кінці діастоли та систоли в В- чи М-режимі [1,2], бажано в декількох кардіальних циклах [1,2] (Рис. 1). Технічні удосконалення в обробці зображення дозволили поліпшити розрішення кардіальних структур. Тому сьогодні можливо вимірювати безпосередню товщину міжшлуночкової перегородки та інші виміри камер та структур, що визначається, як справжній кордон між тканиною та кров’ю, а не відстань між крайовими ехо-сигналами, як рекомендувалося раніше [5]. Використання лінійних вимірів в В-режимі дозволяє подолати звичайну проблему неперпендикулярних косих вимірів поперечних розмірів структур та камер в М-режимі, що призводять до переоцінки величин розмірів порожнин та товщини стінок.
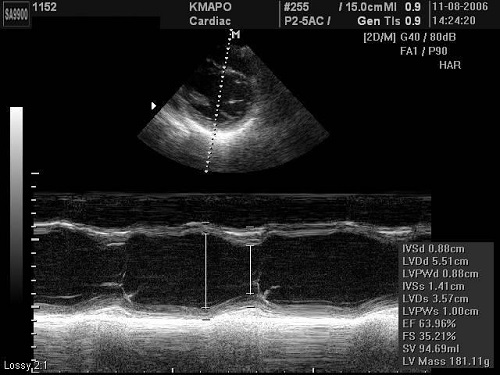
Рис. 1. Вимір кінцево-діастолічного (КДР) – великий розмір, та кінцево-систолічного (КСР) – маленький розмір – діаметрів ЛШ в М-режимі під контролем В-режиму в парастернальному доступі по короткій вісі ЛШ для оптимізації медіально-латерального позиціонування курсору променя.
Для отримання волюмометрічних вимірів до найбільш важливих доступів при кількісних вимірах в В-режимі відносяться парастернальний доступ по короткій вісі ЛШ на рівні папілярних м’язів та апікальні 4- та 2-камерні доступи. Волюмометрічні виміри потребують ручного обведення ендокардіальних меж. При цьому при розрахунку маси міокарда ЛШ папілярні м’язи слід виключати (Рис. 6). Точні виміри потребують оптимальної візуалізації границі ендокарду для мінімізації потреби у екстраполяції. Рекомендується, щоб базальна межа площини порожнини ЛШ проводилася прямою лінією, що поєднує латеральну та септальну межі мітрального кільця в апікальній 4-камерній, та передню та нижню межі мітрального кільця в апікальній 2-камерній позиціях.
Кінець діастоли може бути визначений, як початок комплексу QRS, але краще його визначати як проміжок часу безпосередньо після закриття мітрального клапану або проміжок кардіального циклу, коли розмір порожнини ЛШ є найбільшим. При синусовому ритмі це відповідає моменту безпосередньо після систоли передсердь. Кінець систоли краще визначити як проміжок кардіального циклу перед розкриттям мітрального клапану або коли розмір ЛШ є найменшим. В апікальній 2-камерній позиції рух мітрального клапана не завжди чітко візуалізуються, тому кінцево-діастолічний та кінцево-систолічний об’єми, відповідно, як найбільший та найменший.
При виконанні ЧСЕхоКГ рекомендованими для вимірів порожнини ЛШ є середньо-стравохідний (Рис. 2) та трансгастральний (Рис. 3) 2-камерні зрізи. Діаметри ЛШ вимірюються від краю ендокарду передньої стінки до краю ендокарду нижньої стінки перпендикулярно довгій вісі шлуночка на межі базальної та середньої треті ЛШ. Рекомендованим доступом для вимірювання товщини стінок ЛШ при ЧСЕхоКГ є трансгастральна позиція по короткій вісі ЛШ (Рис. 4). При ЧСЕхКГ величина довгої вісі в середньо-стравохідній 4-камерній позиції та позиції по довгій вісі часто занижується, тому для вимірів рекомендовано використовувати 2-камерну позицію. Треба намагатися запобігати вкорочення довгої вісі ЛШ в черезстравохідних позиціях, записуючи зрізи, що показують найбільший розмір камери, знаходячи кут для виміру діаметрів камери, перпендикулярний довгій вісі камери, а не вимірювати максимальний діаметр по короткій вісі.
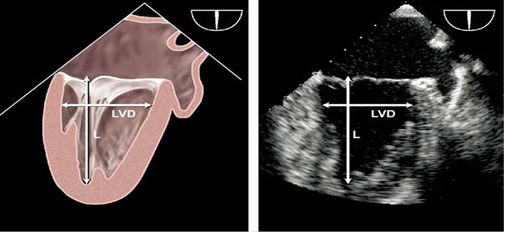
Рис. 2. Черезстравохідні виміри довжини (L) та поперечного діаметру (LVD) ЛШ з середньо-стравохідної 2-камерної позиції, що звичайно найкраще візуалізується під кутами від 60 до 900 [1].
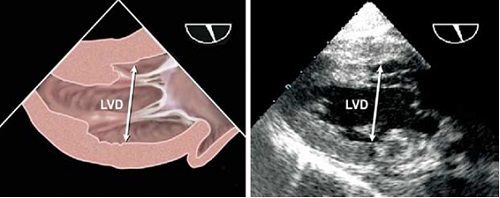
Рис. 3. Черезстравохідні виміри поперечного діаметру (LVD) ЛШ з трансгастральної 2-камерної позиції ЛШ, що найкраще візуалізується під кутом приблизно 90-1100 після оптимізації максимального розміру ЛШ, що візуалізується, шляхом медіально-латеральної ротації [1].
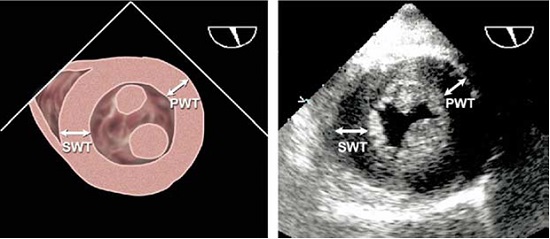
Рис. 4. Черезстравохідні виміри товщини стінок ЛШ – МШП та ЗС з трансгастрального доступу по короткій вісі ЛШ на рівні папілярних м'язів, що звичайно найкраще візуалізується під кутом від 0 до 300 [1].
Розрахунок маси міокарда ЛШ
В клінічній практиці розміри камери ЛШ часто використовуються для розрахунку показників систолічної функції ЛШ, у той час як в епідеміологічних дослідженнях та клінічних випробуваннях єдиним великим застосуванням ЕхоКГ був розрахунок маси міокарду (ММ) ЛШ та її зміни підчас антигіпертензивної терапії [13,19]. Всі алгоритми розрахунку маси ЛШ за використанням М-, чи В-режиму, чи трьохвимірної ЕхоКГ, базуються на вирахуванні об’єму порожнини ЛЖ з об’єму, що обмежує епікард для визначення об’єму міокарда ЛШ. Цей об’єм після цього конвертується в масу шляхом множення на щільність міокарду. Таким чином, кількісний розрахунок маси ЛШ потребує акуратної ідентифікації поверхні між порожниною та ендокардом, а також між епікардом та перикардом.
Сьогодні більшість розрахунків маси ЛШ виконується із застосуванням лінійних вимірів в М-режимі під В-режим-контролем, чи, більш часто останнім часом в В-режимі [20]. Формула для розрахунку маси ЛШ виходячи з лінійних розмірів, що рекомендована Американським товариством з ехокардіографії (ASE) (кореляція з даними аутопсії r=0,90, p<0,001 [21]), основана на моделі ЛШ як витягнутого еліпса:
ММ ЛШ = 0,8 х {1,04[(КДР + ЗСд + МШПд)3 – КДР3]} + 0,6 г,
де ЗСд та МШПд – кінцево-систолічна товщина задньої стінки ЛШ та міжшлуночкової перегородки, відповідно, КДР – кінцево-діастолічний розмір ЛШ. Ця формула є адекватною для застосування у пацієнтів без значних порушень геометрії ЛШ (напр., у хворих з гіпертензіжю). Оскільки формула потребує возведення первинних вимірів в куб, навіть найменша помилка вимірів також возводиться в куб. Підрахунок відносної товщини стінок (ВТС) ЛШ по формулі (2 х ЗСд) / КДР дозволяє розрізняти збільшення маси ЛШ на концентричну (ВТС ЛШ ≥0,42) та ексцентричну (ВТС ЛШ ≤0,42) гіпертрофію, а також дозволяє виділити концентричне ремоделювання ЛШ (нормальна ММ ЛШ при збільшенні ВТС ЛШ ≥0,42) (Рис. 5) [22].
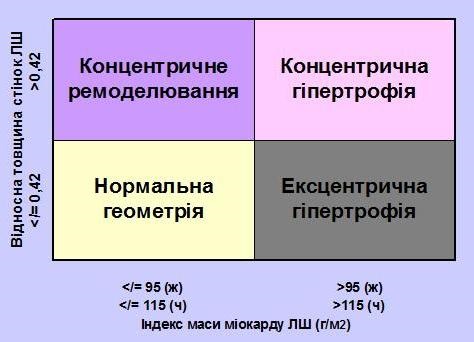
Рис. 5. Порівняння відносної товщини ЛШ (ВТС ЛШ). Пацієнти з нормальною ММ ЛШ можуть мати концентричне ремоделювання (нормальна ММ ЛШ при збільшенні ВТС ЛШ ≥0,42) чи нормальну геометрію (ВТС ЛШ ≤0,42) при нормальній ММ ЛШ. Пацієнти зі збільшеною ММ ЛШ можуть мати концентричну (ВТС ЛШ ≥0,42) чи ексцентричну (ВТС ЛШ ≤0,42) гіпертрофію. Ці визначення ММ ЛШ базуються на лінійних вимірах [22].
Найбільш часто використовані методи визначення маси міокарда ЛШ в В-режимі базуються на формулі «площа-довжина» та моделі усіченого еліпса, як детально описано в рекомендаціях ASE з кількісної оцінки ЛШ 1989 р. [2]. Обидва методи були доведені на початку 1980-х рр. на тваринних моделях та порівнянні результатів преморбідних ехограм з визначенням маси ЛШ при автопсіях. Обидва методи засновані на визначенні міокардіальної площі на рівні середини папілярних м'язів в позиції по короткій вісі. Епікард обводиться для отримання загальної площі (А1), а ендокард обводиться для визначення площі порожнини (А2). Площа міокарда (Аm) розраховується як їх різниця: Аm=А1 – А2. Після цього розраховується радіус b=√A2/π, та середня товщина стінок ЛШ (Рис. 6). Маса міокарда ЛШ може бути розрахована по одній з формул, наведених на Рис. 6. При наявності значних порушень регіональної скоротливості (напр., ІМ), може використовуватися біплановий метод Симпсона, хоча цей метод залежить від адекватного визначення меж ендокарду та епікарду ЛШ, що часто є досить складним в цій позиції. Більшість лабораторій отримують ці виміри в кінці діастоли, виключаючи папілярні м’язи при обведенні міокардіальної площі.
Черезстравохідна оцінка маси ЛШ також є високо точною, але з невеликими систематичними розбіжностями при визначенні товщини ЗС ЛШ. Зокрема, маса міокарда, визначена за товщиною стінок ЛШ підчас ЧСЕхоКГ в середньому буває вища на 6 г/м2.
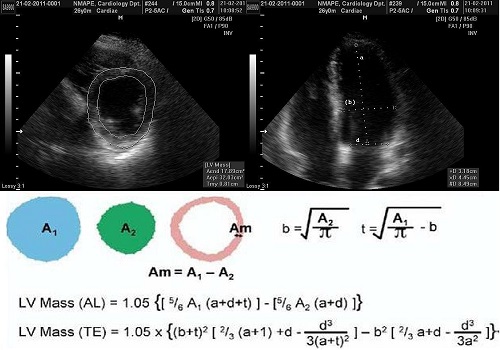
Рис. 6. Два методи для визначення маси ЛШ за формулами «площа-довжина» (AL) та усіченого еліпсоїду (TE) з парастернального доступу по короткій вісі ЛШ та апікальної 4-камерної позиції в В-режимі. А1 = загальна площа ЛШ; А2 = площа порожнини ЛШ; Аm = площа міокарду; а – відрізок довгої вісі від найбільшого поперечного розміру ЛШ до верхівки; b – радіус короткої вісі; d – відрізок довгої вісі від найбільшого поперечного розміру ЛШ до площини мітрального кільця. Радіус (b) та середня товщина стінок (t) розраховуються по площам епікардіальній та порожнини ЛШ в парастернальний позиції по короткій вісі ЛШ (LV mass = маса міокарду ЛШ).
Систолічна функція ЛШ: лінійні та волюмометричні виміри.
Багато ехокардіографічних лабораторій покладаються на виміри в М- чи В-режимі для визначень кількісних параметрів. Лінійні виміри в М- чи В-режимі довели свою відтворюваність з доволі низькою варіабельністю при вимірах одним чи декількома дослідниками [20,23-26]. Хоча лінійні виміри функції ЛШ не є достовірними при наявності виражених регіональних порушень сегментарної скоротливості, у пацієнтів з неускладненою гіпертензією, ожирінням, чи клапанною патологією такі порушення регіональної скоротливості є рідкими за умов відсутності клінічно визнаного ІМ. Таким чином, ФС та його взаємозв’язок з кінцево-систолічним напруженням часто дає корисну інформацію в клінічних дослідженнях [27]. Методи Тейхольца чи Квінонса, що використовувались раніше для розрахунку ФВ ЛШ з лінійних розмірів ЛШ, можуть призводити до неточних вимірювань в результаті наявних порушень геометрії ЛШ, тому що ФВ ЛШ, отримана з лінійних розмірів є проекцією лінійних розмірів на трьох-вимірну структуру [28,29]. Відповідно, використання лінійних вимірів для розрахунку ФВ ЛШ не рекомендовано у клінічній практиці.
Скорочення м’язових волокон в середньому шарі стінки ЛШ може краще відображати внутрішню скоротливість, ніж скорочення субендокардіального шару міокарда. Розрахунок ФС саме середнього, а не субендокардіального, шару міокарда є особливо корисним в виявленні систолічної дисфункції в умовах концентричної гіпертрофії [30]. ФС середнього шару (ФС СШ) може бути розраховано з лінійних вимірів диастолічного та систолічного розміру порожнини ЛШ та товщини стінок ЛШ на основі математичних моделей [30,31] за наступними формулами:
Внутрішня оболонка = [(КДР + МШПд / 2 + ЗСЛШд / 2)3 – КДР3 + КСР3]1,3 – КДР
ФС СШ = ([КДР - МШПд / 2 + ЗСЛШд / 2] – [КСР + внутрішня оболонка]) / (КДР - МШПд / 2 + ЗСЛШд / 2) х 100%
Найбільш часто використованим вимірів об’ємів ЛШ в В-режимі є біплановий метод дисків (модифікована формула Симпсона). Сьогодні цей метод є рекомендованим методом вибору при визначенні об’ємів ЛШ згідно з консенсусом комітету експертів (Рис. 7). Принцип, що лежить в основі цього методу, полягає в тому, що загальний об’єм ЛШ розраховується з сумації об’ємів еліптоїдних дисків. Висота кожного диску розраховується як фракція (звичайно 1/20) довгої вісі ЛШ в 2- та 4-камерних апікальних позиціях. Поперечна площа диску базується на двох діаметрах, розрахованих в 2- та 4-камерній взаємно перпендикулярних позиціях. Коли не можна вивести адекватно дві ортогональні позиції, можливо використання однієї позиції, і тоді диск вважається правильно круглим, а його площина розраховується по одному діаметру. Але наявність порушень регіональної скоротливості є великим обмеженням при використанні однієї площини замість двох ортогональних.
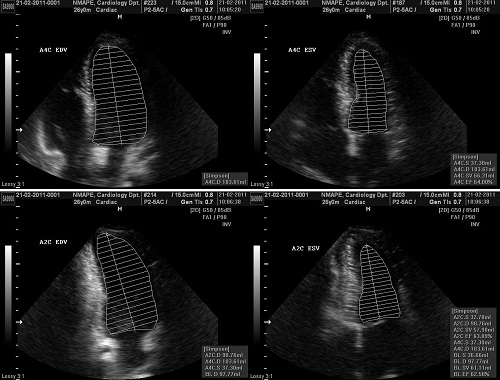
Рис. 7. Двохмірні виміри для розрахунку об’ємів за біплановим методом дисків (модифікована формула Симпсона) в апікальній 4-камерній (А4С) та апікальній 2-камерній (А2С) позиціях наприкінці діастоли (КДР ЛШ) та систоли (КСР ЛШ). Папілярні м’язи мають бути викреслені підчас обведення меж ендокарду.
Альтернативним методом розрахунку об’ємів ЛШ, коли неможливо чітко визначити межі апікального ендокарду, є метод, що базується на перепущені, що ЛШ має форму кулі – метод «площа-довжина». Методом планіметрії розраховується площа порожнини ЛШ в мезовертрикулярному відділі в парастернальній позиції по короткій вісі ЛШ на рівні папілярних м'язів, після чого вимірюється довжина ЛШ від середньої точки мітрального кільця до верхівки ЛШ в апікальній 4-камерній позиції. Ці виміри проводяться наприкінці діастоли та систоли, а об’єми розраховуються по формулі: Об’єм = [5 х площа х довжина] / 6. Для індексації об’ємів найчастіше використовують площу поверхні тіла (ППТ), що вимірюється у метрах квадратних.
ФВ розраховується з розрахованих вищеописаними методами кінцево-діастолічного (КДО) та кінцево-систолічного об’ємів (КСО) за формулою:
Фракція викиду = (КДО – КСО) / КДО.
Значення для градації зниженої систолічної функції ЛШ, наведені в Таб. 6, наводять конвенційну практику використання тих самих граничних значень для жінок та чоловіків. Втім, накопичення даних ЕхоКГ та магнітного резонансу (МРТ) свідчать, що ФВ ЛШ та інші показники у здорових жінок є дещо вищими, ніж у чоловіків [32,33]. Кількісна оцінка об’ємів ЛШ з використанням ЧСЕхоКГ ускладнена важкістю виведення нескорочених зрізів порожнини ЛШ з стравохідних доступів. Втім, при ретельному виконанні, дані прямого порівняння об’ємів та ФВ ЛШ за даними ЧСЕхоКГ та ТТЕхоКГ не демонструють достовірних відмінностей, або ці відмінності мінімальні [8,9].
Реферативні значення для вимірів ЛШ.
Як показано на Таб. 4-6, реферативні значення для лінійних вимірів ЛШ, що були отримані від етнічно гетерогенної популяції з 510 дорослих нормотензивних індивідів без зайвої ваги та без цукрового діабету білої, негроїдної та монголоїдної (Американські індіанці) рас без доведеної серцево-судинної патології. Раніше були наведені детальні описання використаної популяції [20,34-36]. Реферативні дані волюмометрічних вимірів також були отримані з дорослої здорової популяції [37].
Нормальні значення для ММ ЛШ є різними для чоловіків та жінок при їх індексації до ППТ (Таб. 4). Найкращій метод для нормалізації вимірів ММ ЛШ у дорослих є досі предметом дискусії. Хоча ППТ найчастіше використовується в клінічних дослідженнях, цей метод все ж таки недооцінює розповсюдженість гіпертрофії ЛШ у пацієнтів з надлишковою масою тіла та ожирінням. Здатність виявляти гіпертрофію ЛШ, пов’язану з ожирінням та серцево-судинними захворюваннями, підвищується індексацією ММ ЛШ за рахунок її взаємозв’язку з ростом людини [2,7]. До сьогодні наявні дані не дають відповіді, чи може така індексація ММ ЛШ покращити чи погіршити предиктивні дані щодо серцево-судинних подій. Слід замітити, що реферативні межі для маси ЛШ в Таб. 4 є нижчими, ніж ті, що були раніше опубліковані в деяких попередніх ехокардіографічних дослідженнях, але є майже ідентичними тим даним, що були отримані підчас автопсій, а також до реферативних значень, що використовувались у клінічних дослідженнях [19,20,36,38,39]. Хоча в деяких попередніх дослідженнях отримані дані пропонували певні расові розбіжності в вимірах ММ ЛШ, консенсусна доступна література вказує, що між клінічно здоровими суб’єктами білої та негроїдної рас немає достовірної різниці. Але дані недавніх досліджень показали наявність раса-залежної різниці в ремоделюванні ЛШ у дорослих хворих з гіпертензією [40]. Хоча чутливість, специфічність та предикативна цінність вимірів товщини стінок ЛШ для виявлення гіпертрофії ЛШ є нижчою порівняно з розрахунком ММ ЛШ, часто це самий легкий спосіб в клінічній практиці ідентифікувати гіпертрофію ЛШ за допомогою реєстрації потовщення МШП та ЗС ЛШ.
Використання розрахунків маси ЛШ у дітей є ускладненим необхідністю індексації вимірів до розмірів тіла пацієнта. Метою індексації є урахування нормального росту м’язової маси тіла дитини без зневажання патологічних ефектів у пацієнтів надлишковою масою тіла чи ожирінням. Таким чином, індексована ММ ЛШ в ранньому дитинстві може бути порівняна з послідовними вимірами в підлітковому віці та в дорослому віці. Найбільш широко у підлітків та дітей старшого віку використовують розподіл ММ ЛШ на зріст в метрах з возведенням в ступінь 2,5 чи 3,0, тому що цей метод найкраще корелює з індексацією ММ ЛШ до м’язової маси тіла [42]. Сьогодні загально використаним є проміжне значення 2,7 [43,44]. У дітей молодшого віку (до 8 років) найбільш ідеальний метод індексації ще досі – предмет дослідження, хоча найбільш прийнятним сьогодні є зріст в другій ступені [45].
Таб. 4. Референтні значення та градація порушень ММЛШ та геометрії ЛШ.
|
|
Жінки
|
Чоловіки
|
|
Межі норми
|
Легке підвищення
|
Помірне підвищення
|
Важке підвищення
|
Межі норми
|
Легке підви-щення
|
Помірне підвищення
|
Важке підвищення
|
|
Лінійний метод
|
|
|
ММ ЛШ, г
|
67-162
|
163-186
|
187-210
|
≥211
|
88-224
|
225-258
|
259-292
|
≥293
|
|
Індекс ММ ЛШ / ППТ, г/м2
|
43-95
|
96-108
|
109-121
|
≥122
|
49-115
|
116-131
|
132-148
|
≥149
|
|
ММ ЛШ / зріст, г/м
|
41-99
|
100-115
|
116-128
|
≥129
|
52-126
|
127-144
|
145-162
|
≥163
|
|
ММЛШ/ зріст, г/м2,7
|
18-44
|
45-51
|
52-58
|
≥59
|
20-48
|
49-55
|
56-63
|
≥64
|
|
ВТС ЛШ, см
|
0,22-0,42
|
0,43-0,47
|
0,48-0,52
|
≥0,53
|
0,24-0,42
|
0,43-0,46
|
0,47-0,51
|
≥0,52
|
|
Товщина МШП, см
|
0,6-0,9
|
1,0-1,2
|
1,3-1,5
|
≥1,6
|
0,6-1,0
|
1,1-1,3
|
1,4-1,6
|
≥1,7
|
|
Товщина ЗСЛШ, см
|
0,6-0,9
|
1,0-1,2
|
1,3-1,5
|
≥1,6
|
0,6-1,0
|
1,1-1,3
|
1,4-1,6
|
≥1,7
|
|
В-режим
|
|
|
ММ ЛШ, г
|
66-150
|
151-171
|
172-182
|
>193
|
96-200
|
201-227
|
228-254
|
>255
|
|
ММ ЛШ / ППТ, г/м2
|
44-88
|
89-100
|
101-112
|
≥113
|
50-102
|
103-116
|
117-130
|
≥130
|
|
|
|
|
|
|
|
|
|
|
|
ППТ – площа поверхні тіла; ЛШ – лівий шлуночок. Виділено: найбільш доведені та рекомендовані виміри.
Таб. 5. Референтні значення та градація дилатації ЛШ.
|
|
Жінки
|
Чоловіки
|
|
Межі норми
|
Легке підвищен-ня
|
Помірне підви-щення
|
Важке підвищення
|
Межі норми
|
Легке підвищен-ня
|
Помірне підви-щення
|
Важке підви-щення
|
|
Розміри ЛШ
|
|
|
КДР ЛШ
|
3,9-5,3
|
5,4-5,7
|
5,8-6,1
|
≥6,2
|
4,2-5,9
|
6,0-6,3
|
6,4-6,8
|
≥6,9
|
|
Індекс КДР/ППТ, см/м2
|
2,4-3,2
|
3,3-3,4
|
3,5-3,7
|
≥3,8
|
2,2-3,1
|
3,2-3,4
|
3,5-3,6
|
≥3,7
|
|
Індекс КДР/зріст, см/м
|
2,5-3,2
|
3,3-3,4
|
3,5-3,6
|
≥3,7
|
2,4-3,3
|
3,4-3,5
|
3,6-3,7
|
≥3,8
|
|
Об'єм ЛШ
|
|
|
КДО ЛШ, мл
|
56-104
|
105-117
|
118-130
|
≥131
|
67-155
|
156-178
|
179-201
|
≥201
|
|
Індекс КДО / ППТ, мл/м2
|
35-75
|
76-86
|
87-96
|
≥97
|
35-75
|
76-86
|
87-96
|
≥97
|
|
КСО, мл
|
19-49
|
50-59
|
60-69
|
≥70
|
22-58
|
59-70
|
71-82
|
≥83
|
|
Індекс КСО / ППТ, мл/м2
|
12-30
|
31-36
|
37-42
|
≥43
|
12-30
|
31-36
|
37-42
|
≥43
|
ППТ – площа поверхні тіла; ЛШ – лівий шлуночок. Виділено: найбільш доведені та рекомендовані виміри.
Таб. 6. Референтні значення та градація зниження скоротливої функції ЛШ.
|
|
Жінки
|
Чоловіки
|
|
|
Межі норми
|
Легке зни-ження
|
Помірне зни-ження
|
Важке зниження
|
Межі норми
|
Легке зниження
|
По-мірне зни-ження
|
Важке зни-ження
|
|
Лінійний метод
|
|
Фракційне скорочення ендокарду, %
|
27-45
|
22-26
|
17-21
|
≤16
|
25-43
|
20-24
|
15-19
|
≤14
|
|
Фракційне скорочення середнього шару міокарду, %
|
15-23
|
13-14
|
11-12
|
≤10
|
14-22
|
12-13
|
10-11
|
≤10
|
|
В-режим
|
|
Фракція викиду, %
|
≥55
|
45-54
|
30-44
|
<30
|
≥55
|
45-54
|
30-44
|
<30
|
Виділено: найбільш доведені та рекомендовані виміри.
Трьохвимірна оцінка об’ємів та маси.
Трьохвимірний об’єм камери та маса трьохвимірної структури неповно характеризуються одновимірним або двохвимірними підходами, бо базуються на геометричних припущеннях. Хоча в минулому ці неточності вважалися неподоланими та таким, що мають мінімальне клінічне значення, у більшості ситуацій потрібні якомога точні виміри, особливо коли має місце оцінка плину захворювання в динаміці підчас серій дослідження. Протягом останніх п’ятнадцяти років стали доступними декілька трьох-вимірних ехокардіографічних технік, що дозволяють вимірювати об’єми порожнини та ММ ЛШ [46-59]. Їх концептуально можна поділити на техніки, що базуються на реконструкції отриманих підчас дослідження двохмірних зображень, та техніки отримання даних в режимі реального часу матричним датчиком, яка також відома як трьохвимірна ЕхоКГ в режимі реального часу. Після отримання «сирих» даних, розрахунки об’ємів ЛШ та ММ ЛШ потребує визначення меж ендокардіальних поверхонь (а також і епікардіальних меж для розрахунку маси) з використанням ручних та напівавтоматичних алгоритмів. Ці визначені межі потів обробляються для розрахунку об’єму порожнини чи міокарду методом сумації дисків [54,56] чи іншими методами [46-48].
Незалежно від методів отримання зображень чи аналізу, трьохвимірна ЕхоКГ не покладається на геометричні припущення для розрахунку об’ємів/маси, та не має недоліків у вигляді помилок у позиціонуванні площини сканування, що може призвести до штучного укорочення камери ЛШ. Дослідження, що порівнювали результати розрахунків об’ємів та маси ЛШ у порівнянні з іншими «золотими стандартами» (напр., МРТ), підтвердили точність трьохвимірної ЕхоКГ. У порівнянні з МРТ, об’єми ЛШ та ПШ, розраховані за допомогою трьохвимірної ЕхоКГ були достовірно точнішими з меншими розбіжностями та варіабельністю результатів залежно від виконавців дослідження, ніж двохвимірна ЕхоКГ [46,54,57,60]. Також була продемонстрована перевага трьохвимірної ЕКГ у розрахунку ММ ЛШ порівняно з М- та В-режимом [55,57,59]. Об’єм та маса ПШ, розраховані за допомогою трьохвимірної ЕхоКГ, також достовірно корелювали з даними, отриманими за даними МРТ [58,61]. Сучасні обмеження при проведенні трьохвимірної кількісної оцінки, включають необхідність синусового ритму, гірша візуалізація порівняно з В-режимом, та час, необхідний для обробки та аналізу даних. Втім, в майбутньому, вірогідно, що ці обмеження будуть усунуті.
Регіональна функція ЛШ.
В 1989 р. ASE рекомендувало 16-сегментарну модель для оцінки сегментарної скоротливості ЛШ [2]. Ця модель складає по 6 сегментів базального та мезовентрикулярного (серединного) відділів ЛШ та 4 сегментів на рівні верхівки (Рис. 8). Точки прикріплення стінок ПШ до ЛШ визначає межі МШП, яка на базальному та мезовентрикулярному рівнях ділиться на передню та нижню (нижньо-перегородкова) частини. Далі проти часової стрілки, інші сегменти базального та серединного відділів визначаються як нижній, нижньо-латеральний (задній), передньо-латеральний (боковий) та передній. Верхівковий відділ включає септальний, нижній, латеральний (боковий) та передній сегменти. Ця модель сьогодні широко використовується в ехокардіографії. Напроти, в при методах візуалізації з перфузією радіоактивними агентами, магнітному резонансному скануванні та комп’ютерній томографії серця частіше використовують більшу кількість сегментів.
В 2002 р. Робоча група Американської асоціації серця з сегментарної оцінки функції міокарду при різних методах візуалізації серця в рамках спроби встановити стандарти сегментарного ділення ЛШ для всіх засобів візуалізації запропонувала 17-сегментарну модель (Рис. 8) [62]. Ця модель відрізняється від попередньої 16-сегментарної переважно тільки додаванням 17-го сегменту – власно верхівки (ковпачок верхівки). Ковпачок верхівки – це сегмент безпосередньо під закінченням порожнини ЛШ. Вважається, що сучасні засоби поліпшення ехокардіографічного зображення, включаючи «гармоніку» та контрастування, в майбутньому дозволять поліпшити візуалізацію власно апікального сегменту підчас ЕхоКГ. Обидві моделі є досить практичними для клінічного використання, при цьому достатньо детальними для напівкількісного аналізу. 17-сегментарна модель повинна використовуватися підчас досліджень з перфузією міокарда та при будь-яких спробах порівняння різних методик візуалізаціях. 16-сегментарна модель теж є абсолютно придатною для визначення порушень регіональної скоротливості, оскільки ковпачок верхівки (17-й сегмент) є нерухомим.
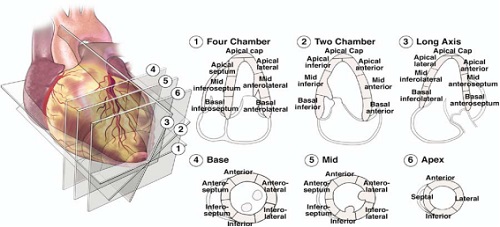
Рис. 8. Сегментарний аналіз стінок ЛШ засновується на схематичних зображеннях парастернальних та апікальних доступів по короткому та довгому зрізам на трьох різних рівнях (базальному, серединному та апікальному). Апікальні сегменти звичайно візуалізуються з апікальних 4-камерної, 2-камерної та 3-камерної позицій. Власно верхівка може бути оцінена тільки підчас дослідження з використанням контрасту. 16-сегментарная модель може використовуватись без урахування оцінки власно верхівки, як описано в рекомендаціях ASE 1989 р. 17-сегментарна модель, що включає власно верхівку (покришку), була запропонована Робочою групою Американської асоціації серця з сегментарної оцінки функції міокарду при різних методах візуалізації серця [62].
Маса та розмір міокарду, що оцінювалися підчас аутопсії, стали основою для визначення відділів та сегментів. При розділенні ЛШ на базальний, мезовентрикулярний (серединний), що обмежений довжиною папілярних м'язів, та апікальний відділи (третини) було визначено, що у дорослих на базальний відділ припадає 43%, на серединний – 36%, та на апікальний відділ – 21% маси міокарда [63]. 16-сегментарна модель наближається до цього співвідношення, створюючи наступний розподіл маси міокарда: 37,% для базальної та серединної третин, та 25% - для апікального відділу. 17-сегментарна модель створює такий розподіл: 35,3%, 35,3 та 29,4% для базального, серединного та апікального відділів (включаючи власно апікальний сегмент), відповідно.
Існує індивідуальна варіабельність кровопостачання сегментів міокарду ЛШ з точки зору басейнів коронарних артерій. Втім, сегменти звичайно відповідають басейнам 3 головних коронарних артерій, розподіл кровопостачання котрими при ТТЕхоКГ показаний на Рис. 9 [62].
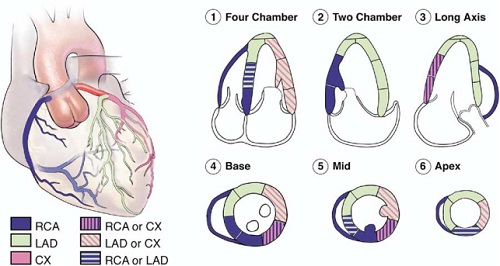
Рис. 9. Типовий розподіл басейнів правої коронарної артерії (RCA = ПКА), передньої міжшлуночкової гілки лівої коронарної артерії (LAD = ПМШГ ЛКА) та огинаючої гілки ЛКА (CX = ОГ ЛКА). Розповсюдження басейнів коронарних артерій може варіювати у різних пацієнтів (деякі сегменти мають варіабельне коронарне кровопостачання з різних артерій) (Four Chamber = A4C; Two Chamber = A2C; Long Axis = апікальная 3-камерна позиція по довгій вісі ЛШ; or - або).
З 1970-х років ЕхоКГ використовується для оцінки регіональної скоротливості стінок ЛШ при інфаркті та ішемії [64-66]. Визнано, що регіональне кровопостачання та регіональна систолічна функція ЛШ є взаємопов’язаними, в тому числі у сенсі залежності типу порушення скоротливості від ступеня порушення коронарного кровотоку [67]. Хоча регіональні порушення скоротливості в стані спокою можуть не реєструватися до перекриття просвіту артерії вище за 85%, при навантаженні навіть коронарний стеноз до 50% звуження просвіту артерії може призводити до регіональної міокардіальної дисфункції. Визнано, що ЕхоКГ може переоцінювати кількість ішемізованого або інфарктного міокарду, оскільки суміжні неішемізовані сегменти можуть бути залучені в зону порушення регіональної скоротливості за рахунок підтягування, зсуву регіонального навантаження чи оглушення міокарда [68]. Таким чином, слід приймати до уваги характер потовщення та руху стінки. Крім того, слід пам’ятати, що порушення регіональної скоротливості можуть виникати також при відсутності атеросклеротичного ураження коронарних артерій (напр., диссинхронія при блокаді лівої ніжки пучка Гіса).
Рекомендовано, щоб кожний сегмент аналізувався окремо, а напівкількісний підрахунок проводився на основі їх рухів та систолічного потовщення. В ідеалі, функція кожного сегменту має бути верифікована з різних множинних доступів. Кількісні еквіваленти функції сегменту наступні: нормо- чи гіперкінез = 1 бал; гіпокінез = 2 бала; акінез (відсутнє потовщення) = 3 бали; дискінез (парадоксальний рух в систолу) = 4 бали, та аневризма (діастолічна деформація) = 5 балів [1]. Індекс локальної скоротливості (ІЛС) розраховується з суми балів усіх сегментів, що вдалося візуалізувати, поділеної на кількість візуалізованих сегментів.
Оцінка ремоделювання ЛШ та використання ЕхоКГ в клінічних дослідженнях.
Ремоделювання ЛШ описує процес, при якому серце змінює свої розміри, геометрію та функцію протягом часу. Кількісна оцінка підчас ТТЕхоКГ в В-режимі дозволяє характеризувати ремоделювання ЛШ, що відбувається як у здорових індивідів, так і при різних серцевих захворюваннях. Ремоделювання ЛШ може бути фізіологічним, коли серце збільшується у розмірі, але функціонує нормально підчас зростання організму, завдяки фізичним тренуванням та підчас вагітності. Деякі дослідження продемонстрували, що як ізометричні, так і ізотонічні фізичні вправи призводять до ремоделювання розмірів порожнин ЛШ та ПШ, та до збільшення товщини стінок [69-73]. Ці зміни у високо тренованих серцях професійних спортсменів прямо пов’язані з типом та тривалістю тренувань, та чітко характеризовані саме ехокардіографічно. При ізометричних вправах відбувається непропорційне збільшення маси ЛШ порівняно зі збільшенням діастолічного об’єму ЛШ, що призводить до значно більшого підвищення відношення товщини стінки до розміри порожнини (співвідношення h/R) порівняно із здоровими індивідами не-спортсменами без суттєвих змін показників глобальної скоротливої функції ЛШ [69-73]. Це фізіологічне гіпертрофічне ремоделювання «спортивного» серця є зворотним при припиненні інтенсивних тренувань, є пов’язаним з загальним збільшенням м’язової маси тіла [70], та запускається підвищеною симпатичною активністю в серці [74]. Ремоделювання може носити компенсаторний характер при хронічному перенавантаженні тиском внаслідок системної гіпертензії або аортального стенозу, що призводить до концентричної гіпертрофії (підвищених масі міокарду та ВТС ЛШ при нормальних розмірах порожнин та збереженій ФВ ЛШ) (Рис. 5). Компенсаторне ремоделювання ЛШ також відбувається при хронічному перевантаженні об’ємом, що асоціюється з мітральною чи аортальною недостатністю, що індукує зміни архітектури шлуночка, що характеризуються як ексцентрична гіпертрофія з дилатацією порожнини ЛШ та на початку нормальною скоротливою функцією. Перевантаження тиском та об’ємом може довго залишатися компенсованим відповідним типом гіпертрофії, що нормалізує напруження стінки таким чином, що гемодинаміка та ФВ ЛШ довгий час залишаються стабільними. Втім, у більшості пацієнтів, якщо хронічне збільшення післянавантаження не може бути нормалізованим вчасно, процеси ремоделювання стають патологічними.
Перехід до патологічного ремоделювання визначається прогресуючою дилатацією шлуночка, розтягненням контурів його порожнини, порушенням нормальної геометрії мітрального кільця та підклапанного апарату, що призводять до мітральної регургітації. Додаткове перевантаження об’ємом за рахунок мітральної регургітації потенціює прогресування зниження систолічної функції та розвиток серцевої недостатності. Дилатація ЛШ провокує розвиток мітральної регургітації, а мітральна регургітації потенціює прогресування подальшої дилатації ЛШ, його ремоделювання та контрактильної дисфункції.
Зміни у розмірах та геометрії ЛШ, що викликаються гіпертензією (Рис. 5), відображують підлеглі гемодинамічні порушення, асоційовані з підвищенням артеріального тиску [22,75]. Ехокардіографічна картина перенавантаження тиском у вигляді концентричної гіпертрофії є типовою для суб’єктів з гіпертензією, та асоціюється з високим систолічним артеріальним тиском та високим периферійним судинним опором. Напроти, ексцентрична гіпертрофія ЛШ асоціюється з нормальним рівнем периферійного опору, але з високим серцевим індексом, відповідним до надлишкового об’єму циркулюючої крові. Концентричне ремоделювання (нормальна маса ЛШ з підвищеною ВТС ЛШ) характеризується з високим периферичним опором, низьким серцевим індексом та підвищеною жорсткістю артеріальної стінки [76,77].
Унікальний різновид ремоделювання відбувається після ІМ як результат різкої втрати частини скоротливих кардіоміоцитів [22,78]. Рання експансія інфарктної зони асоціюється з ранньою дилатацією ЛШ, у той час як підвищення регіонального напруження стінок перерозподіляється на інші стінки для збереження ударного об’єму. Вираженість раннього та пізнього постінфарктного ремоделювання визначається рядом факторів, включаючи розмір та локалізацію інфаркту, симпато-адреналову активацію, ап-регуляцію системи ренін-ангіотензин-альдостерон та секреції натрій-уретичних пептидів. Від однієї треті до половини пацієнтів після ІМ страждають від прогресивної дилатації ЛШ [79,80] з розтягненням порожнини та розширенням геометрії ЛШ та розвитком вторинної мітральної регургітації. Мітральна регургітація ще більше індукує прогресування дисфункції ЛШ та розвиток застійної серцевої недостатності. Патологічне ремоделювання ЛШ є фінальним загальним шляхом до серцевої недостатності незалежно від того, що є першим начальним стимулом до неї – хронічне перенавантаження тиском чи об’ємом, генетично зумовлена кардіоміопатія чи ІМ. Ішемічна хвороба серця є причиною дисфункції ЛШ у приблизно двох третин хворих з серцевою недостатністю [81].
Хоча описане ремоделювання ЛШ у пацієнтів з артеріальною гіпертензією, хронічною клапанною регургітацією та первинними кардіоміопатіями, безпосередньо перехід до клінічно маніфестної серцевої недостатності є менш відомим, оскільки перехід до неї є дуже пролонгованим. На відміну від них, час від ІМ до розвитку серцевої недостатності є значно коротшим та добре задокументованим.
Традиційні кількісні ехокардіографічні виміри, рекомендовані для оцінки ремоделювання ЛШ включають оцінку об’ємів ЛШ в двох чи в одній проекції згідно рекомендацій ASE. Хоча двопланові та однопланові визначення об’ємів не є взаємно замінними, вони всі є однаково чутливими для виявлення час-залежного ремоделювання ЛШ та прогресування скоротливої дисфункції [77]. У багатьох дослідженнях у хворих після гострого інфаркту міокарду чи з серцевою недостатністю було продемонстровано, що об’єми ЛШ та похідна ФВ є пре дикторами небажані серцево-судинні події, включаючи смертність, повторний інфаркт, серцеву недостатність, шлуночкові аритмії та мітральну регургітацію [78-81]. ASE рекомендує використання кількісного визначення об’ємів ЛШ, ФВ ЛШ, маси міокарду ЛШ та його геометрії, як описано в вище наведених відповідних розмірах для визначення відповідного типу ремоделювання ЛШ, викликаного фізіологічними чи патофізіологічними причинами. Крім того, ці виміри забезпечують прогностичну інформацію, що відповідає загальним демографічним даним.
Кількісна оцінка ПШ та виносного тракту ПШ.
Нормальний ПШ представляє собою складну структуру у формі на півмісяця, що огорнута навколо ЛШ, та візуалізується неповністю при будь-якому одиночному зрізі у В-режимі. Тому акуратна оцінка морфології та функції ПШ потребує інтеграції висновків з множинних ехокардіографічних зрізів, включаючи парастернальні доступи по довгій та короткій вісям, зріз приносного тракту ПШ, апікальний 4-камерний та субкостальний доступи. Хоча було описано багато методів кількісної ехокардіографічної оцінки ПШ, в клінічній практиці до сьогодні оцінка структури та функції ПШ залишається здебільш якісною. Втім, достатня кількість недавніх досліджень підкреслює важливість функції ПШ як предиктора багатьох серцево-легеневих захворювань, що наводить на думку, що потрібні більш кількісні критерії для рутинної оцінки ПШ у більшості клінічних обставин.
В нормі ПШ порівняно з ЛШ має значно тонші стінки. Нормальний ПШ є прилаштованим до низького опору малого кола кровообігу і, внаслідок цього, низького пост навантаження. Таким чином, в нормі в ПШ спостерігається порівняно низький тиск, а сам ПШ має високу піддатливість та еластичність. Як наслідок, ПШ є набагато більш чутливим до зростання післянавантаження , а зміни у розмірі та функції ПШ є індикаторами підвищення легеневого судинного опору та вторинного перенавантаження, що передається від перенавантажених лівих відділів. Гостре підвищення післянавантаження у дорослих проявляється дилатацією ПШ, а хронічне – його концентричною гіпертрофією. Крім того, власніа патологія ПШ, така як інфаркт чи дисплазія ПШ [82] можуть викликати дилатацію ПШ чи потовщення його стінки. Таким чином, оцінка розмірів ПШ та товщини його стінок є, по суті, ключем до оцінки його функції.
Вільна стінка ПШ, що в нормі не перевищує по товщині 0,5 см, вимірюється в М- чи В-режимі. Хоча товщина вільної стінки ПШ може бути оцінена в апікальній чи парастернальній позіції по довгій вісі, сьогодні вважається, що саме діастолічна товщина стінки ПШ, виміряна на рівні хорд трикуспідального клапана на висоті зубця R ЕКГ, є більш відтворюваною з меншою варіабельністю та більш тісно корелює з кінцево-систолічним тиском ПШ (Рис. 10) [75]. При цьому треба запобігати переоцінки товщини, що може при вимірюванні бути викликана наявністю епікардіального жиру та значною трабекулярністю ПШ.
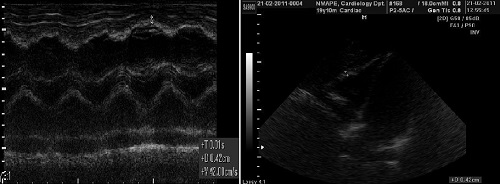
Рис. 10. Методи вимірювання товщини вільної стінки ПШ (стрілки) в М-режимі (зліва) та В-режимі в субкостальній позиції по довгій вісі ЛШ (зправа).
Якісна оцінка розміру ПШ може бути легко виконана з апікальної 4-камерної позиції (Рис. 11). В цій позиції площа та діаметр на рівні середньої треті ПШ мають бути меншими за ЛШ. У випадках помірного збільшення, площа порожнини ПШ стає порівняною за розмірами з ЛШ, та часто приймає участь в формуванні верхівки серця. При прогресуванні дилатації, площа порожнини ПШ починає перебільшувати таку ЛШ, а верхівка формується правим, а не лівим шлуночком.
Кількісну оцінку ПШ також найкраще виконувати в апікальній 4-камерній позиції. При цьому треба намагатися вивести справжній нескорочений вид порожнини ПШ в апікальній 4-камерній позиції для отримання максимального поперечного діаметру ПШ. Простим методом кількісної оцінки розміру ПШ є визначення поперечних діаметрів ПШ на рівні середини та базального відділу ПШ (Рис. 11). Крім того, в цій позиції можна також виміряти повздовжній розмір П. В таб. 7 наведені нормальні розміри ПШ в апікальній 4-камерній позиції. На відміну від попередніх рекомендацій [76,80,83], останні рекомендації ASE з ехокардіографічної оцінки правих відділів серця у дорослих 2010 р. [84] не встановлюють меж легкого, помірного та важкого відхилення правих відділів серця від норми, а наводять лише нормативні значення, пропонуючи всі значення вище верхньої межі норми вважати патологічними.
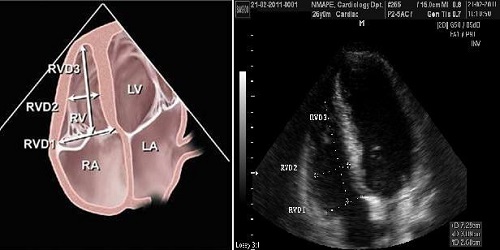
Рис. 11. Визначення поперечних (базального та серединного на рівні папілярних м'язів ЛШ) та повздовжнього розмірів ПШ в апікальній 4-камерній позиції (RVD1 – базальний поперечний розмір ПШ; RVD2 – серединний поперечний розмір ПШ; RVD3 – повздовжній розмір ПШ).
Таб. 7. Референтні значення та граничні значення розмірів ПШ та легеневої артерії.
|
Межі норми
|
|
Розміри ПШ (Рис. 12)
|
|
Базальний діаметр ПШ (ПШ 1), см
|
2,4-4,2
|
|
Серединний діаметр ПШ (ПШ 2), см
|
2,0-3,5
|
|
Повздовжній діаметр ПШ (ПШ 3), см
|
5,6-8,6
|
|
Діаметри ВТПШ (Рис. 13, 14)
|
|
Над АК (ВТПШ 1), см
|
2,1-3,5
|
|
Над КЛА (ВТПШ 2), см
|
1,7-2,7
|
|
Діаметр ЛА
|
|
Під КЛА (ЛА 1), см
|
1,5-2,1
|
ПШ – правий шлуночок; ВТПШ – виносний тракт ПШ; АК – аортальний клапан; ЛА – легенева артерія; КЛА – клапан легеневої артерії.
Таб. 8. Референтні значення та граничні значення розмірів та функції ПЖ в апікальній 4-камерній позиції.
|
|
Межі норми
|
|
Діастолічна площа ПШ, см2
|
10-25
|
|
Систолічна площа ПШ, см2
|
4-14
|
|
Фракційне скорочення площі ПШ, %
|
35-63
|
Крім того, розміри ПШ можуть бути оцінені при ЧСЕхоКГ в середньо стравохідній 4-камерній позиції (Рис. 12). Середньостравохідна 4-камерна позиція, що взагалі відповідає апікальній 4-камерній при ТТЕхоКГ, виводиться з рівня середини ЛП та проходить через верхівку ЛШ з багатоплановим налаштуванням кута сканування таким чином, щоб вивести максимальний діаметр трикуспідального кільця (звичайно між 10 та 200).
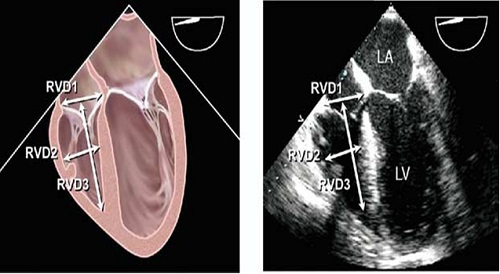
Рис. 12. Черезстравохідні ехокардіографічні виміри діаметрів ПШ з середньо-стравохідної 4-камерної позиції, що найкраще візуалізуються після оптимізації максимального розміру ПШ, що візуалізується в зрізі між 0 та 200 [1].
Систолічна функція ПШ звичайно в клінічній практиці оцінюється якісно. При якісній оцінці слід оцінювати зсув трикуспідального кільця. В систолу трикуспідальне кільце в нормі зсувається в напрямку верхівки на 1,6-3,0 см [84]. Зменшення екскурсії трикуспідального кільця менше 1,5 см асоціюється з погіршенням прогнозу при ряді серцево-судинних захворювань [84, 85]. Хоча існує певна кількість методів для точної кількісної оцінки, точні розрахунки об’ємів ПШ та його ФВ лишається проблемною внаслідок складної геометрії та нестачі стандартних методів визначення об’ємів ПШ. Втім, для оцінки функції ПШ можуть бути використані певні ехокардіографічні методики.
Фракційна зміна площі ПШ, що визначається в апікальній 4-камерній позиції, є простим методом оцінки функції ПШ, що корелює з ФВ ПШ за даними МРТ (r=0,88) та є пов’язаною з прогнозом при ряді захворювань [81, 86]. Нормальні площа та фракційна зміна площі ПШ наведені в таб. 8. Додаткова оцінка систолічної функції ПШ включає застосування тканинної допплерографії для визначення швидкості руху трикуспідального кільця та визначення індексу міокардіальної функції ПШ (індекс Тея) [87].
Виносний тракт ПШ (ВТПШ) пролягає від передньо-верхнього сегменту ПШ до легеневої артерії (ЛА), включаючи клапан ЛА (КЛА). Він найкраще візуалізується при нахилі зрізу з парастернальної позиції по довгій вісі трохи уверх, та у парастернальній позиції по короткій вісі на рівні магістральних судин. Також його можна візуалізувати з субкостальної позиції по довгій та короткій вісі, та в апікальному доступі. Вимірювання ВТПШ є найбільш точним з парастернальної позиції по короткій вісі (Рис. 13) безпосередньо проксимальніше КЛА. Середні значення вимірів ВТПШ наведені в таб. 7, При ЧСЕхоКГ звичайно найкращій вид ВТПШ безпосередньо проксимальніше від КЛА виводиться з середньо-стравохідної позиції виносного та приносного трактів ПШ (Рис. 14).
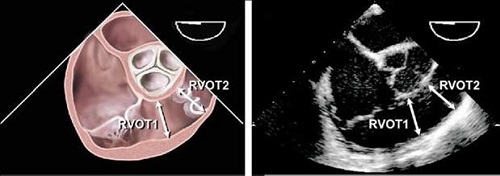
Рис. 13. Вимірювання ВТПШ на субпульмонарному рівні (ВТПШ 1) та рівні кільця КЛА (ВТПШ 2) в середньо-стравохідній позиції по короткій вісі на рівні аортального клапана з використанням мультипланового датчика між приблизно 45 та 700.
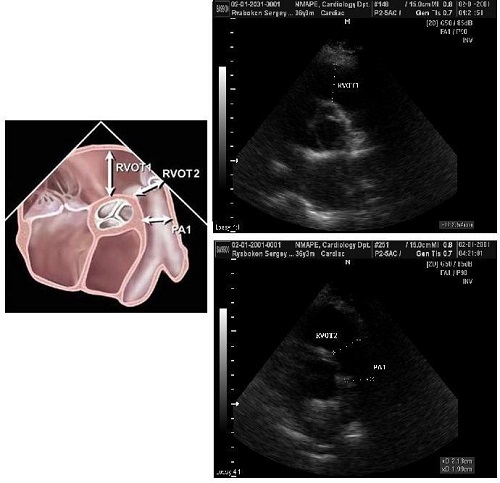
Рис. 14. Вимірювання ВТПШ на рівні кільця КЛА (ВТПШ 2) та головного стовбура ЛА в парастернальній позиції по короткій вісі ЛШ на рівні магістральних судин.
Кількісні виміри лівого та правого передсердь
ЛП виконує 3 головні фізіологічні ролі, що впливають на наповнення та скоротливість ЛШ. ЛП служить у якості скоротливої помпи, що вкладає від 15 до 30% до наповнення ЛШ, є фізіологічним резервуаром, що збирає кров з легеневих вен підчас систоли шлуночка, та є кондуїтом для перетікання накопиченої крові з ЛП до ЛШ підчас ранньої діастоли ЛШ [88]. Підвищення розміру ЛП асоціюється з поганим прогнозом при серцево-судинній патології [89-91]. Збільшення розмірів передсердь звичайно пов’язане з підвищеним напруженням стінки передсердя в результаті підвищення тиску наповнення [92,93]. Хоча підвищення об’ємів наповнення може викликати збільшення розміру ЛП, небажані виходи, що асоціюються зі збільшенням розмірів та об’єму, більш сильно асоціюються зі збільшенням тиску наповнення. Існує взаємозв'язок між збільшеним розміром ЛП та ризиком розвитку фібриляції передсердь, інсульту [94-102], загальної смертності після ІМ [103,104] та ризиком смертності та госпіталізації у хворих з дилатаційною кардіоміопатією [105-109]. Збільшення ЛП є маркером як ступеня важкості, так і хронічного характеру систолічної дисфункції ЛШ та ступеня підвищення тиску у ЛА [89,92,93].
Розмір ЛП вимірюється наприкінці систоли шлуночків, коли камера ЛП має найбільший об’єм. При отриманні зображень для розрахунку об’єму ЛП слід запобігати отримання косих зрізів, щоб не принизити його справжній розмір. Тобто, слід отрииимувати найбільший розмір ЛП з тих, що вдалося візуалізувати, що означає, що площина ультразвукового зрізу проходила через максимальну коротку вісь передсердя. Довжину ЛП також слід максимізувати, удосконалюючись, що зріз пройшов через справжню довгу вісь ЛП. При виконанні планіметрії ЛП слід виключати з об’єму устя легеневих вен та вушко ЛП, якщо вони візуалізуються.
При ЧСЕхоКГ ЛП часто не вміщується повністю у сектор візуалізації. Тому виміри об’єму ЛП підчас ЧСЕхоКГ не є вірогідними, хоча можлива його приблизна оцінка при комбінації вимірів з різних площин візуалізації.
Лінійні виміри ЛП
ЛП може бути візуалізоване з багатьох ехокардіографічних зрізів, в яких можна отримати декілька потенційних кількісних вимірів. Втім, велика кількість попередніх клінічних досліджень віддає перевагу саме передньо-задньому (ПЗ) поперечному розміру ЛП в парастернальній позиції по довгій вісі ЛШ в М- чи В-режимі, як стандарту лінійного розміру ЛП (Рис. 15) [94,96,97,99,105,106]. Конвенційним для виміру в М-режимі є вимірювання від верхнього (переднього) краю задньої стінки кореня аорті до верхнього краю задньої стінки ЛП. Втім, для запобігання помилки за рахунок варіації кількості простору між ЛП та коренем аорті, рекомендовано для встановлення курсору при вимірі використовувати нижній (задній) край кореня аорти.
Хоча ці лінійні виміри показали добру кореляцію з вимірами підчас ангіографічних досліджень та до сьогодні широко використовуються в клінічній практиці та наукових дослідженнях, вони не досить акуратно відбивають істинний розмір ЛП [110,111]. Оцінка розміру ЛП по ПЗ поперечному розміру має на увазі, що між ПЗ поперечним розміром та всіма іншими розмірами зберігається постійний взаємозв’язок по мірі збільшення порожнини ЛП в патології, що дуже часто не є так [112,113]. Збільшення ПЗ поперечного розміру може обмежуватися з боку грудної клітини між грудиною та хребтом, не зважаючи на прогресивне збільшення об’єму ЛП. Переважне розширення ЛП в верхньо-нижньому та медіально-латеральному напрямках змінюють геометрію ЛП так, що ПЗ поперечний розмір вже не буде репрезентативним з точки зору оцінки розмірів ЛП. З цих причин, використання тільки ПЗ поперечного розміру для оцінки розміру порожнини ЛП може бути оманливим та повинне доповнюватись визначенням об’єму ЛП, особливо при ознаках його перенавантаження та збільшення, як в рутинній клінічній практиці, так і підчас наукових досліджень.
Визначення об’єму ЛП.
При визначенні розміру ЛП в клінічній практиці сьогодні перевага віддається визначенню об’єму, а не лінійним вимірам, тому що вони дозволяють точніше оцінити розміри порожнини ЛП при його асиметричному ремоделюванні [112]. Крім того, визначено, що взаємозв’язок ризику та прогнозу серцево-судинних захворювань достовірно сильніший саме з об’ємом ЛП, а не його лінійними розмірами [98,114]. Результати ехокардіографічної оцінки об’єму ЛП в дослідженнях порівнювали з даними мультиспіральної комп’ютерної томографії, біпланової контрастної вентрикулографії та МРТ [110,115-117]. Ці дослідження показали чи високу кореляцію, чи навіть тенденцію до недооцінки ЕхоКГ об’ємів ЛП у порівнянні з іншими методами візуалізації.
Найпростішим методом оцінки об’єму ЛП є формула куба, яка має на увазі, що об’єм ЛП представляє собою сферу з діаметром, що дорівнює ПЗ поперечному розміру ЛП. Втім, цей метод виявився гіршим порівняно з іншими методами оцінки об’єму ЛП [110,112,118]. Краще за все об’єм ЛП розраховується методом еліпсоїда чи метдом Симпсона [89,90,98,102,103,110-112,116-118].
Модель еліпсоїда має на увазі, що об’єм ЛП може бути адекватно представленим продовгуватим еліпсом з об’ємом 4π/3 х (L/2) х (D1/2) x (D2/2), де L – це довга вісь еліпсоїда, а D1 та D2 – ортогональні поперечні розміри по короткій вісі. Об'єм ЛП може бути оцінений з використанням цієї біпланової формули «площа-довжина», представивши ПЗ поперечний розмір ЛП, отриманий з парастернальної позиції по довгій вісі, як D1, медіально-латеральний розмір у парастернальній позиції по короткій вісі, як D2, а повздовжній розмір ЛП в апікальній 4-камерній позиції, як L [118-120]. Також були запропоновані спрощені методи оцінки об’єму ЛП з використанням неортогональних лінійних розмірів [114]. Але об’єм, визначений за допомогою лінійних розмірів є дуже залежним від ретельного вибору локалізації виміра та направлення ліній поперечних розмірів, при чому було показано, що ці методи розрахунку суттєво недооцінюють істинний об’єм ЛП [118].
Для того, щоб оцінити поперечний розмір ЛП при використанні формули еліпсоїда більш надійно, можна обкреслити площу ЛП в межах довгої вісі з отриманням комбінованого розміру. Цей розмір приймає до уваги всю границю ЛП, а не один лінійний вимір. Коли площа в межах довгої вісі підставляється в формулу замість поперечного розміру, то використовується наступна біпланова формула «площа-довжина»: 8А1А2 / 3πL, де А1 та А2 представляють максимальну площу ЛП, отриману методом планіметрії відповідно з апікальних 4- та 2-камерної позицій, а L – повздовжній розмір ЛП. Під повздовжнім розміром розуміється довжина довгої вісі ЛП, що визначається як довжина перпендикулярної лінії, що проведена від середини площини мітрального кільця до верхньої стінки ЛП (Рис. 16). В формулі «площа-довжина» довжина вимірюється як в 4-х, так і 2-камерній позиціях, а найкоротший з цих двох вимірів використовується в формулі.
Також формула «площа-довжина» може бути розрахована з однієї площини, типово в апікальній 4-камерній позиції, виходячи з припущення, що А1=А2, щоб об’єм, таким чином, дорівнював 8(А1)2 / 3πL (Рис. 16) [121]. Втім, слід пам’ятати, що цей метод базується на геометричному припущенні, що може призводити до погрішності. У літніх пацієнтів діафрагма піднімає верхівку серця вище, що збільшує кут між шлуночком та передсердям, таким чином, апікальна 4-камерна позиція в таких випадках у літніх людей пересікає передсердя тангенціально, що веде до недооцінки об’єму при використанні тільки однієї площини у формулі «площа-довжина». Тому, враховуючи досвід більшості попередніх клінічних досліджень, при використанні моделі еліпсоїда рекомендовано використовувати біпланову формулу «площа-довжина» (Рис. 15 та 16).
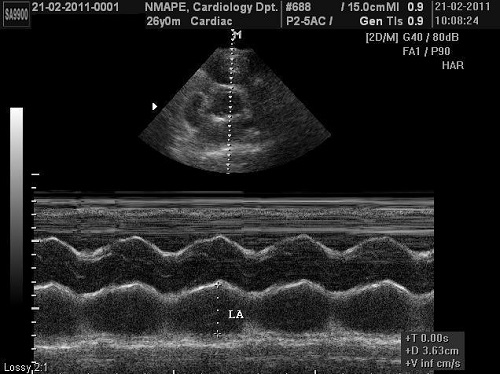
Рис. 15. Вимірювання поперечного ПЗ розміру ЛП в В-режимі та М-режимі під контролем зображення в В-режимі в парастернальній позиції по короткій вісі на рівні аортального клапана. Сьогодні лінійний метод не є рекомендованим.
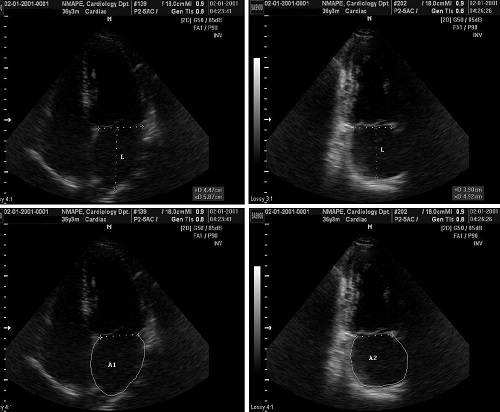
Рис. 16. Розрахунок об’єму ЛП методом «площа-довжина» з використанням апікальних 4-камерної та 2-камерної позицій наприкінці систоли шлуночків, коли розмір передсердь максимальний за формулою 8 /3π [(А1)(A2) / L]. Довжина ЛП (L) вимірюється від задньої (верхньої) стінки ЛП перпендикулярно до лінії, що поєднує точки прикріплення стулок мітрального клапану. В формулі використовується той вимір L з двох позицій, що є коротшим.
Також об’єм ЛП може бути визначений з використанням методу Симпсона подібно до того ж, як визначаються об’єми ЛШ, виходячи з припущення, що об’єм геометричної фігури може бути розрахований з суми об’ємів менших фігур меншого об’єму, що складають цю фігуру. Частіше за все, алгоритм Симпсона ділить ЛП на серію овальних дисків з умовною висотою h та ортогональними меншою та більшою вісями D1 та D2 (метод дисків). Об'єм всього ЛП може бути визначений з суми об’ємів кожного окремого диска. Об'єм розраховується за формулою π/4 (h) Σ (D1) (D2). Ця формула є виведеною за допомогою комп’ютерної програми, а розрахунковий об’єм забезпечується програмним забезпеченням ехокардіографа в режимі реального часу (Рис. 17).
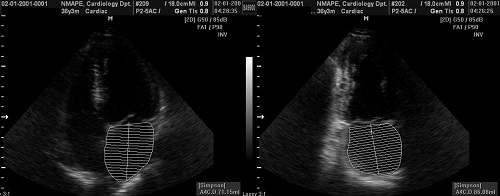
Рис. 17. Розрахунок об’єму ЛП біплановим методом дисків (модифікований метод Симсона) з використання апікальних 4-х та 2-камерної позицій наприкінці систоли шлуночків, коли передсердя мають найбільший розмір.
Використання метода Симпсона для розрахунку об’єму ЛП теж потребує використання біпланової планіметрії ЛП. Оптимальні контури повинні отримуватися ортогонально навкруги довгої вісі ЛП в апікальних трансторакальних позиціях – 4-х та 2-камерної. При цьому слід пам’ятати, що легеневі вени не повинні включатися до порожнини ЛП. Нижня межа повинна бути представлена площиною мітрального кільця.
Також можна використовувати використання однієї планіметричної площини для визначення об’єму ЛП при припущенні, що Симпсонові диски наближаються до ідеально сферичних: V = π/4 (h) Σ (D1)2. Але, як було вже зазначено вище, така формула робить припущення, що ширина ЛП в 2-х та 4-камерній позиціях є ідентичною, що дуже часто не так, тому цій формулі не можна віддавати перевагу.
Трьохвимірна ЕхоКГ повинна надавати найбільш точну оцінку об’єму ЛП та є багатообіцяючою. Втім, до сьогодні не існує консенсусних даних щодо саме метода, що повинен використовуватись для отримання даних, та немає доказових порівнянь з вже встановленими нормативами [122-124].
Нормальні значення вимірів ЛП
Неіндексовані лінійні виміри ЛП взяті з когорти Фремінгемського дослідженні серця з 1099 учасників у віці від 20 до 45 років без ознак ожиріння, середнього росту, та без серцево-судинної патології (Таб. 9) [11]. Декілько вищі значення були наведені у дослідженні в когорті з 767 учасників без серцево-судинної патології, де ожиріння та зріст не були критеріями виключення [114]. Але відомо, що соматотип та вік впливають на розмір ЛП [10,88,114]. Також помічена залежність розміру ЛП від статі, хоча, ця залежність майже повністю нівелюється більш чіткою залежністю від розміру тіла [88,114,121,125]. Вплив розміру тіла на розмір ЛП типово коригується індексацією до якогось антропометричного індексу. При чому з дитячого віку індексований об’єм ЛП змінюється дуже незначно [126]. Було запропоновано декілька методів індексації, такі як індекс зросту, маси тіла, приблизній м’язовій масі тіла, та ППТ [10,114]. Найбільш частим рекомендованим більшістю літературних даних та рекомендацій є індексація розмірів ЛП до ППТ.
Нормальний індекс об’єму ЛП до ППТ був визначений з використанням рекомендованих біпланових методів розрахунку («площа-довжина» чи метод дисків Симпсона) у декількох дослідженнях з залученням декількох сотень індивідів, та становить 22±6 мл/м2 [89,121,127,128]. Існує також норматив нормального об’єму ЛП, втім, у клінічній практиці рекомендовано вживати саме індекс об’єму ЛП до ППТ, як такий, що враховує варіабельність розміру тіла пацієнтів. Оскільки ризик кардіальних подій та розмір ЛП є тісно взаємопов’язаними, визначення нормальних реферативних значень для об’єму ЛП є навіть більш важливим, ніж просто характеристика ступеня збільшення лінійного розміру ЛП. Сьогодні існує велика кількість взаємно підтверджуючих статей, що свідчать про прогресивне збільшення ризику серцево-судинних подій, асоційоване зі збільшенням об’ємів ЛП вище цих нормативних значень [90,98,100-104,107-109,129]. З часом, індексація об’єму ЛП повинна стати рутинним виміром в ехокардіографічні лабораторії, оскільки вона відбиває тягар та хронічний характер підвищення тиску наповнення ЛШ та є потужним пре диктором прогнозу.
Праве передсердя.
Щодо кількісної оцінки правого передсердя (ПП) існує набагато менше даних досліджень та клінічних даних. Хоча ПП може бути оцінене якісно з багатьох різних позицій, кількісна оцінка розміру ПП найчастіше виконується з апікальної 4-камерної позиції. Поперечний розмір повинен вимірюватись перпендикулярно довгій вісі ПП від латеральної межі ПП до міжпередсердної перегородки. Нормативні значення для поперечного розміру ПП наведені в таб. 9. Хоча розмір ПП може варіювати залежно від статі, на сьогодні не існує окремих реферативних значень для жінок та чоловіків.
Таб. 9. Референтні значення та градація збільшення розмірів / об’ємів ЛП.
|
|
Жінки
|
Чоловіки
|
|
Межі норми
|
Легке підвищен-ня
|
Помірне підви-щення
|
Важке підвищення
|
Межі норми
|
Легке підвищен-ня
|
Помірне підви-щення
|
Важке підви-щення
|
|
Розміри передсердя
|
|
|
ПЗ розмір ЛП, см
|
2,7-3,8
|
3,9-4,2
|
4,3-4,6
|
≥4,7
|
3,0-4,0
|
4,1-4,6
|
4,7-5,2
|
≥5,2
|
|
Індекс ЛП розміру ЛП/ППТ, см/м2
|
1,5-2,3
|
2,4-2,6
|
2,7-2,9
|
≥3,0
|
1,5-2,3
|
2,4-2,6
|
2,7-2,9
|
≥3,0
|
|
Поперечний розмір ПП, см
|
2,9-4,5
|
4,6-4,9
|
5,0-5,4
|
≥5,5
|
2,9-4,5
|
4,6-4,9
|
5,0-5,4
|
≥5,5
|
|
Індекс поперечного розміру ПП/ППТ, см/м2
|
1,7-2,5
|
2,6-2,8
|
2,9-3,1
|
≥3,2
|
1,7-2,5
|
2,6-2,8
|
2,9-3,1
|
≥3,2
|
|
Площа передсердя
|
|
|
Площа ЛП, см2
|
≤20
|
20-30
|
30-40
|
>40
|
≤20
|
20-30
|
30-40
|
>40
|
|
Об'єм передсердя
|
|
Об'єм ЛП, мл
|
22-52
|
53-62
|
63-72
|
≥73
|
|
|
|
≥79
|
|
Індекс об’єму ЛП/ ППТ, мл/м2
|
22±6
|
29-33
|
34-39
|
≥40
|
22±6
|
29-33
|
34-39
|
≥40
|
|
|
|
|
|
|
|
|
|
|
|
|
Хоча з визначення об’єму ПП дані є обмеженими, оцінка об’ємів ПП має бути більш надійною та точною для визначення розміру ПП, ніж лінійні виміри. Оскільки не існує стандартних ортогональних позицій візуалізації ПП для виконання біпланових розрахунків, в декількох невеликих дослідженнях для оцінки об’єму ПП застосовувалися методи «площа-довжина» та дисків Симпсона в одній проекції [121,131,132]. Ми вважаємо, що сьогодні існує замало взаємно підтверджуючих літературних даних, які б дозволили рекомендувати певні нормативні волюмометричні значення для ПП. Втім, обмежена кількість даних з невеликої кількості здорових індивідів дозволяє стверджувати, що індексований нормальний об’єм ПП є подібним до нормативних значень ЛП у чоловіків (21 мл/м2), але є незначно меншим у жінок [121]. Нормальні межі максимального систолічного поперечного розміру ПП становлять 3,4-5,3 см при нормальній кінцево-систолічній площі в апікальній 4-камерній позиції 10-18 см2 [84].
Кількісні виміри аорти та нижньої порожнистої вени
Виміри аорти.
Запис зображення повинен виконуватися з парастернального акустичного вікна по довгій вісі ЛШ для візуалізації кореня аорті та проксимального відділу висхідної аорти. Для візуалізації виносного тракту ЛШ та кореня аорти повинен використовуватися В-режим, а для візуалізації та запису зображення кореня аорти слід використовувати різні види з різних міжреберних проміжків та на різній відстані від лівого краю грудини. Праві парастернальній доступи, що записуються у положенні пацієнта на правому боці, також можуть бути корисними. Виміри звичайно проводяться: 1) на рівні кільця аортального клапана (АК) (рівень прикріплення стулок); 2) на рівні максимального діаметру синусів Вальсальви; 3) на рівні синотубулярного переходу (перехід синусів Вальсальви в тубулярну частину висхідної аорти).
Види, що використовуються для вимірів, мають бути ті, що дозволяють побачити найбільший діаметр аорти, а особливо важливим є використання максимального поперечного діаметру, перпендикулярного до довгої вісі судини в даному конкретному доступі. Деякі експерти надають перевагу виміру поперечного діаметра від внутрішнього краю до внутрішнього краю з метою кореляції з іншими методами візуалізації аорти, зокрема МРТ та комп’ютерною томографією. Втім, існуючі сьогодні нормативні дані щодо розмірів аорти для ЕхоКГ були отримані методом виміру від верхнього краю до верхнього краю (Рис. 18). Прогрес у якості ехокардіографічного зображення завдяки технологіям поліпшення розрішення має мінімізувати різницю між цими двома методиками, хоча Українська Асоціація фахівців з ЕхоКГ рекомендує використовувати вимірювання від внутрішнього до внутрішнього краю.
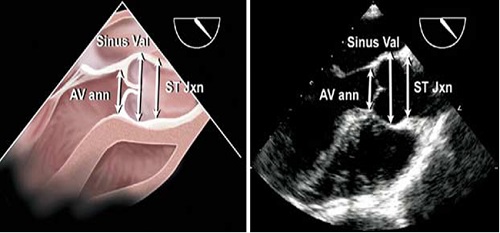
Рис. 18. Вимірювання діаметрів кореня аорти на рівні кільця АК, синусів Вальсальви та синотубулярного переходу. Діаметр кільця конвенційно вимірюється на рівні прикріплення стулок АК. Хоча наведена методика вимірів від верхнього краю до верхнього краю, деякі експерти віддають перевагу вимірам від внутрішнього краю до внутрішнього краю (AV ann – кільце АК, Sinus Val – синуси Вальсальви, ST Jxn – синотубулярний перехід), до чого схиляється і Українська асоціація фахівців з ЕхоКГ [1].
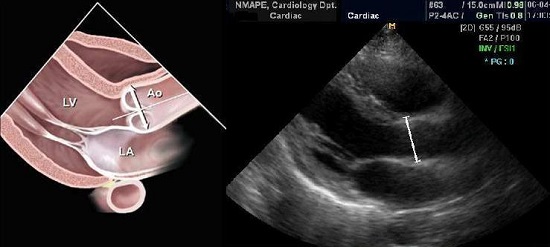
Рис. 19. Вимірювання діаметру кореня аорти на рівні синусів Вальсальви у В-режимі з парастернальної позиції по довгій вісі ЛШ. Хоча на рисунку вказана техніка виміру «від верхнього краю до верхнього краю», деякі експерти надають перевагу техніці «від внутрішнього краю до внутрішнього краю» (див. текст для обговорення).
Сьогодні віддають перевагу вимірам діаметрів аорти в В-режимі над вимірами в М-режимі, тому що циклічні рухи серця та результуючі зміни положення курсору М-режиму відносно максимального діаметра синусів Вальсальви призводять до систематичного заниження (~2 мм) діаметра аорти в М-режимі порівняно з даними В-режиму [133]. Діаметр кільця АК вимірюється між точками прикріплення стулок АК (від внутрішнього краю до внутрішнього краю) в парастернальній або апікальній позиціях по довгій вісі ЛШ, які дозволяють вивести максимальний діаметр кільця АК. При цьому в разі необхідності (напр., субоптимальна візуалізація) корисно одночасно проводити кольорове допплерівське картування порожнини для кращої диференціації поверхонь.
Грудний відділ аорти краще можна візуалізувати за допомогою ЧСЕхоКГ, ніж ТТЕхоКГ, тому що більша її частина при ЧСЕхоКГ знаходиться в полі досягнення черезстравохідним датчиком. Висхідна аорта може бути візуалізоване з середньо-стравохідного доступу по довгій вісі на приблизно 1300 та з середньо-стравохідного доступу по довгій вісі висхідної аорти. Коротку вісь висхідної аорти отримують з середньо-стравохідних доступів під кутом приблизно 450. Для вимірів низхідної аорти короткі зрізи можуть бути отримані під кутом 00, а довгі зрізи – під кутом близько 900, по всій довжині від діафрагми до дуги аорти (Рис. - 19). Власно дуга аорти та два з трьох великих брахіоцефальних судин можуть бути візуалізовані в більшості пацієнтів. Існує «сліпа пляма» верхньої частини висхідної аорти та проксимальної частини дуги аорти, що не може бути побачена підчас ЧСЕхоКГ внаслідок біфуркації трахеї, що заважає.
Визначення дилатації кореня аорти.
Найбільш сильно корелює з ППТ та віком діаметр аорти на рівні синусів Вальсальви. Тому, згідно опублікованих математичних рівнянь, ППТ може бути використана як предиктор діаметру кореня аорти в трьох вікових групах: молодших 20 років, від 20 до 40 років, та старших 40 років [133]. Дилатація кореня аорти на рівні синусів Вальсальви визначається як діаметр кореня аорти, що перевищує верхню межу 95% довірчого інтервалу розподілу в великій референтній популяції [134]. Дилатація аорти може бути легко зафіксована за допомогою використання раніше опублікованих номограм залежності діаметру кореня аорти від ППТ (Рис. 20) [133]. Рівняння для визначення очікуваного діаметру аорти на рівні синусів Вальсальви відносно до ППТ для кожної з вікових груп наведені на рис. 20. Індекс кореня аорти, або відношення реального діаметру кореня аорти до очікуваного за номограмою розрахувати можна, поділивши отриманий діаметр кореня аорти на рівні синусів Вальсальви у даного пацієнта на очікуваний діаметр згідно номограми даної вікової групи. Дилатація кореня аорти має потужну асоціацію з виникненням, наявністю та прогресуванням аортальної регургітації [134] та ризиком розшарування аорти [135]. Наявність артеріальної гіпертензії, виявляється, має мінімальний вплив на діаметр кореня аорти, але є асоційованою зі збільшенням більш дистальних сегментів грудного відділу аорти [134, 136].
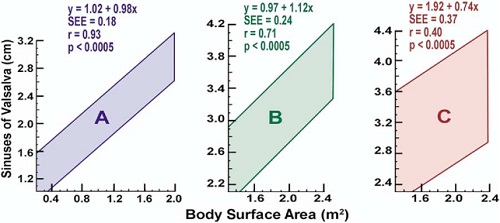
Рис. 20. 95% довірчій інтервал для діаметру кореня аорти на рівні синусів Вальсальви на основі площі поверхні тіла для дітей та підлітків (А), дорослих 20-39 років (В) та дорослих старше 40 років та старше (С) (Sinuses of Valsalva – синуси Вальсальви у см; Body Surface Area – площа поверхні тіла у м2) [133].
Оцінка нижньої порожнистої вени.
Дослідження нижньої порожнистої вени (НПВ) з субкостальної позиції повинно бути частиною рутинного трансторакального ехокардіографічного дослідження. Загально погоджено, що діаметр НПВ слід вимірювати в лежачому положенні пацієнта на відстані від 1,0 до 2,0 см до місця впадіння НПВ в ПП перпендикулярно довгій вісі НПВ в субкостальній позиції по довгій вісі шлуночків (Рис. 21). Діаметр НПВ зменшується підчас вдихання у відповідь на негативний інтраторакальний тиск, що призводить до підвищення наповнення ПП з системних колекторних вен. Діаметр НПВ та відсоток зменшення діаметра підчас вдихання корелює з тиском у ПП. Цей взаємозв’язок отримав назву індексом колабування [138]. Оцінка інспіраторної відповіді НПВ часто потребує різкого короткого вдихання, тому що нормальна амплітуда дихання часто не провокує такої відповіді.
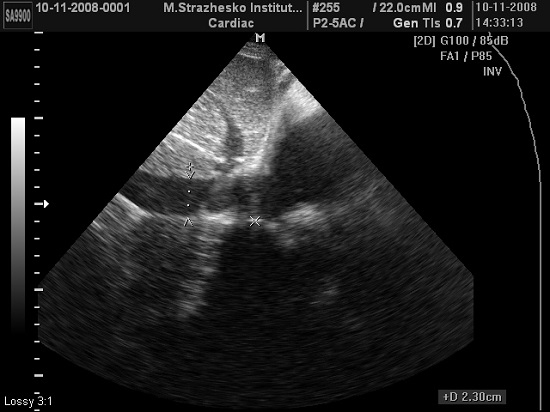
Рис. 21. Вимірювання діаметру НПВ в субкостальній позиції по довгій вісі шлуночків на відстані від 1,0 до 2,0 см від місця впадіння НПВ у ПП.
На відміну від попередніх нормативів [1], згідно яких в нормі діаметр НПВ не перевищує 1,7 см, останні рекомендації ASE з оцінки правих відділів серця у дорослих [84] дещо збільшили межі норми. Згідно них, в нормі максимальний діаметр НПВ не перевищує 2,1 см. При нормальному тиску у ПП (0-5 мм рт. ст.) НПВ зменшується у діаметрі щонайменш на 50%. Дилатація НПВ >2,1 см при нормальному інспіраторному колапсі (≥50%) або зменшення інспіраторного колапсу <50% при нормальному діаметрі НПВ свідчать про незначно підвищений тиск у ПП (6-10 мм рт. ст.). Коли інспіраторний колапс становить менше 50%, тиск у ПП звичайно складає 11-15 мм рт. ст. Нарешті, дилатація НПВ та відсутність будь-яких інспіраторних коливань говорить про значно підвищений тиск у ПП (>15 мм рт. ст.). Остання ситуація, звичайно, супроводжується рестриктивним наповненням ПШ та переважанням діастолічного кровотоку в печінкових венах (Таб. 10).
Напроти, зменшення діаметру НПВ (звичайно <1,2 см) та її спонтанний колапс часто спостерігається при наявності зниження ОЦК [137].
Існує декілька додаткових станів, про які слід пам’ятати при оцінці НПВ. Дилатація НПВ з нормальним індексом колабування часто спостерігається у спортсменів. Деякі дослідження [138,139] довели, що середній діаметр НПВ у спортсменів становив 2,31±0,46 см порівняно з 1,14±0,13 см у аналогічній за віком групі контролю. Найбільші діаметри НПВ знаходили у професійних пловців.
Таб. 10. Оцінка тиску в ПП (ЦВТ) на основі діаметру та інспіраторного колапсу НПВ.
|
Показник
|
Нормальний (0-5 mm Hg)
|
Незначне підвищення
(5-10 mm Hg)
|
Помірне підвищення
(10-15 mm Hg)
|
Значне підвищення
(≥15 mm Hg)
|
|
Діаметр НПВ, см
|
≤ 2,1 см
|
≤ 2,1 см
|
>2,1 см
|
>2,1 см
|
|
Інспіраторний колапс, %
|
>50%
|
<50%
|
25-50%
|
0-25%
|
Одне з досліджень показало, що дилатована НПВ у хворих на штучній вентиляції легенів не завжди є показником підвищення тиску в ПП. Втім, маленький діаметр НПВ (<1,2 см) мав специфічність 100%, але низьку чутливість при тиску у ПП <10 мм рт. ст. [140]. Результати більш недавнього дослідження наводять дані про кращу кореляцію між діаметром НПВ та тиском у ПП, коли діаметр НПВ вимірюється наприкінці видиху та в кінці діастоли в М-режимі [141].
Використання діаметру НПВ та його динамічних коливань є рекомендованим для визначення тиску у ПП. Ця методика повинна використовуватися у визначенні систолічного тиску в легеневій артерії на основі пікової швидкості потоку трикуспідальної регургітації.
Література.
1. Lang R.M. Recommendations for Chamber Quantification: A Report from the American Society of Echocardiography’s Guidelines and Standards Committee and the Chamber Quantification Writing Group, Developed in Conjunction with the European Association of Echocardiography, a Branch of the European Society of Cardiology // J. Am. Soc. Echocardiogr. – 2005. – Vol. 18. – p. 1440-1463
2. Schiller N.B., Shah P.M., Crawford M., et al. Recommendations for quantitation of the left ventricle by two-dimensional echocardiography: American Society of Echocardiography committee on standards, subcommittee on quantitation of two-dimensional echocardiograms // J. Am. Soc. Echocardiogr. – 1989. – Vol. 2. – p. 358-67.
3. Hirata K., Watanabe H., Beppu S., et al. Pitfalls of echocardiographic measurement in tissue harmonic imaging: in vitro and in vivo study // J. Am. Soc. Echocardiogr. 2002. – Vol. 15. – p. 1038-44.
4. McGavigan A.D., Dunn F.G., Goodfield N.E. Secondary harmonic imaging overestimates left ventricular mass compared to fundamental echocardiography // Eur. J. Echocardiogr. – 2003. – Vol. 4. – p. 178-81.
5. Feigenbaum H., Armstrong W., Ryan T. Feigenbaum’s echocardiography. 6th ed. Philadelphia: Lippincott, Williams and Wilkins. – 2005.
6. Mulvagh S.L., DeMaria A.N., Feinstein S.B., et al. Contrast echocardiography: current and future applications // J. Am. Soc. Echocardiogr. – 2000. – Vol. 13. – p. 331-42.
7. Nahar T., Croft L., Shapiro R., et al. Comparison of four echocardiographic techniques for measuring left ventricular ejection fraction // Am. J. Cardiol. – 2000. – Vol. 86. – p. 1358-62.
8. Colombo P.C., Municino A., Brofferio A., et al. Cross-sectional multiplane transesophageal echocardiographic measurements: comparison with standard transthoracic values obtained in the same setting // Echocardiography. – 2002. – Vol. - 19. – p. 383-90.
9. Hozumi T., Shakudo M., Shah P.M. Quantitation of left ventricular volumes and ejection fraction by biplane transesophageal echocardiography // Am. J. Cardiol. – 1993. – Vol. 72. – p. 356-9.
10. Vasan R.S., Levy D., Larson M,G,, Benjamin E,J. Interpretation of echocardiographic measurements: a call for standardization // Am // Heart. J. – 2000. - Vol. 139. - p. 412-22.
11. Vasan R.S., Larson M.G., Levy D., et al. Distribution and categorization of echocardiographic measurements in relation to reference limits: the Framingham heart study; formulation of a height- and sex-specific classification and its prospective validation // Circulation. – 1997. – Vol. 96. – p. 1863-73.
12. Devereux R.B., Roman M.J. Evaluation of cardiac and vascular structure by echocardiography and other noninvasive techniques. In: Laragh J.H., Brenner B.M., editors. Hypertension: pathophysiology, diagnosis, treatment. 2nd ed. New York: Raven Press; 1995. p. - 1969-85.
13. Gottdiener J.S., Bednarz J., Devereux R., et al. American Society of Echocardiography recommendations for use of echocardiography in clinical trials // J. Am. Soc. Echocardiogr. – 2004. – Vol. 17. – p. 1086-119.
14. Wyatt H.L., Heng M.K., Meerbaum S., et al. Cross-sectional echocardiography, I: analysis of mathematic models for quantifying mass of the left ventricle in dogs // Circulation. - 1979. - Vol. 60. - p. 1104-13.
15. Reichek N., Helak J., Plappert T., et al. Anatomic validation of left ventricular mass estimates from clinical two-dimensional echocardiography: initial results // Circulation. – 1983. – Vol. 67. – p. 348-52.
16. Helak J.W., Reichek N. Quantitation of human left ventricular mass and volume by two-dimensional echocardiography: in vitro anatomic validation // Circulation. – 1981. – Vol. 63. – p. 1398-407.
17. Schiller N.B., Skioldebrand C.G., Schiller E.J., et al. Canine left ventricular mass estimation by two-dimensional echocardiography // Circulation. – 1983. – Vol. 68. – p. 210-6.
18. Triulzi M.O., Gillam L.D., Gentile F., et al. Normal adult cross-sectional echocardiographic values: linear dimensions and chamber areas // Echocardiography. – 1984. – Vol. 1. – p. 403-26.
19. Devereux R.B., Wachtell K., Gerdts E., et al. Prognostic significance of left ventricular mass change during treatment of hypertension // JAMA. – 2004. – Vol. 292. – p. 1-7.
20. Ilercil A., O’Grady M.J., Roman M.J., et al. Reference values for echocardiographic measurements in urban and rural populations of differing ethnicity: the strong heart study // J. Am. Soc. Echocardiogr. – 2001. – Vol. 14. – p. 601-11.
21. Devereux R.B., Alonso D.R., Lutas E.M., et al. Echocardiographic assessment of left ventricular hypertrophy: comparison to necropsy findings // Am. J. Cardiol. – 1986. – Vol. 57. – p. 450-8.
22. Ganau A., Devereux R.B., Roman M.J., et al. Patterns of left ventricular hypertrophy and geometric remodeling in essential hypertension // J. Am. Coll. Cardiol. – 1992. – Vol. 19. – p. 1550-8.
23. Devereux R.B., de Simone G., Pickering T.G., et al. Relation of left ventricular midwall function to cardiovascular risk factors and arterial structure and function // Hypertension. – 1998. – Vol. 31. – p. 929-36.
24. Palmieri V., Dahlof B., DeQuattro V., et al. Reliability of echocardiographic assessment of left ventricular structure and function. - p. the PRESERVE prospective randomized study evaluating regression of ventricular enlargement // J. Am. Coll. Cardiol. – 1999. – Vol. 34. – p. 1625-32.
25. Nidorf S.M., Picard M.H., Triulzi M.O., et al. New perspectives in the assessment of cardiac chamber dimensions during development and adulthood // J. Am. Coll. Cardiol. – 1992. – Vol. 19. – p. 983-8.
26. Pearlman J.D., Triulzi M.O., King M.E., et al. Limits of normal left ventricular dimensions in growth and development: analysis of dimensions and variance in the two-dimensional echocardiograms of 268 normal healthy subjects // J. Am. Coll. Cardiol. – 1988. – Vol. 12. – p. 1432-41.
27. Lang R.M., Borow K.M., Neumann A., Janzen D. Systemic vascular resistance: an unreliable index of left ventricular afterload // Circulation. – 1986. – Vol. 74. – p. 1114-23.
28. Quinones M.A., Waggoner A.D., Reduto L.A., et al. A new, simplified and accurate method for determining ejection fraction with two-dimensional echocardiography // Circulation. – 1981. – Vol. 64. – p. 744-53.
29. Teichholz L.E., Kreulen T., Herman M.V., Gorlin R. Problems in echocardiographic volume determinations: echocardiographic-angiographic correlations in the presence of absence of asynergy // Am. J. Cardiol. – 1976. – Vol. 37. – p. 7-11.
30. de Simone G., Devereux R.B., Roman M.J., et al. Assessment of left ventricular function by the midwall fractional shortening/end-systolic stress relation in human hypertension // J. Am. Coll. Cardiol. – 1994. – Vol. 23. – p. 1444-51.
31. Shimizu G., Zile M.R., Blaustein A.S., Gaasch W.H. Left ventricular chamber filling and midwall fiber lengthening in patients with left ventricular hypertrophy: overestimation of fiber velocities by conventional midwall measurements // Circulation. – 1985. – Vol. 71. – p. 266-72.
32. Celentano A., Palmieri V., Arezzi E., et al. Gender differences in left ventricular chamber and midwall systolic function in normotensive and hypertensive adults // J. Hypertens. – 2003. – Vol . 21. – p. 1415-23.
33. Gerdts E., Zabalgoitia M., Bjornstad H., et al. Gender differences in systolic left ventricular function in hypertensive patients with electrocardiographic left ventricular hypertrophy (the LIFE study) // Am. J. Cardiol. – 2001. – Vol. 87. – p. 980-3.
34. Devereux R.B., Roman M.J., de Simone G., et al. Relations of left ventricular mass to demographic and hemodynamic variables in American Indians: the strong heart study // Circulation. – 1997. – Vol. 96. – p. 1416-23.
35. Devereux R.B., Bella J.N., Palmieri V., et al. Left ventricular systolic dysfunction in a biracial sample of hypertensive adults: the hypertension genetic epidemiology network (HyperGEN) study // Hypertension. – 2001. – Vol. 38. – p. 417-23.
36. Roman M.J., Pickering T.G., Schwartz J.E., et al. Association of carotid atherosclerosis and left ventricular hypertrophy // J. Am. Coll. Cardiol. – 1995. – Vol. 25. – p. 83-90.
37. Wahr D.W., Wang Y.S., Schiller N.B. Left ventricular volumes determined by two-dimensional echocardiography in a normal adult population // J. Am. Coll. Cardiol. – 1983. – Vol. 1. – p. 863-8.
38. de Simone G., Daniels S.R., Devereux R.B., et al. Left ventricularmass and body size in normotensive children and adults: assessment of allometric relations and impact of overweight // J. Am. Coll. Cardiol. – 1992. – Vol. 20. – p. 1251-60.
39. Devereux R.B., Palmieri V., Sharpe N., et al. Effects of once-daily angiotensin-converting enzyme inhibition and calcium channel blockadebased antihypertensive treatment regimens on left ventricular hypertrophy and diastolic filling in hypertension: the prospective randomized enalapril study evaluating regression of ventricular enlargement (preserve) trial // Circulation. – 2001. – Vol. 104. – p. 1248-54.
40. Kizer J.R., Arnett D.K., Bella J.N., et al. Differences in left ventricular structure between black and white hypertensive adults: the hypertension genetic epidemiology network study // Hypertension. – 2004. – Vol. 43. – p. 1182-8.
41. Devereux R.B., Casale P.N., Kligfield P., et al. Performance of primary and derived M-mode echocardiographic measurements for detection of left ventricular hypertrophy in necropsied subjects and in patients with systemic hypertension,mitral regurgitation and dilated cardiomyopathy // Am. J. Cardiol. – 1986. – Vol. 57. – p. 1388-93.
42. Malcolm D.D., Burns T.L., Mahoney L.T., Lauer R.M. Factors affecting left ventricular mass in childhood: the Muscatine study // Pediatrics. – 1993. – Vol. 92. – p. 703-9.
43. Daniels S.R., Meyer R.A., Liang Y.C., Bove K.E. Echocardiographically determined left ventricular mass index in normal children, adolescents and young adults // J. Am. Coll. Cardiol. – 1988. – Vol. 12. – p. 703-8.
44. Daniels S.R., Kimball T.R., Morrison J.A., et al. Indexing left ventricular mass to account for differences in body size in children and adolescents without cardiovascular disease // Am. J. Cardiol. – 1995. – Vol. 76. – p. 699-701.
45. de S.G., Devereux R.B., Daniels S.R., et al. Effect of growth on variability of left ventricular mass: assessment of allometric signals in adults and children and their capacity to predict cardiovascular risk // J. Am. Coll. Cardiol. – 1995. - Vol. 25. – p. 1056-62.
46. Gopal A.S., Keller A.M., Rigling R., et al. Left ventricular volume and endocardial surface area by three-dimensional echocardiography: comparison with two-dimensional echocardiography and nuclear magnetic resonance imaging in normal subjects // J. Am. Coll. Cardiol. – 1993. – Vol. 22. – p. 258-70.
47. Handschumacher M.D., Lethor J.P., Siu S.C., et al. A new integrated system for threedimensional echocardiographic reconstruction: development and validation for ventricular volume with application in human subjects // J. Am. Coll. Cardiol. – 1993. – Vol. 21. – p. 743-53.
48. Jiang L., Vazquez de Prada J.A., Handschumacher M.D., et al. Quantitative three-dimensional reconstruction of aneurysmal left ventricles: in vitro and in vivo validation // Circulation. – 1995. – Vol. 91. – p. 222-30.
49. King D.L., Harrison M.R., King D.L. Jr., at al. Improved reproducibility of left atrial and left ventricular measurements by guided three-dimensional echocardiography // J. Am. Coll. Cardiol. – 1992. – Vol. 20. – p. 1238-45.
50. Kuhl H.P., Franke A., Frielingsdorf J., et al. Determination of left ventricular mass and circumferential wall thickness by three-dimensional reconstruction: in vitro validation of a new method that uses a multiplane transesophageal transducer // J. Am. Soc. Echocardiogr. – 1997. – Vol. 10. – p. 107-19.
51. Roelandt J.R., Ten Cate F.J., Vletter W.B., Taams M.A. Ultrasonic dynamic three-dimensional visualization of the heart with a multiplane transesophageal imaging transducer // J. Am. Soc. Echocardiogr. – 1994. – Vol. 7. – p. 217-29.
52. Sheikh K., Smith S.W., von Ramm O., Kisslo J. Real-time, three-dimensional echocardiography: feasibility and initial use // Echocardiography. – 1991. – Vol. 8. – p. 119-25.
53. Wollschlager H., Zeiher A.M., Geibel A., et al. Transespohogeal echo computer tomography: computational reconstruction of any desired view of the beating heart. In: Hanrath P, Uebis R, Krebs W, editors. Cardiovascular imaging by ultrasound. Dordrecht: Kluwer. – 1993.
54. Buck T., Hunold P., Wentz K.U., et al. Tomographic three-dimensional echocardiographic determination of chamber size and systolic function in patients with left ventricular aneurysm: comparison to magnetic resonance imaging, cineventriculography, and two-dimensional echocardiography // Circulation. – 1997. – Vol. 96. – p. 4286-97.
55. Kuhl H.P., Franke A., Merx M., et al. Rapid quantification of left ventricular function and mass using transesophageal three-dimensional echocardiography: validation of a method that uses long-axis cutplanes // Eur. J. Echocardiogr. – 2000. – Vol. 1. – p. 213-21.
56. Nosir Y.F., Fioretti P.M., Vletter W.B., et al. Accurate measurement of left ventricular ejection fraction by three-dimensional echocardiography: a comparison with radionuclide angiography // Circulation. – 1996. – Vol. 94. – p. 460-6.
57. Gopal A.S., Schnellbaecher M.J., Shen Z., et al. Freehand three-dimensional echocardiography for determination of left ventricular volume and mass in patients with abnormal ventricles: comparison with magnetic resonance imaging // J. Am. Soc. Echocardiogr. – 1997. – Vol. 10. – p. 853-61.
58. Shiota T., Jones M., Chikada M., et al. Real-time three-dimensional echocardiography for determining right ventricular stroke volume in an animal model of chronic right ventricular volume overload // Circulation. – 1998. – Vol. 97. – p. 1897-900.
59. Mor-Avi V., Sugeng L., Weinert L., et al. Fast measurement of left ventricular mass with real-time three-dimensional echocardiography: comparison with magnetic resonance imaging // Circulation. – 2004. – Vol. 110. – p. 1814-8.
60. Jiang L., Siu S.C., Handschumacher M.D., et al. Three-dimensional echocardiography: in vivo validation for right ventricular volume and function // Circulation. – 1994. – Vol. 89. – p. 2342-50.
61. Jiang L., Vazquez de Prada J.A., Handschumacher M.D., et al. Three-dimensional echocardiography: in vivo validation for right ventricular free wall mass as an index of hypertrophy // J. Am. Coll. Cardiol. – 1994. – Vol. 23. – p. 1715-22.
62. Cerqueira M.D., Weissman N.J., Dilsizian V., et al. Standardized myocardial segmentation and nomenclature for tomographic imaging of the heart: a statement for healthcare professionals from the cardiac imaging committee of the council on clinical cardiology of the American Heart Association // Circulation. – 2002. – Vol. 105. – p. 539-42.
63. Edwards W.D., Tajik A.J., Seward J.B. Standardized nomenclature and anatomic basis for regional tomographic analysis of the heart // Mayo Clin. Proc. – 1981. – Vol. 56. – p. 479-97.
64. Heger J.J., Weyman A.E., Wann L.S., et al. Cross-sectional echocardiography in acutemyocardial infarction: detection and localization of regional left ventricular asynergy // Circulation. – 1979. – Vol. 60. – p. 531-8.
65. Kerber R.E., Abboud F.M. Echocardiographic detection of regionalmyocardial infarction: an experimental study // Circulation. – 1973. – Vol. 47. – p. 997-1005.
66. Weiss J.L., Bulkley B.H., Hutchins G.M., Mason S.J. Twodimensional echocardiographic recognition of myocardial injury in man: comparison with postmortem studies // Circulation. – 1981. – Vol. 63. – p. 401-8.
67. Ross J. Jr. Myocardial perfusion-contraction matching: implications for coronary heart disease and hibernation // Circulation. - 1991. – Vol. 83. – p. 1076-83.
68. Lieberman A.N., Weiss J.L., Jugdutt B.I., et al. Two-dimensional echocardiography and infarct size: relationship of regional wall motion and thickening to the extent of myocardial infarction in the dog // Circulation. – 1981. – Vol. 63. – p. 739-46.
69. Fagard R., Aubert A., Lysens R., et al. Noninvasive assessment of seasonal variations in cardiac structure and function in cyclists // Circulation. – 1983. – Vol. 67. – p. 896-901.
70. Fisher A.G., Adams T.D., Yanowitz F.G., et al. Noninvasive evaluation of world-class athletes engaged in different modes of training // Am. J. Cardiol. – 1989. – Vol. 63. – p. 337-41.
71. Vos M., Hauser A.M., Dressendorfer R.H., et al. Enlargement of the right heart in the endurance athlete: a two-dimensional echocardiographic study // Int. J. Sports Med. – 1985 – Vol 6. – p 271-5.
72. Douglas P.S., O’Toole M.L., Hiller W.D., Reichek N. Left ventricular structure and function by echocardiography in ultraendurance athletes // Am. J. Cardiol. – 1986. – Vol. 58. – p. 805-9.
73. Pelliccia A., Maron B.J., Spataro A., et al. The upper limit of physiologic cardiac hypertrophy in highly trained elite athletes // N. Engl. J. Med. – 1991. – Vol. 324. – p. 295-301.
74. Neri Serneri G.G., Boddi M., Modesti P.A., et al. Increased cardiac sympathetic activity and insulin-like growth factor-I formation are associated with physiological hypertrophy in athletes // Circ. Res. – 2001. – Vol. 89. – p. 977-82.
75. Matsukubo H., Matsuura T., Endo N., et al. Echocardiographic measurement of right ventricular wall thickness: a new application of subxiphoid echocardiography // Circulation. – 1977. – Vol. 56. – p. 278-84.
76. Foale R., Nihoyannopoulos P., McKenna W., et al. Echocardiographic measurement of the normal adult right ventricle // Br // Heart. J. – 1986. – Vol. 56. – p. 33-44.
77. Roman M.J., Ganau A., Saba P.S., et al. Impact of arterial stiffening on left ventricular structure // Hypertension. – 2000. – Vol.36. – p. 489-94.
78. Picard M.H., Wilkins G.T., Ray P.A., Weyman A.E. Natural history of left ventricular size and function after acute myocardial infarction: assessment and prediction by echocardiographic endocardial surface mapping // Circulation. – 1990. – Vol. 82. – p. 484-94.
79. St John Sutton M., Pfeffer M.A., Moye L., et al. Cardiovascular death and left ventricular remodeling two years after myocardial infarction: baseline predictors and impact of long-term use of captopril; information fromthe survival and ventricular enlargement (SAVE) trial // Circulation. – 1997. – Vol. 96. – p. 3294-9.
80. Weyman A. Practices and principles of echocardiography. 2nd ed. Philadelphia: Lippincott, Williams and Wilkins. – 1994.
81. Zornoff L.A., Skali H., Pfeffer M.A., et al. Right ventricular dysfunction and risk of heart failure and mortality after myocardial infarction // J. Am. Coll. Cardiol. – 2002. – Vol. 39. – p. 1450-5.
82. Yoerger D.M., Marcus F., Sherrill D., et al. Echocardiographic findings in patients meeting task force criteria for arrhythmogenic right ventricular dysplasia: new insights from the multidisciplinary study of right ventricular dysplasia // J. Am. Coll. Cardiol. – 2005. – Vol. 45. – p. 860-5.
83. Schenk P., Globits S., Koller J., et al. Accuracy of echocardiographic right ventricular parameters in patients with different end-stage lung diseases prior to lung transplantation // J // Heart. . Lung. Transplant. – 2000. – Vol. 19. – p. 145-54.
84. Rudski L.G., et al. Guidelines for the Echocardiographic Assessment of the Right Heart in Adults: A Report from the American Society of Echocardiography Endorsed by the European Association of Echocardiography, a registered branch of the European Society of Cardiology, and the Canadian Society ofEchocardiography // J. Am. Soc. Echocardiogr. – 2010. – Vol. 23. – P. 685-713.
85. Samad B.A., Alam M., Jensen-Urstad K. Prognostic impact of right ventricular involvement as assessed by tricuspid annular motion in patients with acute myocardial infarction // Am. J. Cardiol. – 2002. – Vol. 90. – p. 778-81.
86. Maslow A.D., Regan M.M., Panzica P., et al. Precardiopulmonary bypass right ventricular function is associated with poor outcome after coronary artery bypass grafting in patients with severe left ventricular systolic dysfunction // Anesth. Analg. – 2002. – Vol. 95. – p. 1507-18.
87. Severino S., Caso P., Cicala S., et al. Involvement of right ventricle in left ventricular hypertrophic cardiomyopathy: analysis by pulsed Doppler tissue imaging // Eur. J. Echocardiogr. – 2000. – Vol. 1. – p. 281-8.
88. Spencer K.T., Mor-Avi V., Gorcsan J. III, et al. Effects of aging on left atrial reservoir, conduit, and booster pump function: a multiinstitution acoustic quantification study // Heart. – 2001. – Vol. 85. – p. 272-7.
89. Tsang T.S., Barnes M.E., Gersh B.J., et al. Left atrial volume as a morphophysiologic expression of left ventricular diastolic dysfunction and relation to cardiovascular risk burden // Am. J. Cardiol. – 2002. – Vol. 90. – p. 1284-9.
90. Tsang T.S., Barnes M.E., Gersh B.J., et al. Prediction of risk for first age-related cardiovascular events in an elderly population: the incremental value of echocardiography // J. Am. Coll. Cardiol. – 2003. – Vol. 42. – p. 1199-205.
91. Kizer J.R., Bella J.N., Palmieri V., et al. Left atrial diameter as an independent predictor of first clinical cardiovascular events in middle-aged and elderly adults: the strong heart study // Am // Heart. J. In press. – 2005.
92. Simek C.L., Feldman M.D., Haber H.L., et al. Relationship between left ventricular wall thickness and left atrial size: comparison with other measures of diastolic function // J. Am. Soc. Echocardiogr. – 1995. – Vol. 8. – p. 37-47.
93. Appleton C.P., Galloway J.M., Gonzalez M.S., et al. Estimation of left ventricular filling pressures using two-dimensional and Doppler echocardiography in adult patients with cardiac disease: additional value of analyzing left atrial size, left atrial ejection fraction and the difference in duration of pulmonary venous and mitral flow velocity at atrial contraction // J. Am. Coll. Cardiol. – 1993. – Vol. 22. – p. 1972-82.
94. Benjamin E.J., D’Agostino R.B., Belanger A.J., et al. Left atrial size and the risk of stroke and death: the Framingham heart study // Circulation. – 1995. – Vol. 92. – p. 835-41.
95. Bolca O., Akdemir O., Eren M., et al. Left atrial maximum volume is a recurrence predictor in lone atrial fibrillation: an acoustic quantification study // Jpn. Heart. J. – 2002. – Vol. 43. – p. 241-8.
96. Di Tullio M.R., Sacco R.L., Sciacca R.R., Homma S. Left atrial size and the risk of ischemic stroke in an ethnically mixed population // Stroke. – 1999. – Vol. 30. – p. 2019-24.
97. Flaker G.C., Fletcher K.A., Rothbart R.M., et al. Clinical and echocardiographic features of intermittent atrial fibrillation that predict recurrent atrial fibrillation: stroke prevention in atrial fibrillation (SPAF) investigators // Am. J. Cardiol. – 1995. – Vol. 76. – p. 355-8.
98. Tsang T.S., Barnes M.E., Bailey K.R., et al. Left atrial volume: important risk marker of incident atrial fibrillation in 1655 older men and women // Mayo Clin. Proc. – 2001. – Vol. 76. – p. 467-75.
99. Vaziri S.M., Larson M.G., Benjamin E.J., Levy D. Echocardiographic predictors of nonrheumatic atrial fibrillation: the Framingham heart study // Circulation. – 1994. – Vol. 89. – p. 724-30.
100. Barnes M.E., Miyasaka Y., Seward J.B., et al. Left atrial volume in the prediction of first ischemic stroke in an elderly cohort without atrial fibrillation // Mayo Clin. Proc. – 2004. – Vol. 79. – p. 1008-14.
101. Tsang T.S., Barnes M.E., Gersh B.J., et al. Risks for atrial fibrillation and congestive heart failure in patients ≥65 years of age with abnormal left ventricular diastolic relaxation // Am. J. Cardiol. – 2004. – Vol. 93. – p. 54-8.
102. Tsang T.S., Gersh B.J., Appleton C.P., et al. Left ventricular diastolic dysfunction as a predictor of the first diagnosed nonvalvular atrial fibrillation in 840 elderly men and women // J. Am. Coll. Cardiol. – 2002. – Vol. 40. – p. 1636-44.
103. Moller J.E., Hillis G.S., Oh J.K., et al. Left atrial volume: a powerful predictor of survival after acute myocardial infarction // Circulation. – 2003. – Vol. 107. – p. 2207-12.
104. Beinart R., Boyko V., Schwammenthal E., et al. Long-term prognostic significance of left atrial volume in acute myocardial infarction // J. Am. Coll. Cardiol. – 2004. – Vol. 44. – p. 327-34.
105. Modena M.G., Muia N., Sgura F.A., et al. Left atrial size is themajor predictor of cardiac death and overall clinical outcome in patients with dilated cardiomyopathy: a long-term follow-up study // Clin. Cardiol. – 1997. – Vol. 20. – p. 553-60.
106. Quinones M.A., Greenberg B.H., Kopelen H.A., et al. Echocardiographic predictors of clinical outcome in patients with left ventricular dysfunction enrolled in the SOLVD registry and trials: significance of left ventricular hypertrophy: studies of left ventricular dysfunction // J. Am. Coll. Cardiol. – 2000. – Vol. 35. – p. 1237-44.
107. Rossi A., Cicoira M., Zanolla L., et al. Determinants and prognostic value of left atrial volume in patients with dilated cardiomyopathy // J. Am. Coll. Cardiol. – 2002. – Vol. 40. – p. 1425.
108. Dini F.L., Cortigiani L., Baldini U., et al. Prognostic value of left atrial enlargement in patients with idiopathic dilated cardiomyopathy and ischemic cardiomyopathy // Am. J. Cardiol. – 2002. – Vol. 89. – p. 518-23.
109. Sabharwal N., Cemin R., Rajan K., et al. Usefulness of left atrial volume as a predictor of mortality in patients with ischemic cardiomyopathy // Am. J. Cardiol. – 2004. – Vol. 94. – p. 760-3.
110. Schabelman S., Schiller N.B., Silverman N.H., Ports T.A. Left atrial volume estimation by two-dimensional echocardiography // Catheter Cardiovasc. Diagn. – 1981. – Vol. 7. – p. 165-78.
111. Wade M.R., Chandraratna P.A., Reid C.L., et al. Accuracy of nondirected and directedM-mode echocardiography as an estimate of left atrial size // Am. J. Cardiol. – 1987. – Vol. 60. – p. 1208-11.
112. Lester S.J., Ryan E.W., Schiller N.B., Foster E. Best method in clinical practice and in research studies to determine left atrial size // Am. J. Cardiol. – 1999. – Vol. 84. – p. 829-32.
113. Loperfido F., Pennestri F., Digaetano A., et al. Assessment of left atrial dimensions by cross sectional echocardiography in patients withmitral valve disease // Br. Heart J. – 1983. – Vol. 50. – p. 570-8.
114. Pritchett A.M., Jacobsen S.J., Mahoney D.W., et al. Left atrial volume as an index of left atrial size: a population-based study // J. Am. Coll. Cardiol. – 2003. – Vol. 41. – p. 1036-43.
115. Kircher B., Abbott J.A., Pau S., et al. Left atrial volume determination by biplane two-dimensional echocardiography: validation by cine computed tomography // Am. Heart. J. – 1991. – Vol. 121. – p. 864-71.
116. Rodevan O., Bjornerheim R., Ljosland M., et al. Left atrial volumes assessed by three- and two-dimensional echocardiography compared to MRI estimates // Int. J. Card. Imaging. – 1999. – Vol. 15. – p. 397-410.
117. Vandenberg B.F., Weiss R.M., Kinzey J., et al. Comparison of left atrial volume by two-dimensional echocardiography and cine-computed tomography // Am. J. Cardiol. – 1995. – Vol. 75. – p. 754-7.
118. Khankirawatana B., Khankirawatana S., Porter T. How should left atrial size be reported? Comparative assessment with use of multiple echocardiographic methods // Am. Heart. J. – 2004. – Vol. 147. – p. 369-74.
119. Hiraishi S., DiSessa T.G., Jarmakani J.M., et al. Two-dimensional echocardiographic assessment of left atrial size in children // Am. J. Cardiol. – 1983. – Vol. 52. – p. 1249-57.
120. Jessurun E.R., van Hemel N.M., Kelder J.C., et al. The effect of maze operations on atrial volume // Ann. Thorac. Surg. – 2003. – Vol. 75. – p. 51-6.
121. Wang Y., Gutman J.M., Heilbron D., et al. Atrial volume in a normal adult population by two-dimensional echocardiography // Chest. – 1984. – Vol. 86. – p. 595-601.
122. Keller A.M., Gopal A.S., King D.L. Left and right atrial volume by freehand three-dimensional echocardiography: in vivo validation using magnetic resonance imaging // Eur. J. Echocardiogr. – 2000. – Vol. 1. – p. 55-65.
123. Khankirawatana B., Khankirawatana S., Lof J., Porter T.R. Left atrial volume determination by three-dimensional echocardiography reconstruction: validation and application of a simplified technique // J. Am. Soc. Echocardiogr. – 2002. – Vol. 15. – p. 1051-6.
124. Poutanen T., Ikonen A., Vainio P., et al. Left atrial volume assessed by transthoracic three-dimensional echocardiography and magnetic resonance imaging: dynamic changes during the heart cycle in children // Heart. – 2000. – Vol. 83. – p. 537-42.
125. Knutsen K.M., Stugaard M., Michelsen S., et al. M-mode echocardiographic findings in apparently healthy, non-athletic Norwegians aged 20-70 years: influence of age, sex and body surface area // J. Intern. Med. – 1989. – Vol. 225. – p. 111-5.
126. Pearlman J.D., Triulzi M.O., King M.E., et al. Left atrial dimensions in growth and development: normal limits for two-dimensional echocardiography // J. Am. Coll. Cardiol. – 1990. – Vol. 16. – p. 1168-74.
127. Gutman J., Wang Y.S., Wahr D, Schiller N.B. Normal left atrial function determined by 2-dimensional echocardiography // Am. J. Cardiol. – 1983. – Vol. 51. – p. 336-40.
128. Thomas L., Levett K., Boyd A., et al. Compensatory changes in atrial volumes with normal aging: is atrial enlargement inevitable? // J. Am. Coll. Cardiol. – 2002. – Vol. 40. – p. 1630-5.
129. Losi M.A., Betocchi S., Aversa M., et al. Determinants of atrial fibrillation development in patients with hypertrophic cardiomyopathy // Am. J. Cardiol. – 2004. – Vol. 94. – p. 895-900.
130. Schnittger I., Gordon E.P., Fitzgerald P.J., Popp R.L. Standardized intracardiacmeasurements of two-dimensional echocardiography // J. Am. Coll. Cardiol. – 1983. – Vol. 2. – p. 934-8.
131. DePace N.L., Ren J.F., Kotler M.N., et al. Two-dimensional echocardiographic determination of right atrial emptying volume: a noninvasive index in quantifying the degree of tricuspid regurgitation // Am. J. Cardiol. – 1983. – Vol. 52. – p. 525-9.
132. Kaplan J.D., Evans G.T. Jr., Foster E., et al. Evaluation of electrocardiographic criteria for right atrial enlargement by quantitative two-dimensional echocardiography // J. Am. Coll. Cardiol. – 1994. – Vol. 23. – p. 747-52.
133. Roman M.J., Devereux R.B., Kramer-Fox R., O’Loughlin J. Two-dimensional echocardiographic aortic root dimensions in normal children and adults // Am. J. Cardiol. – 1989. – Vol. 64. – p. 507-12.
134. Roman M.J., Devereux R.B., Niles N.W., et al. Aortic root dilatation as a cause of isolated, severe aortic regurgitation: prevalence, clinical and echocardiographic patterns, and relation to left ventricular hypertrophy and function. Ann. Intern. Med. – 1987. – Vol. 106. – p. 800-7.
135. Morrison D., Devereux R., Roman M.J. Association of aortic root dilation with aortic dissection: a case-control study // J. Am. Coll. Cardiol. – 2003. – p. 467A (abstr 861-3).
136. Kim M., Roman M.J., Cavallini M.C., et al. Effect of hypertension on aortic root size and prevalence of aortic regurgitation // Hypertension. – 1996. – Vol. 28. – p. 47-52.
137. Moreno F.L., Hagan A.D., Holmen J.R., et al. Evaluation of size and dynamics of the inferior vena cava as an index of right-sided cardiac function // Am. J. Cardiol. – 1984. – Vol. 53. – p. 579-85.
138. Kircher B.J., Himelman R.B., Schiller N.B. Noninvasive estimation of right atrial pressure from the inspiratory collapse of the inferior vena cava // Am. J. Cardiol. – 1990. – Vol. 66. – p. 493-6.
139. Goldhammer E., Mesnick N., Abinader E.G., et al. Dilated inferior vena cava: a common echocardiographic finding in highly trained elite athletes // J. Am. Soc. Echocardiogr. – 1999. – Vol. 12. – p. 988-93.
140. Jue J., Chung W., Schiller N.B. Does inferior vena cava size predict right atrial pressures in patients receiving mechanical ventilation? // J. Am. Soc. Echocardiogr. – 1992. – Vol. 5. – p. 613-9.
141. Bendjelid K., Romand J.A., Walder B., et al. Correlation between measured inferior vena cava diameter and right atrial pressure depends on the echocardiographic method used in patients who are mechanically ventilated // J // Am. Soc. Echocardiogr. – 2002. – Vol. 15. – p. 944-9.