 Мілтон Пакер протягом року працював над новаторською гіпотезою, яка пов’язує адипокіни та вісцеральне ожиріння із серцевою недостатністю зі збереженою фракцією викиду (СНзбФВ).
Мілтон Пакер протягом року працював над новаторською гіпотезою, яка пов’язує адипокіни та вісцеральне ожиріння із серцевою недостатністю зі збереженою фракцією викиду (СНзбФВ).
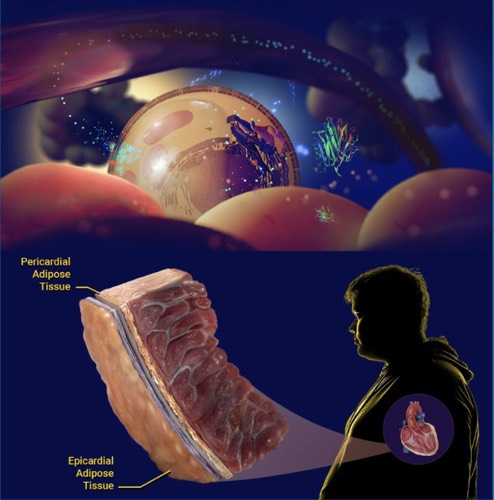
Гіпотеза пропонує єдину концептуальну модель, яка може радикально змінити те, як клініцисти розуміють і лікують СНзбФВ. У її основі лежить розуміння того, що СНзбФВ не є захворюванням кардіоміоцитів або результатом лише супутніх патологічних процесів. Натомість це захворювання дисфункціональної вісцеральної жирової тканини, яку тривалий час вважали лише резервуаром для зберігання тригліцеридів. Однак сьогодні добре відомо, що вісцеральний жир — той, що оточує внутрішні органи — є метаболічно активним ендокринним органом. Він секретує сигнальні молекули, тобто адипокіни, які передають біологічний стан жирової тканини до інших органів.
Пакер пояснює, що жирова тканина у худорлявої та здорової людини має кардіопротекторні, протизапальні та антифібротичні властивості. Однак зі збільшенням маси вісцеральної жирової тканини її біологія змінюється. Вона стає прозапальною, прогіпертрофічною, профібротичною та антинатрійуретичною. За його словами, серце є особливо чутливим до впливу цих адипокінів.
Дослідження показують, що підвищені рівні прозапальних адипокінів підвищують ризик розвитку СНзбФВ, посилюють тяжкість захворювання та пов’язані з гіршим прогнозом.
Згідно з цією гіпотезою, змінене середовище адипокінів пояснює основні риси СНзбФВ. Затримка натрію призводить до збільшення об’єму плазми. Системне та міокардіальне запалення сприяє коронарній мікросудинній дисфункції та фіброзу серця. Прогіпертрофічні сигнали стимулюють патологічне ремоделювання шлуночків.
Пакер поділяє адипокіни на три групи. До першої групи належать адипокіни з кардіопротекторною дією, такі як адипонектин, які захищають від запалення та фіброзу. До другої групи належать кардіопротекторні молекули, рівень яких підвищується при ожирінні як компенсаторна відповідь організму — спроба протидіяти шкоді, спричиненій вісцеральним жиром. До третьої групи належать прозапальні, прогіпертрофічні, профібротичні та антинатрійуретичні білки, секреція яких значно підвищується при ожирінні.
СНзбФВ виникає внаслідок дисбалансу, спричиненого ожирінням: збільшується рівень адипокінів третього типу, зменшується рівень адипокінів першого типу, а адипокіни другого типу не здатні повністю компенсувати цей дисбаланс.
Гіпотеза адипокінів ґрунтується на 12 взаємодоповнюючих лініях доказів. Серед них:
Ожиріння та СНзбФВ мають багато спільних молекулярних, патофізіологічних і клінічних характеристик, включаючи нейрогормональну активацію, затримку натрію, збільшення об’єму плазми, гіпертрофію серця та системне запалення.
Дослідження менделівської рандомізації демонструють зв’язок між вісцеральним ожирінням і СНзбФВ.
Зміни у вісцеральній жировій тканині та рівнях циркулюючих адипокінів спостерігаються за багато років до встановлення діагнозу, прогнозуючи розвиток СНзбФВ, але не СНзнФВ.
Від 85 до 95% пацієнтів із СНзбФВ мають абдомінальне ожиріння та надлишок вісцерального жиру.
Адипокіни мають доведений вплив на структуру та функцію серця, який може призводити до розвитку СНзбФВ. Дисбаланс адипокінів корелює з тяжкістю захворювання.
Баріатрична хірургія або медикаментозне лікування, що зменшують вісцеральний жир, одночасно підвищують рівень адипокінів першого типу та знижують рівень адипокінів третього типу.
Надлишкова жировa тканина також може допомогти визначити пацієнтів, які найбільш імовірно відповідають на сучасні методи лікування СНзбФВ.
Найпереконливіші докази на користь гіпотези отримані в експериментальних дослідженнях, які показують, що сигнальні молекули, які виділяються саме з жирової тканини, можуть викликати СНзбФВ.
Дієта з високим вмістом жиру сама по собі може спричиняти СНзбФВ у тваринних моделях, у яких жирова тканина секретує надзвичайно високі рівні прозапальних адипокінів. Однак якщо пригнічувати секрецію лише одного з таких адипокінів виключно в жировій тканині — але не в серці, нирках або інших органах — СНзбФВ не розвивається. Подібні експерименти були проведені щонайменше для семи різних адипокінів, що забезпечує причинний доказ того, що шкідливі молекулярні сигнали, які походять із дисфункціональної жирової тканини, можуть викликати СНзбФВ.
Гіпотеза адипокінів також допомагає пояснити, чому сучасні методи лікування СНзбФВ можуть бути ефективними. Інгібітори НЗКТГ2, антагоністи мінералокортикоїдних рецепторів і терапія на основі інкретинів можуть зменшувати масу вісцерального жиру та нормалізувати порушений біологічний стан жирової тканини.
Гіпотеза також допомагає пояснити, чому це захворювання частіше виникає у людей старшого віку та у жінок. За словами Пакера, з віком підшкірний жир перерозподіляється у вісцеральні жирові депо. Це явище особливо виражене у жінок після менопаузи.
Науковець також зазначає, що багато людей із ожирінням можуть мати недіагностовану СНзбФВ. Важливо, що зменшення вісцерального жиру до розвитку СНзбФВ потенційно може запобігти виникненню цього захворювання.
За словами Пакера, багато лікарів пояснюють задишку при фізичному навантаженні у людей із ожирінням лише високим індексом маси тіла. Через це такі пацієнти не проходять повного обстеження. Він підкреслює, що це неправильно, оскільки ці пацієнти заслуговують на діагностику, особливо з огляду на те, що сьогодні існують ефективні методи лікування СНзбФВ.
Зараз розробляються нові препарати — так звані модулятори адипокінів — для лікування СНзбФВ. Дослідник зазначає, що майже для кожного адипокіну, описаного у його роботі, вже створюються нові фармакологічні модифікатори. Перші результати виглядають обнадійливо, особливо для препаратів, які блокують активін А — ключовий прозапальний адипокін.
У спеціальному випуску JACC експерти представили план подальших досліджень для перевірки гіпотези адипокінів. Вони окреслили ключові питання та пріоритети досліджень, які мають допомогти краще зрозуміти патофізіологію СНзбФВ і вдосконалити її діагностику, лікування та, можливо, профілактику.
Спеціалісти зазначають, що сміливі гіпотези потребують ретельної перевірки. Роботу було опубліковано не тому, що вона є остаточно доведеною, а тому, що вона стимулює нові питання, створює структуровану основу для наукових досліджень і запрошує до критичного аналізу.
Хоча більшість авторів погоджуються, що дисфункціональна жирова тканина — особливо вісцеральний жир і сигнали адипокінів — є важливим чинником розвитку СНзбФВ , деякі підкреслюють, що це не єдиний механізм захворювання. Існують й інші патофізіологічні шляхи розвитку СНзбФВ, які не пов’язані з ожирінням, і їх також потрібно враховувати у майбутніх дослідженнях.
Експерти також наголошують на необхідності відмови від оцінки ризику лише за індексом маси тіла. Для більш точного визначення ризику слід використовувати окружність талії, кількісну оцінку вісцерального жиру, методи візуалізації та профілі біомаркерів.
Залишається багато невирішених питань, пов’язаних зі статевими відмінностями. Наприклад, чи відрізняються механізми дії адипокінів у чоловіків і жінок, як статеві гормони та репродуктивні зміни впливають на розвиток захворювання, і чому терапія зниження ваги дає різні результати щодо втрати маси тіла, але подібні клінічні результати щодо серцевої недостатності.
Також необхідні подальші трансляційні дослідження для перевірки причинних зв’язків між ожирінням, адипокінами та СНзбФВ, визначення біомаркерів і фенотипів пацієнтів, які найкраще відповідають на лікування.
Крім того, важливо проводити клінічні дослідження нових терапій, спрямованих на адипокіни, а також епідеміологічні дослідження СНзбФВ у худорлявих пацієнтів та в різних етнічних групах населення.
Літературні посилання знаходяться в редакції Webcardio.org