Склад
мультидисциплінарної робочої групи з опрацювання медико-технологічних
документів зі стандартизації медичної допомоги на засадах доказової медицини
пацієнтам із фібриляцією передсердь
|
Жарінов Олег Йосипович
|
завідувач кафедри кардіології та функціональної діагностики Національної медичної академії післядипломної освіти імені П.Л. Шупика МОЗ України, д.м.н., професор, головний позаштатний спеціаліст МОЗ України зі спеціальності «Функціональна діагностика»;
|
|
Талаєва Тетяна Володимирівна
|
в.о. Генерального директора Державного підприємства «Державний експертний центр МОЗ України», д.м.н., професор;
|
|
Ліщишина Олена Михайлівна
|
директор Департаменту стандартизації медичних послуг Державного підприємства «Державний експертний центр МОЗ України», cт.н.с., к.м.н.;
|
|
Божко Ляна Іванівна
|
заступник головного лікаря з медичної роботи, Київська міська станція швидкої медичної допомоги;
|
|
Гетьман Таїсія В’ячеславівна
|
старший науковий співробітник відділу аритмій серця Державної установи «Національний науковий центр «Інститут кардіології імені академіка М.Д. Стражеска» НАМН України», к.м.н.;
|
|
Залевський Валерій Павлович
|
завідувач відділення хірургії складних порушень серцевого ритму і електрокардіостимуляції з рентгенопераційною Державної установи «Національний інститут серцево-судинної хірургії імені М.М. Амосова НАМН України», д.м.н., професор;
|
|
Карпенко Юрій Іванович
|
завідувач кафедри внутрішньої медицини №1 з курсом серцево-судинної патології Одеського національного медичного університету, керівник Одеського регіонального центру кардіохірургії, д.м.н., професор;
|
|
Клименко Ліліана Вікторівна
|
асистент кафедри сімейної медицини та амбулаторно-поліклінічної допомоги Національної медичної академії післядипломної освіти імені П.Л. Шупика, к.м.н.;
|
|
Матюха Лариса Федорівна
|
завідувач кафедри сімейної медицини і амбулаторно-поліклінічної допомоги Національної медичної академії післядипломної освіти імені П.Л. Шупика, д.м.н., професор, головний позаштатний спеціаліст МОЗ України зі спеціальності «Загальна практика – сімейна медицина»;
|
|
Нетяженко Василь Захарович
|
завідувач кафедри пропедевтики внутрішніх хвороб № 1 Національного медичного університету імені О.О. Богомольця, член-кор. НАМН України, д.м.н., професор, головний позаштатний спеціаліст МОЗ України зі спеціальності «Терапія»;
|
|
Романова Олена Миколаївна
|
старший науковий співробітник відділу аритмій серця Державної установи «Національний науковий центр «Інститут кардіології імені академіка М.Д. Стражеска» НАМН України», к.м.н.;
|
|
Руденко Костянтин Володимирович
|
заступник головного лікаря Державної установи «Національний інститут серцево-судинної хірургії імені М.М. Амосова НАМН України», д.м.н., головний позаштатний спеціаліст МОЗ України зі спеціальності «Хірургія серця і магістральних судин у дорослих»;
|
|
Сичов Олег Сергійович
|
завідувач відділу аритмії серця, вчений секретар Державної установи «Національний науковий центр «Інститут кардіології імені академіка М.Д. Стражеска» НАМН України», головний спеціаліст НАМН України за спеціальністю «Функціональна діагностика», д.м.н., професор;
|
|
Стичинський Олександр Сергійович
|
завідувач відділення електрофізіології та рентгенхірургічного лікування серцевих аритмій Державної установи «Національний інститут серцево-судинної хірургії імені М.М. Амосова НАМН України», д.м.н., професор;
|
|
Хіміон Людмила Вікторівна
|
завідувач кафедри сімейної медицини Національної медичної академії післядипломної освіти ім. П.Л. Шупика;
|
|
Яблучанський Микола Іванович
|
завідувач кафедри внутрішньої медицини Харківського національного університету імені В.Н. Каразіна, д.м.н., професор;
|
|
Ягенський Андрій Володимирович
|
керівник Волинського обласного центру кардіоваскулярної патології, д.м.н., професор.
|
Методичний супровід та інформаційне забезпечення
|
Горох Євгеній Леонідович
|
начальник відділу якості медичної допомоги та інформаційних технологій Державного підприємства «Державний експертний центр МОЗ України», к.техн.н.;
|
|
Мельник Євгенія Олександрівна
|
начальник відділу доказової медицини Державного підприємства «Державний експертний центр МОЗ України»;
|
|
Шилкіна Олена Олександрівна
|
начальник відділу методичного забезпечення новітніх технологій у сфері охорони здоров’я Державного підприємства «Державний експертний центр МОЗ України».
|
Державний експертний центр МОЗ України є членом
Guidelines International Network
(Міжнародна мережа настанов)
|
|
|
ADAPTE (Франція)
(Міжнародний проект з адаптації клінічних
настанов)
|
|
Рецензенти:
|
Дзяк Георгій Вікторович
|
ректор Дніпропетровської медичної академії, д.м.н., професор, академік НАМН України;
|
|
Долженко Марина Миколаївна
|
завідувач кафедри кардіології Національної медичної академії післядипломної освіти імені П.Л. Шупика, д.м.н., професор.
|
Список скорочень
Синтез настанови
1. Передмова
2. Вступ............................................................................................................................... 5
2.1 Епідеміологія................................................................................................................ 6
2.1.1 Серцево-судинні наслідки, пов'язані з ФП («результати») ………………………………………..6
2.1.2 Серцево-судинні та інші стани, що асоціюються з ФП…………………………………….…..…..7
2.2 Механізми ФП……………………………………………………………………………….……..……9
2.2.1 Передсердні фактори………………………………………………………………………………….9
2.2.2 Електрофізіологічні механізми………………………………………………………………………10
2.2.3 Генетична схильність…………………………………………………………………………………11
2.2.4 Клінічні кореляції…………………………………………………………………………………….11
3. Діагностика, природний плин і лікування............................................................ ..13
3.1 Визначення.................................................................................................................. 13
3.2 Виявлення................................................................................................................... 13
3.3 Природний перебіг..................................................................................................... 14
3.4 ЕКГ методи діагностики та моніторування фібриляції передсердь........................ 15
3.5. Типи фібриляції передсердь...................................................................................... 16
3.6. Початкове ведення пацієнтів..................................................................................... 17
3.7 Спостереження........................................................................................................... 21
4. Лікування фібриляції передсердь............................................................................. 22
4.1 Антитромботична терапія.......................................................................................... 23
4.1.1 Стратифікація ризику інсульту і тромбоемболій …………………………………………………25
4.1.2 Антитромботична терапія…………………………………………………………………………..28
4.1.3 Сучасні рекомендації щодо антитромботичної терапії…………………………………………...31
4.1.4. Ризик кровотеч………………………………………………………………………………………34
4.1.5 Оптимальне міжнародне нормалізоване відношення …………………………………………….35
4.1.6 Особливі ситуації................................................................................................................................36
4.1.7 Кардіоверсія………………………………………………………………………………………….41
4.1.8 Нефармакологічні методи профілактики інсульту…………………………………………………49
4.2 Контроль частоти серцевих скорочень і ритму........................................................ 49
4.2.1 Контроль частоти серцевих скорочень і ритму під час гострої фази……………………………..49
4.3 Довготривала терапія................................................................................................. 58
4.3.1 Контроль ритму або частоти серцевих скорочень…………………………………………………59
4.3.2 Довготривалий контроль частоти шлуночкового ритму………………………………………….68
4.3.3 Медикаментозний контроль частоти шлуночкового ритму………………………………………69
4.3.4 Абляція і модифікація атріовентрикулярного вузла………………………………………………74
4.3.5 Довготривалий контроль ритму……………………………………………………………………76
4.4 Додаткова терапія..................................................................................................... 102
4.4.1 Інгібітори АПФ та блокатори рецепторів ангіотензину II.................................. 102
4.4.2 Антагоністи альдостерону…………………………………………………………………………..104
4.4.3 Статини……………………………………………………………………………………………….105
4.4.4. Поліненасичені жирні кислоти……………………………………………………………………106
5. Особливі групи.......................................................................................................... 107
5.1 Серцева недостатність............................................................................................. 107
5.2 Спортсмени............................................................................................................... 109
5.3 Вади клапанів серця................................................................................................. 111
5.4 Гострий коронарний синдром................................................................................. 111
5.5 Цукровий діабет....................................................................................................... 112
5.6 Літні люди................................................................................................................. 112
5.7 Вагітність.................................................................................................................. 113
5.8 Післяопераційна фібриляція передсердь................................................................. 115
5.9 Гіпертиреоз............................................................................................................... 118
5.10 Синдром Вольффа-Паркінсона-Уайта................................................................... 119
5.11 Гіпертрофічна кардіоміопатія................................................................................ 120
5.12 Захворювання легень.............................................................................................. 122
Список скорочень
|
АВК
|
Антагоніст вітаміну К
|
|
АЛТ
|
Аланінамінотрансфераза
|
|
АСТ
|
Аспартатамінотрансфераза
|
|
АТ
|
Артеріальний тиск
|
|
ВР
|
Відносний ризик
|
|
ГКС
|
Гострий коронарний синдром
|
|
ДІ
|
Довірчий інтервал
|
|
ЕКГ
|
Електрокардіографія
|
|
ІПП
|
Інгібітор протонної помпи
|
|
КН
|
Клінічна настанова
|
|
КТ
|
Комп'ютерна томографія
|
|
ЛП
|
Ліве передсердя
|
|
ЛШ
|
Лівий шлуночок
|
|
МНВ
|
Міжнародне нормалізоване відношення
|
|
НМГ
|
Низькомолекулярний гепарин;
|
|
НПАК
|
Нові пероральні антикоагулянти
|
|
НФГ
|
Нефракціонований гепарин
|
|
ПАК
|
Пероральний антикоагулянт
|
|
СБП
|
Стент без покриття
|
|
ТЕ-ЕхоКГ
|
Трансезофагеальна ехокардіографія
|
|
ТІА
|
Транзиторна ішемічна атака
|
|
ФП
|
Фібриляція передсердь
|
|
ЧКВ
|
Черезшкірне коронарне втручання
|
|
CHADS2
|
Індес [серцева недостатність, артеріальна гіпертонія, вік, цукровий діабет, інсульт (подвоєння ризику)]
|
|
EHRA
|
Європейська асоціація серцевого ритму
|
|
ESC
|
Європейське товариство кардіологів (European Society of Cardiology)
|
|
|
|
Синтез настанови
За прототип Адаптованої клінічної настанови «Фібриляція передсердь» взято клінічні настанови «Guidelines for the management of atrial fibrillation», ESC, 2010 та «2012 focused update of the ESC Guidelines for the management of atrial fibrillation», ESC, 2012.
Передмова робочої групи з адаптації клінічної настанови
за темою «Фібриляція передсердь»
Впродовж останніх десятиріч в усьому світі для забезпечення якості і ефективності медичної допомоги, для створення якісних клінічних протоколів (Clinical Pathway) та/або медичних стандартів як третинне джерело доказової медицини використовуються клінічні настанови (КН).
Клінічна настанова (Clinical practice guidelines) – це документ, що містить систематизовані положення стосовно медичної та медико-соціальної допомоги, розроблені з використанням методології доказової медицини на основі підтвердження їх надійності та доведеності, і має на меті надання допомоги лікарю і пацієнту в прийнятті раціонального рішення в різних клінічних ситуаціях.
Відповідно до положень наказу МОЗ України від 28.09.2012 р. № 751 «Про створення та впровадження медико-технологічних документів зі стандартизації медичної допомоги в системі Міністерства охорони здоров’я України», зареєстрованого в Міністерстві юстиції України 29.11.2012 р. за № 2001/22313, створення КН в Україні здійснюється шляхом адаптації вже існуючих клінічних настанов, що розроблені на засадах доказової медицини у відомих світових центрах. Клінічні настанови, що розроблені на науковій основі, мають основні ознаки, що відповідають назві, визначенню та змісту клінічних настанов, а саме:
• наявність переліку членів мультидисциплінарної робочої групи;
• наявність зовнішніх рецензентів;
• визначення дати перегляду клінічної настанови;
• наявність шкали рівнів доказів у клінічній настанові;
• список першоджерел літератури (статті за результатами рандомізованих клінічних досліджень, мета-аналізи, огляди літератури) тощо.
Адаптована клінічна настанова за темою «Фібриляція передсердь» створена мультидисциплінарною робочою групою МОЗ України на основі оригінальної Клінічної настанови ESC «Guidelines for the management of atrial fibrillation», 2010 року, яка була попередньо оцінена групою експертів за допомогою Опитувальника AGREE. Результати оцінки задокументовані і зберігаються у робочих матеріалах групи. Механізм адаптації передбачає внесення в оригінальний текст настанови, що залишається незмінним, Коментарів робочої групи, в яких відбивається можливість виконання тих чи інших положень КН в реальних умовах системи охорони здоров’я України, доступність медичних втручань, наявність зареєстрованих в Україні ліків, що зазначені у КН, відповідність нормативної бази щодо організаційних засад надання медичної допомоги тощо.
Запропонована адаптована клінічна настанова не повинна розцінюватись як стандарт медичного лікування. Дотримання положень КН не гарантує успішного лікування в кожному конкретному випадку, її не можна розглядати як посібник, що включає всі необхідні методи лікування або, навпаки, виключає інші. Остаточне рішення стосовно вибору конкретної клінічної процедури або плану лікування повинен приймати лікар з урахуванням клінічного стану пацієнта та можливостей для проведення заходів діагностики і лікування у медичному закладі. Адаптована клінічна настанова «Фібриляція передсердь», відповідно до свого визначення, має на меті надання допомоги лікарю і пацієнту в прийнятті раціонального рішення в різних клінічних ситуаціях, слугує інформаційною підтримкою щодо найкращої клінічної практики на основі доказів ефективності застосування певних медичних технологій, ліків та організаційних засад медичної допомоги.
Клінічна настанова – це рекомендаційний документ з найкращої медичної практики, заснованої на доказах ефективності, в першу чергу для практикуючих лікарів, які надають як первинну, так і спеціалізовану медичну допомогу.
На основі Адаптованої клінічної настанови «Фібриляція передсердь» робоча група розробила Уніфікований клінічний протокол медичної допомоги «Фібриляція передсердь», у якому використані доказові положення адаптованої клінічної настанови щодо ефективності медичних втручань, яка також слугувала основою для визначення індикаторів якості надання медичної допомоги пацієнтам з фібриляцією передсердь.
Представлена адаптована клінічна настанова має бути переглянута не пізніше 2018 р. мультидисциплінарною робочою групою за участю головного позаштатного спеціаліста МОЗ України, практикуючих лікарів, які надають первинну, вторинну та третинну медичну допомогу, науковців, організаторів охорони здоров’я, представників громадських організацій, які зацікавлені у підвищенні якості медичної допомоги, та ін.
1 Передмова
У рекомендаціях підсумовані всі наявні дані щодо лікування і профілактики фібриляції передсердь (ФП). Вони повинні допомогти лікарю при виборі оптимальної стратегії лікування з урахуванням його можливого впливу на результати, а також коефіцієнта користь / ризик методів діагностики і терапії.
Європейським товариством кардіологів (ESC) та іншими організаціями за останні роки опублікована велика кількість рекомендацій. Враховуючи їх вплив на клінічну практику, запропоновані правила розробки і критерії оцінки якості рекомендацій, які роблять прозорим процес прийняття рішень. Відповідну інформацію див. на сайті ESC (http://www.escardio.org/ knowledge/guidelines/rules). На першому етапі вибирають експертів у відповідній області, які проводять огляд та критичний аналіз опублікованих даних щодо лікування або профілактики того чи іншого стану (включаючи оцінку коефіцієнта користь / ризик). Якщо можливо, оцінюють результати для суспільства в цілому. Рівень доказів і силу доказів класифікують за спеціальними шкалами (табл. 1 і 2). Комітет ESC з практичних рекомендацій контролює і координує підготовку нових рекомендацій робочими групами, групами експертів або консультативними радами. Комітет несе також відповідальність за схвалення рекомендацій. Коли документ підготовлений і затверджений всіма членами робочої групи, він прямує на рецензію до зовнішніх фахівців. У подальшому документ редагується, остаточно затверджується комітетом з практичних рекомендацій і публікується.
Таблиця 1. Класи рекомендацій
|
Класи
|
Визначення
|
|
Клас I
|
За даними клінічних досліджень та / або на загальну думку, методи лікування або втручання корисні й ефективні
|
|
Клас II
|
Суперечливі дані та / або розбіжність думок з приводу користі / ефективності методу лікування або втручання
|
|
Клас IIa
|
Наявні дані свідчать на користь ефективності методу лікування або втручання
|
|
Клас IIb
|
Користь і ефективність методу лікування чи втручання встановлені менш переконливо
|
|
Клас III
|
За даними клінічних досліджень або спільної думки метод лікування або втручання марні / неефективні і в деяких випадках можуть бути шкідливими
|
Таблиця 2. Рівні доказів
|
Рівень А
|
Результати декількох рандомізованих клінічних досліджень або мета-аналізу
|
|
Рівень В
|
Результати одного рандомізованого клінічного дослідження або великих нерандомізованих досліджень
|
|
Рівень С
|
Загальна думка експертів та / або невеликі дослідження, ретроспективні дослідження, регістр
|
2 Вступ
Фібриляція передсердь (ФП) – це найпоширеніша стійка серцева аритмія, частота якої становить 1-2% загальної популяції. У Європі на ФП страждають більше 6 млн чоловік, а її поширеність принаймні подвоїться за наступні 50 років на тлі постаріння населення. Попередні рекомендації з лікування ФП були опубліковані 4 роки тому, у зв'язку з чим потрібна розробка нової версії рекомендацій.
ФП збільшує ризик інсульту в 5 разів, а кожен п'ятий інсульт розвивається на тлі цієї аритмії. У хворих на ФП ішемічний інсульт часто закінчується смертю, призводить до більш вираженої інвалідизації та рецидивує частіше, ніж у хворих на інсульт іншої природи. Відповідно, ризик смерті у хворих з інсультом, пов'язаним з ФП, збільшується в 2 рази, а витрати – в 1,5 рази. Питанню профілактики інсульту була присвячена велика кількість досліджень, що знайшло відображення в даних рекомендаціях.
У більшості пацієнтів ФП неухильно прогресує з розвитком персистуючої або постійної форм на тлі еволюції основного захворювання. Останнім часом досягнуті певні успіхи у вивченні природного перебігу ФП – від безсимптомних форм до незворотної важкої аритмії, яка асоціюється з розвитком серйозних серцево-судинних результатів. Були зроблені спроби уповільнити або зупинити прогресування ФП, яке може бути наслідком основного серцево-судинного захворювання або природного перебігу самої аритмії. Проте успіхи в цій області виявилися обмеженими.
Численні клінічні дослідження показали, що стратегія контролю синусового ритму не має переваг перед контролем частоти шлуночкового ритму. Більш суворий контроль частоти серцевих скорочень також не давав додаткового ефекту. Ці результати викликають розчарування з урахуванням тяжкості ускладнень ФП, які спостерігалися в епідеміологічних дослідженнях. Однак нові підходи до антиаритмічної терапії можуть призвести до поліпшення результатів лікування.
Проблему раннього розпізнавання ФП значно ускладнює часто прихований перебіг порушення ритму. Приблизно у третини пацієнтів ФП є безсимптомною. Більш рання діагностика аритмії дозволила б своєчасно призначити лікарські засоби, що дозволяють запобігти не тільки наслідкам аритмії, але і прогресуванню ФП з розвитком рефрактерної аритмії. Важливе значення можуть мати моніторування та скринінг, які пропонують проводити автори рекомендацій.
Впродовж останнього десятиліття активно розроблялися немедикаментозні втручання, спрямовані на профілактику розвитку ФП або її прогресування. Встановлено ефективність методів абляції, яку зазвичай проводять черезшкірно за допомогою катетера. Цей метод дає виражений симптоматичний ефект і дозволяє говорити про «лікування» деяких пацієнтів. Роль зазначених методів відображена в нових рекомендаціях. Їх застосування в поєднанні з новими лікарськими засобами, зокрема новими антитромботичними препаратами та більш безпечними антиаритміками, допоможе поліпшити результати у пацієнтів з ФП.
Відмінності систем організації медичної допомоги ускладнюють розробку рекомендацій, які могли б повністю виконуватися в різних країнах Європи. Ці відмінності можуть стосуватися доступності лікарських засобів, системи надання медичної допомоги та популяції пацієнтів. Відповідно, справжні європейські рекомендації, які підготовлені на підставі досліджень, що проводилися в різних країнах світу, можуть бути адаптовані з урахуванням реальної ситуації.
2.1 Епідеміологія
Поширеність ФП в загальній популяції становить 1-2%; цей показник, ймовірно, збільшиться у найближчі 50 років [1-2]. Систематичне моніторування ЕКГ дозволяє виявити ФП у кожного двадцятого пацієнта з гострим інсультом, тобто значно частіше, ніж стандартна ЕКГ у 12 відведеннях. ФП може тривало залишатися недіагностірованою (безсимптомна ФП) [3], а багато пацієнтів з ФП ніколи не госпіталізуються до стаціонару [4]. Відповідно, справжня поширеність ФП, швидше за все, наближається до 2% у загальній популяції [3].
Поширеність ФП збільшується з віком – від <0,5%, у віці 40-50 років до 5-15%, у віці 80 років [1-2, 5-7]. У чоловіків аритмія розвивається частіше, ніж у жінок. Довічний ризик розвитку ФП становить близько 25% після 40 років [8]. Поширеність і захворюваність ФП у представників не європеоїдної раси вивчені гірше. Захворюваність ФП, мабуть, збільшується (13% за останні 20 років).
2.1.1 Серцево-судинні наслідки, пов'язані з ФП («результати»)
ФП асоціюється зі збільшенням ризику смерті, інсульту та інших тромбоемболічних ускладнень, серцевої недостатності та госпіталізацій, погіршенням якості життя, зниженням переносимості фізичного навантаження і дисфункцією лівого шлуночка (ЛШ) (табл. 3).
Таблиця 3. Несприятливі наслідки ФП
|
Результати
|
Зміна ризику у пацієнтів з ФП
|
|
Смерть
|
Збільшення ризику смерті вдвічі
|
|
Інсульт (включаючи геморагічний інсульт і церебральна кровотеча)
|
Збільшення ризику інсульту і більш важкий його перебіг у пацієнтів з ФП
|
|
Госпітализації
|
Госпіталізації часто відмічаються у хворих з ФП і можуть сприяти погіршенню якості життя
|
|
Якість життя та переносимість фізичного навантаження
|
Варіабельні зміни (від відсутності змін до різкого погіршення). ФП супроводжується серцебиттям та іншими симптомами
|
|
Функція лівого шлуночка
|
Варіабельні зміни (від відсутності погіршення до тахікардіоміопатії з гострою серцевою недостатністю)
|
Смертність у хворих з ФП збільшується вдвічі незалежно від інших відомих предикторів смерті [3,9]. У клінічних дослідженнях тільки антитромботична терапія викликала зменшення смертності, пов'язаної з ФП [10].
Інсульт при ФП часто протікає важко і призводить до стійкої інвалідизаціі і смерті. Приблизно кожен п'ятий інсульт є наслідком ФП; більше того, недіагностована прихована ФП може виявитися причиною деяких випадків криптогенного інсульту [3,11]. Пароксизмальна ФП збільшує ризик інсульту в тій же мірі, що і персистуюча [12].
Частка госпіталізацій внаслідок ФП становить 1/3 серед усіх госпіталізацій з приводу порушень ритму серця. Основні причини госпіталізацій – гострий коронарний синдром (ГКС), декомпенсація серцевої недостатності, тромбоемболічні ускладнення і невідкладне лікування аритмії.
ФП може супроводжуватися когнітивною дисфункцією, включаючи судинну деменцію. Невеликі спостережні дослідження свідчать про те, що безсимптомні емболії можуть сприяти погіршенню когнітивної функції у хворих з ФП навіть за відсутності явного інсульту [11].
У хворих з ФП погіршується якість життя і знижується толерантність до фізичного навантаження. У пацієнтів з ФП якість життя значно гірша, ніж у здорових дорослих людей або пацієнтів з коронарною хворобою серця і синусовим ритмом [13].
При нерегулярних і частих скороченнях шлуночків, втрати систоли передсердь і збільшенні кінцевого діастолічного тиску ЛШ часто погіршується функція ЛШ. Контроль як ритму, так і частоти серцевих скорочень дозволяє поліпшити функцію ЛШ у хворих з ФП.
2.1.2 Серцево-судинні та інші стани, що асоціюються з ФП
ФП асоціюється з різними серцево-судинними станами [14,15], які сприяють збереженню аритмії (див. Розділ 2.2). Захворювання, що асоціюються з ФП, є скоріше маркерами загального серцево-судинного ризику та / або ураження серця, а не тільки етіологічними факторами.
Ризик розвитку ФП збільшується з віком, що, можливо, є наслідком вікової втрати та ізоляції міокарда передсердь і супутніх порушень провідності (див. Розділ 2.2).
Артеріальна гіпертонія – це фактор ризику розвитку вперше діагностованої ФП та її ускладнень, таких як інсульт та системні тромбоемболії.
Серцева недостатність II-IV функціонального класу за NYHA спостерігається у 30% хворих з ФП [14,15], а ФП – у 30-40% пацієнтів з серцевою недостатністю (залежно від причини і тяжкості порушення кровообігу). Серцева недостатність може бути наслідком ФП (тахікардіоміопатія або декомпенсація серцевої недостатності при гострому розвитку ФП) і причиною аритмії (внаслідок збільшення тиску в передсердях і перевантаження об'ємом, вторинної дисфункції клапанів і хронічної стимуляції нейрогуморальних систем).
Тахікардіоміопатію слід припускати, якщо дисфункція ЛШ визначається у пацієнтів з тахікардією при відсутності органічного захворювання серця. Діагноз підтверджується, якщо функція ЛШ нормалізується або поліпшується на тлі адекватного контролю частоти серцевих скорочень або відновлення синусового ритму.
Поразку клапанів серця виявляють приблизно у 30% пацієнтів з ФП [14,15]. ФП, пов'язана з розтягуванням лівого передсердя (ЛП) – це ранній прояв мітрального стенозу і / або регургітації. ФП розвивається також на більш пізніх стадіях вад аортального клапана. У минулому «ревматична ФП» зустрічалася часто, однак сьогодні в Європі її діагностують відносно рідко.
Кардіоміопатії, в тому числі первинні захворювання провідної системи серця [16], супроводжуються підвищенням ризику розвитку ФП, особливо у молодих людей. Відносно рідкісні кардіоміопатії діагностують у 10% пацієнтів з ФП [14,15]. У невеликої частини пацієнтів з «ізольованою» ФП експресуются мутації, що асоціюються з «електричними» кардіоміопатіями.
У «старих» епідеміологічних дослідженнях дефект міжпередсердної перегородки асоціювався з розвитком ФП у 10-15% хворих. Цей зв'язок має важливе клінічне значення, враховуючи необхідність антитромботичної терапії у пацієнтів з перенесеними інсультом або транзиторною ішемічною атакою (ТІА) і дефектом міжпередсердної перегородки.
Інші вроджені вади серця, підвищують ризик розвитку ФП, включають в себе єдиний шлуночок, операцію Mustard з приводу транспозиції великих артерій і операцію Фонтена.
На коронарну хворобу серця страждають принаймні 20% хворих з ФП [14,15]. Механізми розвитку ФП при неускладненій коронарній хворобі серця як такої (ішемія передсердь) і взаємодія між ФП і коронарною перфузією [17] не встановлені.
Порушення функції щитовидної залози може бути єдиною причиною ФП і привертає до розвитку її ускладнень. В останніх епідеміологічних дослідженнях гіпертиреоз або гіпотиреоз досить рідко діагностували у хворих на ФП [14,15], проте субклінічна тиреоїдна дисфункція також може давати внесок у її розвиток.
Ожиріння спостерігається у 25% хворих на ФП [15]. У великому німецькому регістрі середній індекс маси тіла у таких пацієнтів склав 27,5 кг / м2 (помірне ожиріння).
Цукровий діабет відзначається у 20% пацієнтів з ФП і може сприяти поразці передсердь. Хронічна обструктивна хвороба легень (ХОЗЛ) зустрічається у 10-15% пацієнтів з ФП і скоріше є маркером серцево-судинного ризику в цілому, а не специфічним фактором.
Апное під час сну, особливо в поєднанні з артеріальною гіпертонією, цукровим діабетом і органічним захворюванням серця, може бути патогенетичним фактором ФП, так як апное викликає збільшення тиску і розміру передсердь або зміни вегетативної системи.
Хронічна хвороба нирок відзначається у 10-15% пацієнтів з ФП. Ниркова недостатність підвищує ризик серцево-судинних ускладнень ФП, хоча результати контрольованих досліджень обмежені.
2.2 Механізми ФП
2.2.1 Передсердні фактори
Патофізіологічні зміни, що передують розвитку ФП
Будь-які органічні захворювання серця можуть викликати повільне, але прогресуюче структурне ремоделювання шлуночків і передсердь. У передсердях цей процес характеризується проліферацією і диференціюванням фібробластів в міофібробласти, підвищеним відкладенням сполучної тканини і фіброзом. Структурне ремоделювання призводить до електричної дисоціації м'язових пучків і неоднорідності проведення, які сприяють розвитку та збереженню ФП. Цей електро-анатомічний субстрат викликає появу множинних невеликих вогнищ циркуляції збудження, які стабілізують аритмію. Структурні зміни, що спостерігаються у пацієнтів з ФП, перераховані в табл. 4.
Таблиця 4. Структурні зміни, пов'язані з ФП
|
Зміни позаклітинного матриксу
Інтерстиціальний фіброз
Запалення
Відкладення амілоїду
Зміни міоцитів
Апоптоз
Некроз
Гіпертрофія
Порушення диференціювання
Накопичення субстрату в клітинах (гемохроматоз, глікогеноз)
Зміни мікросудин
Ремоделювання ендокарда (ендоміокардіальний фіброз)
|
Патофізіологічні зміни, що розвиваються внаслідок ФП
Після початку ФП в різний час відзначаються зміни електрофізіологічних властивостей, механічної функції та ультраструктури передсердь, які мають різні патофізіологічні наслідки [18]. У перші кілька днів після розвитку ФП відбувається вкорочення передсердного ефективного рефрактерного періоду [19]. Електричне ремоделювання сприяє збереженню ФП протягом перших днів після її початку. Основними клітинними механізмами, що лежать в основі укорочення рефрактерного періоду, є придушення струму іонів кальцію через канали L-типу і посилення надходження іонів калію в клітини. Рефрактерний період передсердь відновлюється протягом декількох днів після нормалізації синусового ритму.
Порушення скорочувальної функції передсердь також відбувається протягом декількох днів після розвитку ФП. Основними клітинними механізмами скорочувальної дисфункції вважають зниження надходження іонів кальцію в клітини, порушення виділення іонів кальцію з внутрішньоклітинних депо і порушення обміну енергії в міофібрилах.
У пацієнтів з «ізольованою» ФП були виявлені фіброз і запальні зміни [20].
2.2.2 Електрофізіологічні механізми
Для розвитку та збереження тахіаритмії необхідні тригер і субстрат. Ці механізми не є взаємовиключними і можуть поєднуватися один з одним.
Вогнищеві механізми
Велику увагу привертають до себе вогнищеві механізми, що лежать в основі розвитку і збереження ФП [21]. До клітинних механізмів вогнищевої активності відносять тригерну активність і циркуляцію збудження (re-entry). Важливу роль у розвитку передсердних тахіаритмій відіграють легеневі вени, тканина яких характеризується більш коротким рефрактерним періодом, а також швидкими змінами орієнтації міофібрил. Абляція вогнищ підвищеної активності, які найчастіше локалізуються в області з'єднання легеневих вен з лівим передсердям, призводить до наростаючого подовження тривалості циклу ФП і відновлення синусового ритму у пацієнтів з пароксизмальною ФП, в той час як у пацієнтів з персистуючою ФП вогнища підвищеної активності розподіляються по всіх передсердях, тому абляція або відновлення синусового ритму являють собою більш важке завдання.
Множинні дрібні хвилі
Відповідно до цієї гіпотези ФП зберігається внаслідок хаотичного проведення безлічі незалежних дрібних хвиль. Якщо число таких хвиль не знижується до критичного рівня, то аритмія зберігається. У більшості хворих з пароксизмальною ФП вдається виявити локальні джерела аритмії, в той час як у пацієнтів з персистуючою або постійною ФП подібні спроби часто виявляються безуспішними.
2.2.3 Генетична схильність
ФП, особливо розвивається в більш молодому віці, характеризується спадковою схильністю [22]. В останні роки були описані численні спадкові захворювання серця, що супроводжуються розвитком ФП. Надшлуночкові аритмії, включаючи ФП, можуть спостерігатися при синдромах короткого і подовженого інтервалу QT і синдромі Бругада [23]. ФП часто зустрічається при гіпертрофічній кардіоміопатії, сімейній формі синдрому передчасного збудження і гіпертрофії ЛШ, що асоціюється з мутаціями PRKAG гена. Інші сімейні форми ФП можуть спостерігатися при мутаціях гена, що кодує передсердний натрійуретичний пептид [24], мутаціях гена SCN5A, що асоціюють з порушенням функції натрієвих каналів серця [25], або мутаціях, що супроводжуються посиленням функції натрієвих каналів [26]. У великих дослідженнях кілька генетичних локусів в області PITX2 і ZFHX3 генів асоціювалися з розвитком ФП і кардіоемболічного інсульту [27]. Патофізологічна роль інших генетичних дефектів у розвитку та збереженні ФП не встановлена [23].
2.2.4 Клінічні кореляції
Атріовентрикулярне проведення
У пацієнтів з ФП та нормальною провідною системою (при відсутності додаткових провідних пучків або дисфункції волокон Гіса Пуркіньє) атріовентрикулярний вузол виступає в ролі фільтра, що перешкоджає значному збільшенню частоти шлуночкового ритму. Основними механізмами, що обмежують атріовентрикулярне проведення, є рефрактерність атріовентрикулярного вузла і приховане проведення. Електричні імпульси, що досягають атріовентрикулярного вузла, не завжди проводяться на шлуночки, але можуть змінювати рефрактерність атріовентрикулярного вузла, сповільнюючи або блокуючи наступні скорочення передсердь.
Зміни тонусу симпатичної і парасимпатичної систем визначають варіабельність частоти шлуночкового ритму протягом дня або при фізичному навантаженні. Висока варіабельність шлуночкового ритму часто насилу піддається лікуванню. Серцеві глікозиди, що уповільнюють серцевий ритм внаслідок збільшення тонусу парасимпатичної системи, ефективно контролюють частоту серцевих скорочень у спокої, але в меншій мірі зменшують її під час навантаження. Бета-адреноблокатори і недігідропіридинові антагоністи кальцію знижують частоту шлуночкового ритму в спокої і при навантаженні. У пацієнтів з синдромом передчасного збудження можуть розвинутися загрозливі для життя шлуночкові тахіаритмії. У пацієнтів з ФП і синдромом передчасного збудження застосування препаратів, які сповільнюють атріовентрикулярне проведення, але не збільшують рефрактерний період передсердь і додаткових провідних пучків (наприклад, верапаміл, дилтіазем і серцеві глікозиди), можуть прискорити проведення по додаткових пучках.
Гемодинамічні зміни
Фактори, що впливають на гемодинаміку у пацієнтів з ФП, включають відсутність скоординованих скорочень передсердь, високу частоту і нерегулярність шлуночкового ритму і зниження кровопостачання міокарда, а також стійкі зміни, такі як предсердну і шлуночкову кардіоміопатію.
Раптове порушення скоординованої механічної функції передсердь на тлі ФП призводить до зниження серцевого викиду на 5-15%. Цей ефект більш виражений у пацієнтів зі зниженою піддатливістю шлуночків, у яких скорочення передсердь робить значний внесок у наповнення шлуночків. Висока частота шлуночкового ритму супроводжується порушенням наповнення шлуночків внаслідок скорочення діастоли. Уповільнення міжшлуночкової або внутрішньошлуночкової провідності, залежне від частоти серцевих скорочень, може призвести до диссинхронії лівого шлуночка і додаткового зниження серцевого викиду.
Нерегулярний шлуночковий ритм також знижує серцевий викид. Коливання інтервалів RR викликають високу варіабельність сили подальших скорочень, що часто призводить до появи дефіциту пульсу.
Стійке збільшення частоти шлуночкового ритму більше 120-130 за хвилину може викликати розвиток шлуночкової тахікардіоміопатіі [28]. Зниження частоти серцевих скорочень дозволяє відновити нормальну функцію шлуночків і попередити подальші дилатацію і пошкодження передсердь.
Тромбоемболії
Ризик інсульту і системних емболій у хворих на ФП визначається різними патофізіологічними механізмами [29]. Порушення кровотоку при ФП характеризуються стазом крові в лівому передсерді, зниженням швидкості кровотоку у вушку лівого передсердя і наявністю спонтанних ехосигналів при черезхарчовій ехокардіографії. Зміни ендокарда включають наростаючу дилатацію передсердь, пошкодження ендокарда і набряк / фіброеластичну інфільтрацію позаклітинного матриксу. Вушко лівого передсердя є основним джерелом тромбоемболій (≥ 90%) у пацієнтів з неклапанною ФП [29]. Зміни крові, що відзначаються при ФП, добре відомі і включають активацію гемостазу і тромбоцитів, а також запалення і порушення факторів росту [29].
3. Діагностика, природний плин і лікування
3.1 Визначення
ФП – це серцева аритмія, яку діагностують на підставі наступних критеріїв:
(1) Абсолютно нерегулярні інтервали RR (відповідно, ФП іноді називають «абсолютною» аритмією), тобто інтервали RR не повторюються.
(2) Відсутність зубців Р на ЕКГ. У деяких відведеннях, найчастіше V1, іноді визначається електрична активність передсердь.
(3) Тривалість передсердного циклу (якщо визначається), тобто інтервал між двома збудженнями передсердь, зазвичай варіабельний і становить <200 мс (> 300 за хвилину).
Диференційний діагноз
Деякі надшлуночкові аритмії, насамперед передсердна тахікардія і тріпотіння передсердь, а також часта передсердна ектопія і навіть подвійне антиградне проведення через атріовентрикулярний вузол можуть характеризуватися частими нерегулярними інтервалами RR та імітувати ФП. У більшості пацієнтів з передсердною тахікардією та тріпотінням передсердь спостерігається подовжений передсердний цикл ≥200 мс. При лікуванні антиаритмічними препаратами відзначається збільшення тривалості передсердного циклу на тлі ФП.
Для диференційної діагностики ФП від інших рідкісних надшлуночкових аритмій з нерегулярними інтервалами необхідно зареєструвати ЕКГ під час аритмії. Будь-який епізод передбачуваної ФП слід зафіксувати на ЕКГ у 12 відведеннях, тривалість і якість якої повинні бути достатніми для оцінки передсердної активності. Іноді при частому шлуночковому ритмі блокада атріовентрикулярного вузла на тлі проби Вальсальви, масажу каротидного синуса або внутрішньовенного введення аденозину [30] дозволяє виявити предсердну активність.
3.2 Виявлення
При нерегулярному пульсі слід завжди підозрювати ФП, однак для підтвердження діагнозу необхідно зареєструвати ЕКГ. Якщо аритмія має характерні для ФП ознаки і зберігається досить довго, щоб зареєструвати ЕКГ у 12 відведеннях або протягом принаймні 30 с, діагностують ФП [3,31]. Частоту серцевих скорочень при ФП можна розрахувати на підставі стандартної ЕКГ у 12 відведеннях. Для цього множать число інтервалів RR протягом 10 с (при швидкості запису 25 мм / с) на 6.
Ризик ускладнень ФП не відрізняється при коротких епізодах аритмії і стійких її формах [12]. У зв'язку з цим важливо виявляти пароксизмальну ФП, щоб попередити несприятливі результати (наприклад, інсульт). Однак короткі епізоди передсердної тахікардії, виявлені за допомогою водія ритму, дефібрилятор або інші пристрої, що імплантуються, можуть не супроводжуватися підвищеним ризиком тромбоемболічних ускладнень, якщо їх тривалість не перевищує кілька годин (див. Розділ 3.4).
Першим проявом ФП можуть бути ішемічний інсульт або ТІА. Можна припустити, що у більшості пацієнтів розвитку явної ФП передують безсимптомні епізоди аритмії, які часто проходять самостійно.
Частота рецидивів ФП становить 10% протягом першого року після встановлення діагнозу і близько 5% на рік в подальшому. Супутні захворювання та вік значно прискорюють прогресування ФП і сприяють розвитку ускладнень [3,23].
3.3 Природний перебіг
ФП починається з коротких і рідкісних епізодів, які поступово стають більш тривалими і частими. З часом у багатьох пацієнтів розвиваються стійкі форми ФП (рис. 1). Пароксизмальна ФП зберігається протягом декількох десятиліть тільки у невеликої частини пацієнтів, у яких відсутні фактори, що сприяють прогресуванню ФП (див. Розділ 2.1.2) (2-3% пацієнтів) [32]. Рецидиви пароксизмальної ФП виникають групами [3]. Число епізодів аритмії може варіюватися в широких межах протягом місяців або навіть років [3]. У пацієнтів з клінічно явною ФП часто спостерігаються безсимптомні епізоди ФП незалежно від того, яким був перший епізод аритмії (персистуюча або пароксизмальна ФП). Це має важливе значення при обговоренні доцільності припинення або продовження терапії, спрямованої на профілактику ускладнень ФП.
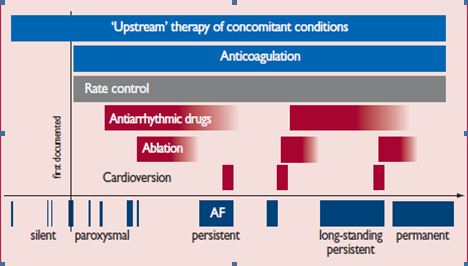
Рис. 1. Природний перебіг ФП
Темно-сині прямокутники ілюструють прогресування ФП (прихована – пароксизмальна – персистуюча – тривала персистуюча – постійна). Вище перераховані можливі підходи до лікування (лікування супутніх захворювань – антикоагуляція – контроль частоти серцевих скорочень – антиаритмічні засоби – абляція – кардіоверсія). Блакитним кольором виділені втручання, які володіють доведеною ефективністю у профілактиці «твердих кінцевих точок», таких як інсульт або гостра серцева недостатність, червоним кольором – методи лікування, які в даний час використовуються для купіювання симптомів, але можуть робити внесок у профілактику ускладнень ФП. Контроль частоти серцевих скорочень (виділений сірим кольором) має важливе значення для зменшення симптомів аритмії і може покращувати серцево-судинні наслідки.
3.4 ЕКГ методи діагностики та моніторування фібриляції передсердь
Інтенсивність і тривалість моніторування слід визначати з урахуванням важливості встановлення діагнозу та його впливу на тактику лікування. У клінічних дослідженнях ФП зазвичай виявляють більш активно, ніж в клінічній практиці [3,33].
Пацієнти із ймовірним, але невстановленим діагнозом ФП
Якщо передбачається наявність ФП, то в першу чергу слід зареєструвати ЕКГ у 12 відведеннях. Клінічні симптоми, такі як серцебиття і задишка, є підставою для моніторування ЕКГ з метою діагностики ФП та оцінки кореляції між симптомами і ритмом. Результати порівняння різних стратегій моніторування обмежені [3,34-37]. Більш активне і тривале моніторування обгрунтовано за наявності виражених симптомів [клас IV за класифікацією Європейської асоціації серцевого ритму (EHRA IV) [див. розділ 3.6], повторних непритомності і можливих показань до антикоагуляції (особливо після криптогенного інсульту) [34,38]. У частини пацієнтів можлива імплантація монітора без відведень для підтвердження діагнозу [39].
Пацієнти зі встановленим діагнозом ФП
Показання до моніторування ЕКГ відрізняються у пацієнтів зі встановленим і невстановленим діагнозом ФП. Якщо передбачаються аритмія або аритмогенні ефекти лікарських засобів, то слід проводити моніторування ЕКГ за допомогою холтерівського методу або зовнішніх моніторів. Якщо пацієнт отримує терапію, спрямовану на контроль ритму або частоти серцевих скорочень, а симптоми аритмії відсутні, то доцільно регулярно реєструвати ЕКГ у 12 відведеннях. У пацієнтів, які отримують антиаритмічну терапію, частота реєстрації ЕКГ у 12 відведеннях залежить від типу антиаритмічного препарату, можливих побічних ефектів, ускладнень і ризику аритмогенної дії.
Методи моніторування ЕКГ
Методи контролю електричної активності серця включають в себе стандартну ЕКГ, яку проводять в плановому порядку або при появі симптомів, холтерівське моніторування ЕКГ (від 24 год до 7 днів), передачу ЕКГ телефоном, зовнішні монітори. Якщо ФП визначається на момент реєстрації, то для підтвердження діагнозу досить стандартної ЕКГ. При пароксизмальній ФП показано моніторування ЕКГ. Холтерівське моніторування протягом 7 днів, щоденна реєстрація ЕКГ або реєстрація ЕКГ при появі симптомів дозволяють виявити аритмію приблизно в 70% випадків; негативні результати досліджень дозволяють передбачити відсутність ФП з точністю 30-50% [3]. У хворих, що перенесли інсульт, обстеження за ступеневою схемою (реєстрація ЕКГ 5 разів на день, холтерівське моніторування ЕКГ протягом доби, а потім 7 днів) дозволяє підвищити частоту діагностики ФП [34].
Методи безперервного моніторування ЕКГ
Імплантуються пристрої, що реєструють електричну активність передсердь, такі як двокамерні водії ритму і дефібрилятори, дозволяють виявити ФП, особливо якщо критерієм діагностики є аритмія тривалістю ≥ 5 хвилин. Більш тривалі епізоди збільшення активності передсердь (наприклад, близько 5,5 год) можуть супроводжуватися тромбоемболічними ускладненнями [35,36]. Імплантуються петльові монітори без відведень дозволяють безперервно контролювати ЕКГ протягом більше 2-х років. Діагностика ФП проводиться автоматично на підставі аналізу інтервалів RR. Попередні результати клінічних досліджень показали високу чутливість, але меншу специфічність діагнозу ФП [40]. Роль подібних пристроїв у звичайній клінічній практиці не встановлена.
3.5. Типи фібриляції передсердь
З урахуванням перебігу і тривалості аритмії виділяють 5 типів ФП: вперше виявлена, пароксизмальна, персистуюча, тривала персистуюча і постійна (рис. 1).
(1) Будь-який перший епізод ФП вважають вперше виявленою ФП незалежно від тривалості і тяжкості симптомів.
(2) При пароксизмальній ФП синусовий ритм відновлюється самостійно зазвичай протягом 48 год. Хоча пароксизми ФП можуть тривати до 7 днів, ключове значення має зазначений термін. Більш ніж через 48 год ймовірність спонтанної кардіоверсії низька, тому необхідно обговорити можливість антикоагуляції (див. Розділ 4.1).
(3) При персистуючій ФП тривалість епізоду ФП перевищує 7 днів або необхідна медикаментозна або електрична кардіоверсія.
(4) Діагноз тривалої персистуючої ФП встановлюють, якщо персистуюча ФП триває протягом ≥ 1 року і обрана стратегія контролю ритму.
(5) Постійну ФП діагностують у тих випадках, коли пацієнт і лікар вважають можливим збереження аритмії. Відповідно, кардіоверсія у таких пацієнтів за визначенням не проводиться. Якщо передбачається відновлення ритму, то аритмію називають «тривалою персистуючою ФП».
Ця класифікація має значення для вибору тактики ведення пацієнтів з ФП (рис. 2), особливо якщо одночасно враховуються симптоми аритмії, а також додаткові індивідуальні чинники і супутні захворювання. Першим проявом прихованої ФП (безсимптомної) можуть бути ускладнення ФП (ішемічний інсульт або тахікардіоміопатія). Безсимптомні епізоди ФП спостерігаються при будь-якій формі аритмії.
Коментар робочої групи:
Неклапанна ФП – це ФП за відсутності ревматичного мітрального стенозу, механічного або біопротезу серцевого клапана або пластики мітрального клапана.
3.6. Початкове ведення пацієнтів
Якщо передбачається або встановлено діагноз ФП, слід ретельно зібрати медичний анамнез (табл. 5). У гостру фазу необхідно, в першу чергу, купіювати симптоми та оцінити ризик, пов'язаний з ФП. Доцільно визначити індекс EHRA (табл. 6), оцінити ризик інсульту (див. Розділ 4.1) і наявність захворювань, що призводять до розвитку ФП (див. Розділ 2.1.2) і ускладнень аритмії (див. Розділ 2.1.1). При аналізі ЕКГ у 12 відведеннях слід звертати увагу на ознаки органічного захворювання серця (наприклад, гострий або перенесений інфаркт міокарда, гіпертрофія лівого шлуночка, блокада ніжки пучка Гіса або синдром передчасного збудження шлуночків, прояви кардіоміопатії або ішемії).
Таблиця 5. Питання, які слід задавати пацієнту із ймовірним або встановленим діагнозом ФП
|
Яким є серцевий ритм при нападі ФП – регулярним чи нерегулярним?
|
|
Які чинники провокують розвиток ФП, наприклад, фізичні навантаження, емоційне напруження або прийом алкоголю?
|
|
Чи відчуваєте Ви помірні або виражені симптоми при епізодах ФП (тяжкість можна оцінити за допомогою індексу EHRA [3], який схожий з індексом CCS-SAF [41]
|
|
Чи виникають напади часто або рідко? Вони тривалі або короткі?
|
|
Чи страждаєте Ви на інші захворювання, такі як артеріальна гіпертонія, коронарна хвороба серця, серцева недостатність, захворювання периферичних артерій, цереброваскулярна хвороба, інсульт, цукровий діабет або хронічне захворювання легенів?
|
|
Чи зловживаєте Ви алкоголем?
|
|
Чи немає у Вас родичів, які страждали ФП?
|
CCS-SAF – Сanadian Cardiovascular Society Severity in Atrial Fibrillation; EHRA – European Heart Rhythm Association
Таблиця 6. Індекс симптомів ФП (EHRA)
|
Клас EHRA
|
Прояви
|
|
I
|
Симптомів немає
|
|
II
|
Легкі симптоми; звичайна життєдіяльність не порушена
|
|
III
|
Виражені симптоми; змінена повсякденна активність
|
|
IV
|
Інвалідизуючі симптоми; нормальна повсякденна активність неможлива
|
EHRA – Европейська асоціація серцевого ритму
Діагностичне обстеження
Нещодавно запропонований індекс симптомів EHRA [3] (табл. 6) – це зручний метод оцінки симптомів ФП. Дуже схожа шкала була розроблена Канадським товариством серцево-судинних хвороб [41]. Індекс EHRA передбачає аналіз тільки симптомів, які пов'язані з ФП або проходять або зменшуються після відновлення синусового ритму або ефективного контролю частоти серцевих скорочень.
План початкового діагностичного обстеження залежить від клінічної картини аритмії. Щоб визначити тип ФП, необхідно з'ясувати, коли розвинувся епізод аритмії (рис. 2). У більшості пацієнтів з ФП тривалістю менше 48 год можлива кардіоверсія (див. Розділ 4.1.7) на фоні введення низькомолекулярного гепарину. При цьому ризик інсульту не збільшується. Якщо ФП зберігається більше 48 год або тривалість її не відома, то перед кардіоверсією слід провести черезстравохідну ехокардіографію, щоб виключити внутрішньосерцевий тромб [42], хоча застосування цього методу може виявитися скрутним при наявності гострого дистресу або неможливим у невідкладних ситуаціях. Трансторакальна ехокардіографія дозволяє отримати важливу інформацію, яка допомагає вибрати тактику ведення, однак вона не дає можливість виключити наявність тромбу у вушку лівого передсердя. У пацієнтів з ФП та ознаками гострої серцевої недостатності необхідно терміново добитися уповільнення ритму; в таких випадках часто потрібно кардіоверсія. При порушенні гемодинаміки слід швидко провести ехокардіографію, щоб оцінити функцію лівого шлуночка і клапанів і тиск у правому шлуночку.
План початкового діагностичного обстеження залежить від клінічної картини аритмії. Щоб визначити тип ФП, необхідно з'ясувати, коли розвинувся епізод аритмії (рис. 2). У більшості пацієнтів з ФП тривалістю менше 48 год можлива кардіоверсія (див. Розділ 4.1.7) на фоні введення низькомолекулярного гепарину. При цьому ризик інсульту не збільшується. Якщо ФП зберігається більше 48 год або тривалість її не відома, то перед кардіоверсією слід провести черезстравохідну ехокардіографію, щоб виключити внутрішньосерцевий тромб [42], хоча застосування цього методу може виявитися скрутним при наявності гострого дистресу або неможливим у невідкладних ситуаціях. Трансторакальна ехокардіографія дозволяє отримати важливу інформацію, яка допомагає вибрати тактику ведення, однак вона не дає можливості виключити наявність тромбу у вушку лівого передсердя. У пацієнтів з ФП та ознаками гострої серцевої недостатності необхідно терміново добитися уповільнення ритму; в таких випадках часто потрібна кардіоверсія. При порушенні гемодинаміки слід швидко провести ехокардіографію, щоб оцінити функцію лівого шлуночка і клапанів і тиск у правому шлуночку.
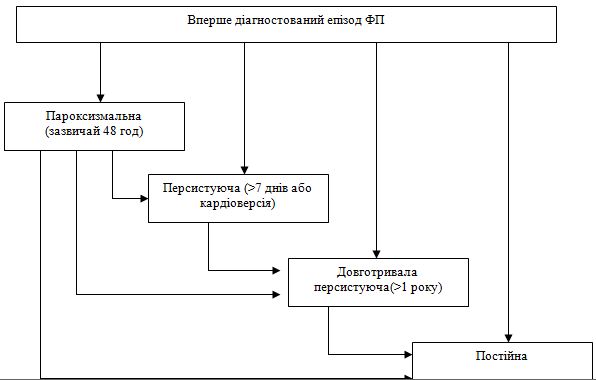
Рис. 2. Різні типи ФП. Аритмія має тенденцію до персистування від пароксизмальної (проходить самостійно зазвичай протягом 48 год) до персистуючої (самостійно не проходить або потрібна кардіоверсія), тривалої персистуючої (зберігається більше 1 року) і в кінцевому випадку постійної форми. Вперше виявлена ФП може бути першим нападом аритмії або проявом постійної форми ФП.
У пацієнтів з інсультом або ТІА слід негайно підтвердити діагноз; для цього зазвичай використовують комп'ютерну томографію (КТ). При порушенні мозкового кровообігу показана адекватна реваскуляризация церебральних судин. У пацієнтів з ФП доцільно оцінювати ризик інсульту. Більшості хворих з гострим епізодом ФП проводиться антикоагуляція за винятком тих випадків, коли ризик тромбоемболічних ускладнень низький (відсутні фактори ризику інсульту) і немає показань до кардіоверсії (наприклад, якщо ритм відновлюється протягом 24-48 год).
На наступному етапі необхідно з'ясувати причини ФП. Ехокардіографія дозволяє виявити ураження шлуночків, клапанів і передсердь, а також рідкісні вроджені вади серця. Визначають функцію щитовидної залози (зазвичай вимірюють сироватковий рівень тиреотропного гормону), проводять розгорнутий загальний аналіз крові, визначають рівень креатиніну в сироватці і білок у сечі, АТ, глюкозу крові натще. У частині випадків доцільно провести печінкові проби. Проба з навантаженням обгрунтована у пацієнтів з ознаками або факторами ризику коронарної хвороби серця. При збереженні дисфункції ЛШ і/або наявності ознак ішемії міокарда пацієнти є кандидатами на коронарну ангіографію.
3.7 Спостереження
Спеціаліст повинен не тільки провести початкове обстеження пацієнта з ФП і призначити адекватне лікування, але і запропонувати структурований план спостереження. У процесі спостереження слід враховувати наступні факти:
• Чи змінився профіль факторів ризику (наприклад, діагностовані цукровий діабет або артеріальна гіпертонія), особливо з точки зору доцільності антикоагуляції?
• Чи показана антикоагуляція – з'явилися нові фактори ризику або, навпаки, необхідність в антикоагулянтній терапії відпала, наприклад, після кардіоверсії у пацієнтів з низьким ризиком тромбоемболічних ускладнень?
• Чи зменшилися симптоми на фоні терапії; якщо ні, то чи слід призначити інші засоби?
• Чи є ознаки або підвищений ризик аритмогенної дії; якщо так, чи слід знизити дозу антиаритмічного препарату або замінити його на інший засіб?
• Чи перейшла пароксизмальна ФП в персистуючу / постійну форму незважаючи на антиаритмічну терапію; якщо так, чи слід змінити її?
• Наскільки адекватний контроль частоти шлуночкового ритму, чи досягнута цільова частота серцевих скорочень у спокої і при навантаженні?
У динаміці слід реєструвати ЕКГ у 12 відведеннях, щоб документувати ритм і частоту серцевих скорочень і виключити прогресування захворювання. Якщо проводиться антиаритмічна терапія, слід звертати увагу на провісники аритмогенної дії, такі як подовження інтервалів PR, QRS або QT, нестійка шлуночкова тахікардія або паузи. При наростанні симптомів проводять повторні аналізи крові, тривале моніторування ЕКГ та ехокардіографію.
Пацієнта слід інформувати щодо переваг і недоліків різних підходів до лікування, включаючи антикоагуляцію, засобів, уповільнюючих ритм, антиаритмічних препаратів або інвазивних втручань. Пацієнти з ізольованою або ідіопатичною ФП повинні знати, що за відсутності серцево-судинного захворювання прогноз сприятливий.
Рекомендації щодо діагностики і початкового лікування
|
Рекомендації
|
Клас
|
Рівень
|
Джерело
|
|
Наявність ФП необхідно підтвердити за допомогою ЕКГ
|
I
|
B
|
3,31
|
|
У пацієнтів з імовірним діагнозом ФП необхідно спробувати зареєструвати ЕКГ за появи відповідних симптомів
|
I
|
B
|
3,31
|
|
Для кількісної оцінки симптомів ФП рекомендується використовувати простий індекс (EHRA)
|
I
|
B
|
3,41
|
|
Всім хворим з ФП слід проводити ретельне фізичне обстеження. Рекомендується зібрати анамнез захворювання серця і аритмії
|
I
|
C
|
|
|
У хворих з важкими симптомами, документованим або передбачуваним захворюванням серця або серцево-судинними факторами ризику рекомендується провести ехокардіографію
|
I
|
B
|
3,23,44
|
|
У хворих, які отримують антиаритмічні засоби, рекомендується регулярно проводити ЕКГ у 12 відведеннях
|
I
|
C
|
|
|
Для підтвердження діагнозу ФП може знадобитися додаткове ЕКГ моніторування
|
IIa
|
B
|
3,33
|
|
Для діагностики прихованої ФП у пацієнтів з можливими ускладненнями аритміями може бути виконано моніторування ЕКГ
|
IIa
|
B
|
3,34
|
|
При застосуванні засобів, уповільнюючих ритм, у пацієнтів з ФП може проводитися холтерівське моніторування ЕКГ для оцінки ефективності контролю ритму і виявлення брадикардії
|
IIa
|
C
|
|
|
При застосуванні засобів, уповільнюючих ритм, у молодих і активних пацієнтів з ФП показана проба з фізичним навантаженням для оцінки ефективності контролю частоти серцевих скорочень
|
IIa
|
C
|
|
|
Хворим зі встановленим або ймовірним діагнозом ФП рекомендується провести ехокардіографію
|
IIa
|
C
|
|
|
Якщо ФП супроводжується симптомами або ускладненнями, пацієнта слід направити на консультацію до кардіолога
|
IIa
|
C
|
|
|
Спеціаліст повинен розробити структурований план спостереження за пацієнтом для лікаря загальної практики
|
IIa
|
C
|
|
|
У пацієнтів, які отримують антиаритмічні засоби, рекомендується регулярно контролювати ЕКГ для оцінки ефективності лікування
|
IIb
|
B
|
3,45,46
|
|
У більшості пацієнтів з ФП обгрунтована консультація фахівця з регулярними інтервалами
|
IIb
|
C
|
|
4. Лікування фібриляції передсердь
Цілі лікування ФП – купіювання симптомів та профілактика тяжких ускладнень. Цих цілей слід добиватися паралельно, особливо при вперше виявленій ФП. Методи профілактики ускладнень включають антитромботичну терапію, контроль частоти шлуночкового ритму і адекватне лікування супутніх захворювань серця. Ці методи лікування самі по собі дають симптоматичний ефект, проте для купіювання симптомів можуть знадобитися кардіоверсія, антиаритмічна терапія або абляция (рис. 3).
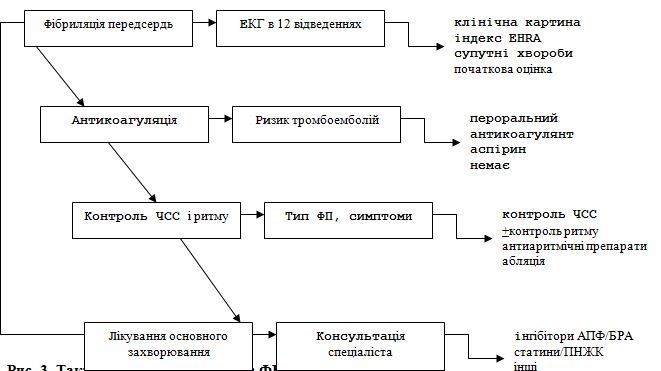
Рис. 3. Тактика ведення пацієнтів з ФП
Коментар робочої групи:
Аспірин – торгова назва, міжнародна непатентована назва - ацетилсаліцилова кислота.
4.1 Антитромботична терапія
Когортні дослідження, а також результати спостереження за пацієнтами контрольних груп в клінічних дослідженнях варфарину дозволили встановити клінічні та ехокардіографічні фактори ризику інсульту у хворих з ФП [47,48]. Однак багато інших можливостей факторів ризику систематично не вивчалися. Нещодавно в двох систематизованих оглядах були вивчені фактори ризику інсульту у хворих з ФП [47,48]. Був зроблений висновок, що перенесені інсульт / ТІА / тромбоемболії, вік, артеріальна гіпертонія, цукровий діабет та органічне ураження серця є важливими факторами ризику. За даними багатофакторного аналізу, наявність помірної або важкої систолічної дисфункції ЛШ була єдиним незалежним ехокардіографічним фактором ризику інсульту. Незалежними предикторами інсульту і тромбоемболій при черезстравохідній ехокардіографії є тромб у лівому передсерді (відносний ризик [ВР] 2,5; р = 0,04), бляшки в аорті (ВР 2,1; p <0,001), спонтанні ехосигнали (ВР 3,7; p <0,001) і низька швидкість кровотоку у вушку лівого передсердя (≤20 см/с; ВР 1,7; p <0,01). У пацієнтів з пароксизмальною ФП ризик інсульту такий же, як у пацієнтів з персистуючою або постійною ФП (за наявності факторів ризику).
У пацієнтів віком <60 років з ізольованою ФП (тобто за відсутності клінічних або ехокардіографічних ознак серцево-судинного захворювання) кумулятивний ризик інсульту дуже низький і становить 1,3% протягом 15 років. У молодих людей з ізольованою ФП ймовірність інсульту збільшується з віком або на тлі розвитку артеріальної гіпертонії, що вказує на важливість періодичної переоцінки факторів ризику інсульту.
Невідповідності
У деяких дослідженнях супутня терапія аспірином впливала на частоту тромбоемболічних ускладнень. Слід зазначити, що частота інсульту зазвичай знижувалася. Ризик його нижче при моніторуванні антикоагуляції у пацієнтів, які отримують антагоністи вітаміну К. У найближчому майбутньому можуть знайти застосування нові пероральні антикоагулянти, ефект яких не потребує моніторування.
Роль факторів ризику з часом може змінюватися. Наприклад, ризик інсульту у хворих з ФП починає збільшуватися після 65 років. У пацієнтів віком ≥75 років (навіть за відсутності інших факторів ризику) є високий ризик розвитку інсульту, а антагоністи вітаміну К щодо ефективності перевершують аспірин [47,48]. З віком у пацієнтів з ФП відносна ефективність антитромбоцитарної терапії в профілактиці ішемічного інсульту знижується, а ефективність антагоністів вітаміну К не змінюється. Таким чином, абсолютна користь останніх у профілактиці інсульту у пацієнтів з ФП з віком збільшується, що підтверджується даними, отриманими клінічною практикою.
У старих дослідженнях критеріями діагностики артеріальної гіпертонії зазвичай служили АТ> 160/95 мм рт. ст. без лікування або застосування антигіпертензивних засобів. У пацієнтів з адекватно контрольованою гіпертонією ризик інсульту і тромбоемболій може бути низьким. Крім того, у зазначених вище систематизованих оглядах клінічний діагноз серцевої недостатності не був постійним фактором ризику інсульту. Фактично цей діагноз не завжди відображає систолічну дисфункцію ЛШ. Хоча високий ризик тромбоемболій у пацієнтів з середньо-важкої або тяжкою систолічною дисфункцією ЛШ не викликає сумніву, наявність його у пацієнтів з серцевою недостатністю та збереженою фракцією викиду не доведене [44,47,48].
Атеросклероз може сприяти підвищенню ризику інсульту. Збільшення ризику інсульту і тромбоемболій у пацієнтів з інфарктом міокарда в анамнезі було відзначено в більшості (але не всіх) досліджень [49], однак діагноз "стенокардії» сам по собі не надійний, тому що у багатьох пацієнтів відсутня коронарна хвороба серця. Крім того, прогноз несприятливий при ФП у пацієнтів із захворюванням периферичних артерій, а бляшки в низхідній частині аорти (за даними черезстравохідної ехокардіографії) – це незалежний фактор ризику інсульту і тромбоемболій.
У жінок ВР тромбоемболій підвищений у 1,6 рази [95% довірчий інтервал (ДІ) 1,3-1,9]. Результати популяційних, когортних і контрольованих клінічних досліджень і опитувань вказують на більш високий ризик тромбоемболічних ускладнень у жінок.
За даними нещодавно проведеного аналізу, протеїнурія збільшує ризик тромбоемболій на 54% (ВР 1,54; 95% ДІ 1,29-1,85). Ризик інсульту вище при розрахунковій швидкості клубочкової фільтрації <45 мл/хв. Таким чином, хронічна хвороба нирок може асоціюватися з підвищеним ризиком тромбоемболій у хворих на ФП, хоча у таких пацієнтів одночасно вища смертність і ризик кровотеч. Ці пацієнти не вивчалися в проспективних контрольованих дослідженнях.
У пацієнтів з тиреотоксикозом можливий розвиток ФП, однак ризик інсульту більшою мірою відображає наявність асоційованих факторів ризику. Інші захворювання, такі як гіпертрофічна кардіоміопатія і амілоїдоз, можуть підвищувати ризик інсульту, проте вони спеціально не вивчалися, а таких пацієнтів не включали в дослідження тромбопрофілактики.
4.1.1 Стратифікація ризику інсульту і тромбоемболій
Ідентифікація клінічних факторів ризику інсульту призвела до розробки різних схем оцінки ризику його розвитку. У більшості випадків пацієнтів штучно розподіляли на групи високого, середнього та низького ризику. Найпростіший метод – це індекс CHADS2 [серцева недостатність, артеріальна гіпертонія, вік, цукровий діабет, інсульт (подвоєння ризику)] (табл. 7), який був запропонований на підставі результатів дослідження SPAF. При розрахунку індексу CHADS2 перенесеними інсульту або ТІА привласнюють 2 бали, а віком ≥ 75 років, артеріальної гіпертонії, цукрового діабету або серцевої недостатності – по 1 балу [50]. Індекс CHADS2 може застосовуватися для швидкої початкової оцінки ризику інсульту. Якщо індекс CHADS2 становить ≥ 2, показана постійна антикоагулянтна терапія антагоністами вітаміну К (цільове МНВ 2,5; діапазон 2,0-3,0) за відсутності протипоказань. Подібний підхід дозволяє поліпшити результати у хворих на ФП у звичайній клінічній практиці [10,51]. Як видно з табл. 7, є чіткий зв'язок між індексом CHADS2 і частотою інсульту [50]. Ризик інсульту вважають низьким, середнім і високим, якщо індекс CHADS2 становить 0, 1-2 і > 2, відповідно.
Таблиця 7. Індекс CHADS2 і частота інсульту
|
Індекс CHADS2
|
Число пацієнтів (n=1733)
|
Частота інсульта, % на ріка (95% довірчий інтервал
|
|
0
|
120
|
1.9 (1.2–3.0)
|
|
1
|
463
|
2.8 (2.0–3.8)
|
|
2
|
523
|
4.0 (3.1–5.1)
|
|
3
|
337
|
5.9 (4.6–7.3)
|
|
4
|
220
|
8.5 (6.3–11.1)
|
|
5
|
65
|
12.5 (8.2–17.5)
|
|
6
|
5
|
18.2 (10.5–27.4)
|
aСкоректовану частоту інсульту розраховували на підставі багатофакторного аналізу (припускали, що пацієнти не отримують аспірин) у госпіталізованих пацієнтів з ФП (публікація 2001). Низьке число пацієнтів з індексом CHADS2 5 і 6 не дозволяє точно оцінити ризик інсульту у таких хворих. Частота інсульту в популяції поступово знижується, тому фактичний ризик інсульту у амбулаторних пацієнтів може відрізнятися від розрахункових показників Gage BF et al. [50]
Робоча група «Stroke in AF» порівняла 12 опублікованих схем оцінки ризику у пацієнтів з неклапанною ФП. Був зроблений висновок про те, що існуючі схеми мають суттєві і клінічно значущі відмінності один від одного. Більшість з них характеризувалися помірною точністю в прогнозі інсульту (показник близько 0,6). Крім того, відсоток пацієнтів, які були віднесені до різних груп ризику за допомогою різних схем, варіювався в широких межах. На підставі індексу CHADS2 більшість пацієнтів були віднесені до категорії середнього ризику, а у всій когорті показник з склав 0,58.
Автори даних рекомендацій пропонують відмовитися від використання категорій низький, середній і високий ризик (враховуючи їх низьке пророкуюче значення) і вважають за доцільне розглядати ризик як континуум. Ми рекомендуємо проводити більш детальний аналіз факторів ризику інсульту і вирішувати питання щодо антитромботичної терапії на підставі їх наявності (або відсутності). Такий підхід обґрунтовується результатами опублікованих досліджень, в яких пероральні антикоагулянти мали перевагу перед аспірином навіть у пацієнтів з середнім ризиком (індекс CHADS2 = 1, тобто за наявності одного фактора ризику) і рідко викликали великі кровотечі. Важливо підкреслити, що застосування антитромбоцитарних препаратів не супроводжувалося зниженням ризику небажаних явищ. Крім того, індекс CHADS2 не включає в себе багато факторів ризику інсульту, а при всебічній оцінці ймовірності його розвитку слід враховувати інші фактори, що модифікують ризик (табл. 8).
Таблиця 8. Індекс CHA2DS2VASc і частота інсульту
|
(а) Фактори ризику інсульту і тромбоемболій у хворих з неклапанною ФП
|
|
Основні фактори ризику
|
Клінічно значущі неосновні фактори ризику
|
|
Інсульт, ТІА або системна емболія в анамнезі, вік ≥75 років
|
Серцева недостатність або помірна / виражена систолічна дисфункція лівого шлуночка (фракція викиду ≤40%), артеріальна гіпертонія, цукровий діабет, жіноча стать, вік 65-74 роки, вада клапана серцяа
|
|
(б) Розрахунок індексу ризику в балах (CHA2DS2VASc
|
|
Фактор ризику
|
Бали
|
|
Серцева недостатність/дисфункція ЛШ
Артеріальна гіпертонія
Вік ≥75 років
Цукровий діабет
Інсульт/ТІА/тромбоемболія
Захворювання судина
Вік 65-74 роки
Жіноча стать
Максимальне значення
|
1
1
2
1
2
1
1
1
9
|
|
(в) Індекс CHA2DSs-VASc і частота інсульту
|
|
Індекс CHA2DSs-VASc
|
Число пацієнтів (n=7329)
|
Частота інсульту, % на рікb
|
|
0
|
1
|
0%
|
|
1
|
422
|
1.3%
|
|
2
|
1230
|
2.2%
|
|
3
|
1730
|
3.2%
|
|
4
|
1718
|
4.0%
|
|
5
|
1159
|
6.7%
|
|
6
|
679
|
9.8%
|
|
7
|
294
|
9.6%
|
|
8
|
82
|
6.7%
|
|
9
|
14
|
15.2%
|
|
|
|
|
|
|
a Інфаркт міокарда в анамнезі, захворювання периферичних артерій, бляшка в аорті. Фактична частота інсульту в сучасних когортних дослідженнях може відрізнятися від розрахункових показників. b Lip et al. [53]
Фракція викиду, розрахована на підставі ехокардіографії, радіонуклідної вентрикулографії, катетеризації серця, магнітно-резонансної томографії та ін.
Коментра робочої групи:
Згідно з правками рекомендацій ESC 2012 року
|
(c) Розрахована частота інсульту в залежності від кількості балів за шкалою CHA2DS2-VASc
|
|
Кількість балів за шкалою CHA2DS2-VASc
|
Кількість пацієнтів (n = 73 538)
|
Розрахована частота інсульту (%/рік)b
|
|
0
|
6369
|
0,78%
|
|
1
|
8203
|
2,03%
|
|
2
|
12771
|
3,71%
|
|
3
|
17371
|
5,92%
|
|
4
|
13887
|
9,27%
|
|
5
|
8942
|
15,26%
|
|
6
|
4244
|
19,74%
|
|
7
|
1420
|
21,50%
|
|
8
|
285
|
22,38%
|
|
9
|
46
|
23,64%
|
Основні фактори ризику (раніше їх називали факторами високого ризику) є інсульт або ТІА в анамнезі, тромбоемболії і старечий вік (≥75 років). Наявність деяких вад клапанів серця (наприклад, мітрального стенозу або протезованого клапану серця) також вказує на високий ризик інсульту. Клінічно значимими неосновними факторами ризику (раніше називали факторами середнього ризику) є серцева недостатність (особливо помірна або тяжка систолічна дисфункція ЛШ, що характеризується зниженням фракції викиду ≤40%), артеріальна гіпертонія або цукровий діабет. До інших таких факторів ризику (раніше їх вважали менш валідними) відносять жіноча стать, вік 65-74 роки і захворювання судин (інфаркт міокарда, бляшка в аорті і захворювання периферичних судин). Фактори ризику є кумулятивними, тому за наявності принаймні двох клінічно значущих неосновних факторів ризику виправдана антикоагулянтна терапія.
Для позначення схеми оцінки ризику у пацієнтів з неклапанною ФП можна використовувати акронім CHA2DS2-VASc [застійна серцева недостатність, артеріальна гіпертонія, вік ≥75 років (вдвічі), цукровий діабет, інсульт (вдвічі), судинне захворювання, вік 65- 74 років і жіноча стать] [52]. При застосуванні цієї схеми 2 бали присвоюються інсульту і ТІА в анамнезі і віком ≥75 років, а по 1 балу – віком 65-74 роки, артеріальній гіпертонії, цукровому діабету, серцевій недостатності, судинним захворюванням (інфаркт міокарда, бляшка в аорті і захворювання периферичних артерій, включаючи реваскуляризацию, ампутацію або ангіографічні зміни) і жіночій статі (табл. 8). Таким чином, у порівнянні з індексом CHADS2 запропонована схема передбачає аналіз додаткових факторів ризику інсульту, які можуть вплинути на рішення про призначення антикоагулянтної терапії (див. Розділ 4.1.1).
4.1.2 Антитромботична терапія
Численні клінічні дослідження переконливо підтвердили ефективність антитромботичної терапії у хворих на ФП.
4.1.2.1 Антагоністи вітаміну К
У 5 великих рандомізованих дослідженнях, опублікованих з 1989 по 1992 рік, вивчали ефективність антагоністів вітаміну К в профілактиці емболій у пацієнтів з неклапанною ФП. У шостому дослідженні оцінювали їхню користь у вторинної профілактики у пацієнтів, які перенесли інсульт або ТІА. За даними мета-аналізу, лікування антагоністами вітаміну К призвело до високо достовірного зниження ВР на 64%, що відповідало абсолютному зниженню ризику будь-якого інсульту на 2,7% [54]. ВР ішемічного інсульту знизився на 67%. Цей ефект був порівнянним при проведенні первинної та вторинної профілактики як інвалідизуючого, так і неінвалідизуючого інсульту. Слід зазначити, що у хворих, які отримували антагоністи вітаміну К, інсульт у багатьох випадках розвивався, коли вони не приймали ці препарати або отримували їх у неадекватних дозах. Загальна смертність при лікуванні антагоністами вітаміну К також значно знизилася (на 26%) у порівнянні з контролем. Ризик розвитку внутрішньочерепних кровотеч був низьким.
Чотири дослідження були плацебо-контрольованими; одне подвійне сліпе дослідження було припинено достроково, враховуючи явну перевагу пероральних антикоагулянтів перед плацебо. В одному дослідженні не брали участі жінки. У трьох дослідженнях дози антагоністів вітаміну К підбирали з урахуванням протромбінового часу, а в двох дослідженнях – на підставі МНВ (цільовий діапазон 2,5-4,0 і 2,0-3,0).
На підставі результатів зазначених досліджень лікування антагоністами вітаміну К рекомендується пацієнтам з ФП, у яких є принаймні 1 фактор ризику інсульту і відсутні протипоказання. При обговоренні доцільності антикоагуляції слід ретельно оцінювати коефіцієнт користь / ризик і враховувати переваги пацієнтів.
4.1.2.2 Антитромбоцитарні препарати
У 8 незалежних рандомізованих контрольованих дослідженнях в цілому у 4876 пацієнтів вивчали ефективність антитромбоцитарних препаратів (найчастіше порівнювали аспірин з плацебо) у профілактиці тромбоемболій у хворих з ФП [54].
В 7 дослідженнях аспірин порівнювали з плацебо або відсутністю терапії. Лікування аспірином призвело до недостовірного зниження частоти інсульту на 19% (95% ДІ від -1% до -35%). При вивченні ефективності первинної та вторинної профілактики абсолютний ризик знизився на 0,8% за рік і на 2,5% за рік, відповідно [54]. Терапія аспірином супроводжувалася зниженням ризику інвалідизуючого інсульту на 13% (95% ДІ від -18% до -36%) і неінвалідизуючого інсульту на 29% (95% ДІ від -6% до -53%). Ризик ішемічного інсульту в групі аспірину знизився на 21% (95% ДІ від -1% до -38%). За даними мета-аналізу контрольованих досліджень всіх антитромбоцитарних засобів, їх застосування призвело до зниження ризику інсульту на 22% (95% ДІ від -6% до -35%).
Доза аспірину значно відрізнялася у різних дослідженнях (від 50 до 1300 мг / добу), проте їх результати були досить однорідними. Сприятливий ефект аспірину в значній мірі відображав результати дослідження SPAF-I, в якому лікування аспірином у дозі 325 мг призвело до зниження ризику інсульту на 42%. Це дослідження характеризувалося внутрішньою неоднорідністю: ефект аспірину значно відрізнявся у пацієнтів, яким була показана (зниження ВР на 94%) і не була показана (зниження ВР на 8%) терапія варфарином. Крім того, аспірин був менш ефективним у пацієнтів старших за 75 років і не знижував ризик важкого або рецидивуючого інсульту. Дослідження SPAF-I було припинено достроково, а його результати можуть бути завищеними.
З фармакологічної точки зору аспірин у дозі 75 мг викликає практично повне інгібування агрегації тромбоцитів. При цьому в низькій дозі (<100 мг) аспірин рідше викликає кровотечі, ніж у більш високих дозах (таких як 300 мг). Якщо показана терапія аспірином, то його доцільно призначати в більш низьких дозах (75-100 мг / добу).
Ступінь зниження ризику інсульту при застосуванні аспірину в порівнянні з плацебо, встановлена при мета-аналізі (на 19%), була в цілому подібною до тієї, що і при призначенні препарату пацієнтам з судинними захворюваннями. Останні часто поєднуються з ФП, тому помірний сприятливий ефект аспірину при ФП, швидше за все, відображає ефективність препарату у хворих з судинними захворюваннями. В останніх дослідженнях у пацієнтів без ФП не була підтверджена ефективність аспірину в первинній профілактиці серцево-судинних результатів.
У дослідженні Japan Atrial Fibrillation Stroke Trial [55] пацієнти з ізольованою ФП були рандомізовані на групу аспірину (150-200 мг/добу) і контрольну групу (не проводилася терапія антитромбоцитарними засобами або антикоагулянтами). Частота несприятливих результатів в групі аспірину була вищою (3,1% на рік), ніж у контрольній групі (2,4% на рік). Крім того, лікування аспірином призвело до недостовірного збільшення ризику великих кровотеч (1,6% і 0,4%).
4.1.2.3 Антагоністи вітаміну К у порівнянні з антитромбоцитарними засобами
У 9 дослідженнях прямо порівнювали антагоністи вітаміну К і аспірин. Антикоагулянти по ефективності достовірно перевершували аспірин і знижували ЗР на 39%. У дослідженні BAFTA антагоністи вітаміну К (цільове МНВ 2-3) мали перевагу перед аспірином у дозі 75 мг / добу в профілактиці фатального і інвалідизуючого інсульту (ішемічного та геморагічного), внутрішньочерепної кровотечі або клінічної значущою артеріальної емболії (зниження ВР на 52%); достовірної різниці ризику великої кровотечі між групами варфарину та аспірину не виявили [56]. Отримані дані узгоджуються з результатами невеликого дослідження WASPO, в якому аспірин у порівнянні з варфарином значно частіше викликав небажані явища (33% і 6%, відповідно; р = 0,002), включаючи серйозні кровотечі. У дослідженнях, які проводилися до BAFTA, ризик внутрішньочерепної кровотечі при застосуванні варфарину під контролем МНВ був удвічі вище, ніж при лікуванні аспірином, хоча абсолютне збільшення ризику було невеликим (0,2% на рік) [54].
4.1.2.4 Інші антитромботичні препарати
У дослідженні ACTIVE W антикоагулянтна терапія за ефективністю перевершувала комбінацію клопідогреля і аспірина (зниження ВР на 40%; 95% ДІ 18-56), а частота кровотеч була порівнянною у двох групах [57]. У дослідженні (ACTIVE A) ризик основних судинних результатів при лікуванні аспірином / клопідогрелем знизився в порівнянні з монотерапією аспірином (ВР 0,89; 95% ДІ 0,81-0,98; P = 0,01), в основному через зниження відносного ризику інсульту на 28% [58]. Частота великих кровотеч значно збільшилася (2,0% і 1,3% на рік, відповідно; ВР 1,57; 95% ДІ 1,29-1,92; P < 0,001) і була в цілому подібною до тієї, що і при лікуванні антагоністами вітаміну К. Слід зазначити, що 50% хворих були включені в дослідження, так як на думку лікаря вони не були кандидатами на лікування антагоністами вітаміну К, а у 23% пацієнтів початково були фактори ризику кровотеч. Таким чином, аспірин в комбінації з клопідогрелем може використовуватися в тих випадках, коли терапія антагоністами вітаміну К не прийнятна, проте два препарати не можуть служити альтернативою останнім при високому ризику кровотеч.
Інші антитромбоцитарні препарати, такі як індобуфен і трифлузал, давали певний ефект у хворих з ФП, однак необхідні додаткові дослідження. Вивчалася комбінована терапія антагоністами вітаміну К (МНВ 2,0-3,0) з антитромбоцитарними засобами, однак вона не давала додаткового ефекту в профілактиці ішемічного інсульту і судинних результатів і частіше викликала кровотечі. Отже, у хворого з ФП, який переніс ішемічний інсульт незважаючи на лікування антагоністом вітаміну К (МНВ 2,0-3,0), доцільне збільшення інтенсивності антикоагуляції (МНВ 3,0-3,5), а не додавання антитромбоцитарного препарату, так як ризик великих кровотеч починає істотно збільшуватися тільки при МНВ ≥ 3,5.
Коментар робочої групи:
Індобуфен станом на 01.10.2015р. не зареєстрований в Україні як лікарський засіб.
4.1.2.5 Нові препарати
В даний час розробляються нові препарати для профілактики інсульту у хворих з ФП – пероральні прямі інгібітори тромбіну (дабігатрану етексилат і AZD0837) і пероральні інгібітори фактора Ха (ривароксабан, апіксабан, едоксабан, бетріксабан, YM150.
У дослідженні RE-LY [59] дабігатран в дозі 110 мг двічі на день не поступався антагоністові вітаміну К по ефективності в профілактиці інсульту і системних емболій і рідше викликав великі кровотечі. При застосуванні дабігатрану в дозі 150 мг двічі на день частота інсульту і системних емболій знизилася, а частота великих кровотеч була порівнянною з такою в групі антагоніста вітаміну К [59]. Дослідження AVERROES було припинено достроково, враховуючи достовірне зниження ризику інсульту і системних емболій при лікуванні апіксабаном в дозі 5 мг двічі на день у порівнянні з аспірином у дозі 81-324 мг/добу при поганій переносимості антагоніста вітаміну К або неможливості його застосування. Безпека апіксабану була прийнятною.
Коментар робочої групи:
Едоксабан та бетріксабан станом на 01.10.2015р. не зареєстровані в Україні як лікарські засоби.
Правильна МНН дабігатрану - дабігатрану етексилат.
Згідно з правками рекомендацій ESC 2012 та EHRA 2013 років:
На сьогоднішній день вивченими є декілька нових антикоагулянтних лікарських засобів, призначених для профілактики інсульту у хворих з ФП. Загалом вони поділяються на два класи – прямі інгібітори тромбіну для перорального прийому (наприклад, дабігатрану етексилат) і інгібітори фактору Xa для перорального прийому (ривароксабан, апиксабан та інші).
У відкритому рандомізованому дослідженні з вивчення застосування тривалої антикоагулянтної терапії дабігатрану етексилатом [Randomized Evaluation of Long-term anticoagulant therapY with dabigatran etexilate, RE-LY], 18 113 пацієнтів з 44 країн, що хворіли на неклапанну форму фібриляції передсердь та мали підвищений ризик розвитку інсульту; середня тривалість періоду спостереження склала 2 роки, сума балів по шкалі CHADS2 – 2,1 бали. Розподіл пацієнтів за балами шкали CHADS2 був наступним: від 0 до 1 балу – 5775 пацієнтів, 2 бали – 6455 пацієнтів та від 3 до 6 балів – 5882 пацієнтів, що відображало широку клінічну практику. Прийом дабігатрану у дозі 110 мг двічі на день виявився не гіршим за застосування АВК щодо попередження інсульту та системного емболізму, обумовлюючи при цьому більш низькі рівні серйозних геморагічних ускладнень. Дабігатран (у дозі 150 мг двічі на добу) виявився значущо більш ефективним за варфарин у відношенні зниження частоти первинної кінцевої точки ефективності, що була відмічена у 134 пацієнтів (1,11% на рік) в групі дабігатрану проти 199 пацієнтів (1,69% на рік) в групі варфарину (ВР 0,66; p< 0,001). При цьому в групі дабігатрану (у дозі 150 мг двічі на добу) у порівнянні з групою варфарину було відмічено достовірне зниження частоти ішемічного інсульту або інсульту не уточненої етіології, що склало 0,92 та 1,20% на рік відповідно (р=0,03), що становить 25%. Частота виникнення геморагічного інсульту в обох групах дабігатрану виявилась суттєво нижчою, ніж у хворих, що отримували варфарин: дабігатран 110 мг двічі на добу/дабігатран 150 мг двічі на добу/варфарин – 0,1% на рік/0,12% на рік/0,38% на рік відповідно, що відповідає зниженню ВР на 69% в групі дабігатрану 110 мг двічі на добу та на 74% в групі дабігатрану 150 мг двічі на добу.
Додаткові дані, що були отримані в ході додаткових спостережень (клінічне дослідженні RELY-ABLE), підтверджують профіль безпеки дабігатрана та узгоджуються з даними дослідження RE-LY.
Дослідження з оцінки ефективності апіксабану у порівнянні із ацетилсаліциловою кислотою для профілактики інсультів [Apixaban VERsus acetylsalicylic acid to pRevent strOkES, AVERROES] було зупинене достроково через отримання чітких доказів на користь зниження ризику інсульту та системного емболізму на фоні застосування апіксабану у дозі 5 мг двічі на добу у порівнянні з аспірином у дозах 81-324 мг один раз на добу у пацієнтів, які не переносять АВК або для яких терапія АВК не підходить, з прийнятним профілем безпечності препарату.
В ході сліпого подвійного плацебо-контрольованого дослідження ROCKET AF (Rivaroxaban Once daily oral direct Factor Xa inhibition Compared with vitamin K antagonism for prevention of stroke and Embolism Trial in Atrial Fibrillation) було проведене порівняння ефективності та безпеки використання ривароксабану і варфарину. Під час дослідження вивчалось застосування ривароксабану 1 раз на добу (20 мг або 15 мг – для пацієнтів із порушенням функції нирок) в порівнянні з варфарином, підібраним по дозі, і воно охопило 14 264 пацієнтів із неклапанною ФП з ризиком розвитку інсульту або ТЕУ. Особливістю цього дослідження було те, що в нього були включені пацієнти високого ризику (згідно оцінці за шкалою CHADS2 ступінь ризику розвитку тромбоемболічних подій складала в середньому 3,48 бали). Це дуже значущий момент з точки зору важливості застосування ривароксабану у пацієнтів з ФП, у яких, за звичай, високий ішемічний ризик тісно пов'язаний з високим геморагічним ризиком.
Згідно з результатами дослідження ROCKET AF за основною кінцевою точкою ефективності ривароксабан (у дозах 20 мг та 15 мг для пацієнтів з порушенням функції нирок середньої тяжкості) в період лікування продемонстрував не гірши показники в порівнянні з варфарином, який вживали в скоригованій дозі, забезпечивши зниження відносного ризику розвитку інсульту і системних ТЕУ на 21% (1,70 vs 2,15 на 100 пацієнто-років; p=0,015).
Ще одним значущим результатом цього дослідження є суттєве зменшення частоти випадків одного з найбільш важких видів інсульту – геморагічного на 41% (0,26 vs 0,44 на 100 пацієнто-років; p=0,024), та фатальних кровотеч на 50% (0,4 vs 0,8 на 100 пацієнто-років; р=0,003) в групі ривароксабану. При лікуванні ривароксабаном також спостерігалось зменшення кількості випадків інфаркту міокарда на 19% (0,91 vs 1,124 на 100 пацієнто-років; p=0,121), зменшення загальної смертності на 15% (1,87 vs 2,21 на 100 пацієнто-років; p=0,073) і зниження загального ризику серцево-судинних подій (інсульту, системних ТЕУ, серцево-судинної смерті та інфаркту міокарду) на 15% (3,91 vs 4,62 на 100 пацієнто-років; p=0,010).
Особливо слід відмітити підгрупу пацієнтів з ураженням нирок. У порівнянні з пацієнтами з нормальною функцією нирок, пацієнти зі зниженою функцією нирок мають вищий ризик як інсульту, так і геморагічних ускладнень антикоагулянтної терапії. Згідно з результатами дослідження ROCKET AF, ривароксабан в дозі 15 міліграм для пацієнтів з кліренсом креатиніну 30-49 мл/хв продемонстрував ефективність не гірше ніж варфарин в скоригованій дозі, забезпечивши зниження відносного ризику розвитку інсульту і системних ТЕУ на 16% (2,77 vs 2,32 на 100 пацієнто-років; p=0,76) та суттєве зниження ризику фатальних кровотеч порівняно з варфарином на 61% (0,74 vs 0,28 на 100 пацієнто-років; 95% ДІ 0,15-0,99).
Метою дослідження ARISTOTLE (Apixaban for Reduction in Stroke and Other Thromboembolic Events in Atrial Fibrillation було проведення порівняння ефективності та безпеки використання апиксабану і варфарину. Під час дослідження вивчалось застосування апиксабану в дозі 5 мг двічі на добу в порівнянні з варфарином, підібраним по дозі, і воно охопило 18 201 пацієнта з неклапанною ФП з ризиком розвитку інсульту або системної тромбоемболії (середній бал за шкалою CHADS2 – 2,1 бали). За результатами дослідження було виявлено що апиксабан у порівнянні з варфарином зменшив ризик розвитку інсульту та ТЕУ на 21% (1,27 vs 1,60%; p<0,001) , виникнення кровотеч на 31% (2,13 vs 3,09%; p<0,001), а смертність знизилася на 11% (3,52 vs 3,94%; p=0,047).
Позитивний терапевтичний ефект НПАК (ривароксабану, дабігатрану, апіксабану та ін..) не вимагав обмежень у раціоні харчування або лабораторного моніторингу, що є важливим аргументом на користь використання нових антикоагулянтів у наший країні в умовах обмежених можливостей контролю МНО.
4.1.3 Сучасні рекомендації щодо антитромботичної терапії
Рекомендації щодо антитромботичної терапії повинні ґрунтуватися на наявності (або відсутності) факторів ризику інсульту і тромбоемболій, а не штучному виділенні груп високого, середнього та низького ризику.
Індекс CHADS2 (див. Розділ 4.1.1) слід використовувати для первісної оцінки ризику інсульту; ця схема особливо зручна для лікарів загальної практики і неспеціалістів. Якщо індекс CHADS2 становить принаймні 2, рекомендується терапія пероральними антикоагулянтами (цільовий діапазон МНВ 2,0-3,0), якщо немає протипоказань. У пацієнтів з індексом CHADS2 0-1 рекомендується проводити більш детальну оцінку ризику інсульту з урахуванням інших факторів ризику тромбоемболій (табл. 9 і рис. 4) – схема CHA2DS2-VASc [52] (див. Табл. 8). У багатьох сучасних клінічних дослідженнях, в яких вивчалася ефективність профілактики інсульту у хворих з ФП, деякі додаткові фактори ризику були критеріями включення [57-59]. У всіх випадках, коли обговорюється антикоагулянтна терапія, слід інформувати пацієнта про переваги і недоліки подібних препаратів, оцінити ризик геморагічних ускладнень, здатність пацієнта контролювати результати терапії і його переваги. У деяких випадках, наприклад, у жінок у віці ≥65 років без інших факторів ризику (індекс CHA2DS2-VASс 1), може бути використаний аспірин, а не пероральні антикоагулянти.
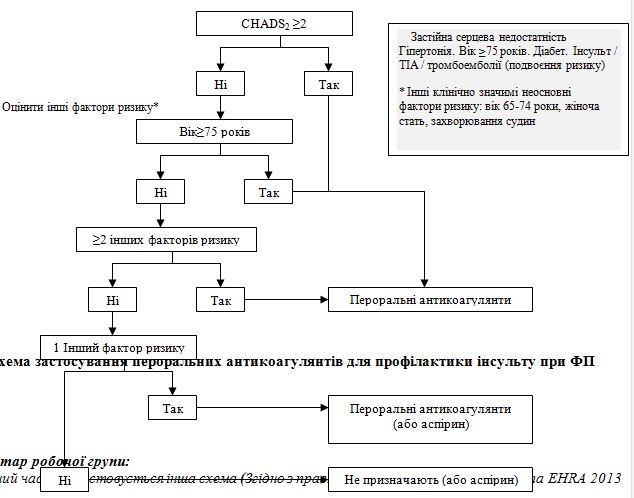
Рис. 4. Схема застосування пероральних антикоагулянтів для профілактики інсульту при ФП
Коментар робочої групи:
На даний час використовується інша схема (Згідно з правками рекомендацій ESC 2012 та EHRA 2013 років)
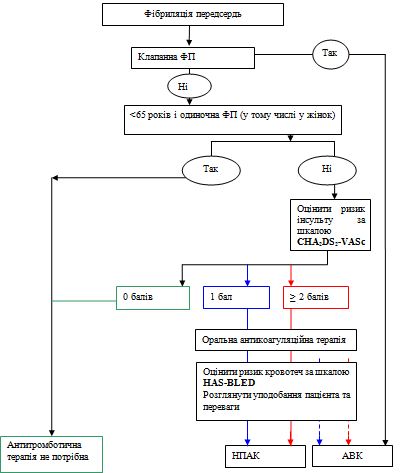
Рисунок 4. Клінічний алгоритм застосування пероральних антикоагулянтів з метою профілактики інсульту при ФП (згідно з поправками 2012 року).
Таблиця 9. Підходи до тромбопрофілактики у пацієнтів з ФП
|
Категорія ризику
|
Індекс CHA2DS2-VASc
|
Рекомендована антитромботична терапія
|
|
Один основний фактор ризику або ≥2 клінічно значущих неосновних факторів ризику
|
≥2
|
Пероральні антикоагулянтиа
|
|
Один клінічно значущий неосновний фактор ризику
|
1
|
Пероральні антикоагулянтиа або аспірин 75-325 мг / добу. Пероральні антикоагулянти мають перевагу перед аспірином
|
|
Немає факторів ризику
|
0
|
Аспірин 75-325 мг / добу або не призначати антитромботичні засоби. Переважно не застосовувати антитромботичні препарати.
|
CHA2DS2-VASc: серцева недостатність, артеріальна гіпертонія, вік ≥75 років (подвоєний ризик), цукровий діабет, інсульт (подвоєний ризик) – захворювання судин, вік 65-74 роки і жіноча стать. МНВ – міжнародне нормалізоване відношення.
аПероральні антикоагулянти – антагоністи вітаміну К; МНВ 2,0-3,0 (цільове значення 2,5). У перспективі можливе застосування нових пероральних антикоагулянтів. Наприклад, якщо дабігатран етексилат в обох дозах буде зареєстрований для профілактики інсульту у пацієнтів з ФП, то рекомендації щодо тромбопрофілактики можуть бути змінені таким чином:
(a) Якщо необхідна пероральна антикоагуляція, то дабігатран може бути альтернативою стандартним антагоністам вітаміну К. (i) Пацієнтам з низьким ризиком кровотеч (індекс HAS-BLED 0-2; див. Табл. 10) дабігатран призначають у дозі 150 мг двічі на день, враховуючи більш високу ефективність у профілактиці інсульту і системних емболій (і більш низьку частоту внутрішньочерепних кровотеч і схожу частоту великих кровотеч у порівнянні з варфарином); (Ii) пацієнтам з більш високим ризиком кровотечі (HAS-BLED ≥3) дабігатран етексилат може бути призначений у дозі 110 мг двічі на день, враховуючи подібну з антагоністами вітаміну К ефективність у профілактиці інсульту і системних емболій і нижчу частоту внутрішньочерепних кровотеч і великих кровотеч.
(b) Хворим з одним клінічно значущим неосновним чинником ризику інсульту може бути призначений дабігатран в дозі 110 мг двічі на день з урахуванням подібної з антагоністами вітаміну К ефективністю у профілактиці інсульту і системних емболій і більш низької частоти внутрішньочерепних і великих кровотеч у порівнянні з антагоністами вітаміну К і (ймовірно) аспірином.
(c) За відсутності факторів ризику (CHA2DS2-VASc = 0) ймовірність інсульту дуже низька, тому рекомендується застосовувати аспірин у дозі 75-325 мг / добу або не призначати антитромботичні засоби. По можливості слід уникати антитромботичної терапії, оскільки користь аспірину в цій групі пацієнтів (наприклад, з ізольованою ФП) переконливо не доведена, а антитромботичні препарати можуть викликати небажані ефекти, особливо кровотечі.
Коментар робочої групи:
Таблиця 9. Стратегія профілактики тромбоемболічних ускладнень у пацієнтів з ФП
(згідно з правками 2012 року).
|
Категорія ризику
|
Кількість балів за шкалою CHA2DS2-VASc
|
Рекомендована антитромботична терапія
|
|
Один «серйозний» фактор ризику або ≥2 «клінічно значущих несерйозних» факторів ризику
|
≥2
|
НПАК або ПАКa
|
|
Один «клінічно значущий несерйозний» фактор ризику
|
1
|
НПАК або ПАК,
Перевагу має НПАК у порівнянні з аспірином.
|
|
Відсутність факторів ризику
|
0
|
Відсутність антитромботичної терапії або аспірин 100-325 мг на добу.
Перевагу має відсутність антитромботичної терапії у порівнянні з аспірином.
|
4.1.4. Ризик кровотеч
Перед початком антикоагуляції необхідно оцінити ризик кровотеч. Незважаючи на антикоагуляції у пацієнтів похилого віку частота внутрішньочерепної кровотечі значно нижча, ніж у минулому, і становить від 0,1 до 0,6%. Це може відображати знижену інтенсивність антикоагуляції, більш ретельний підбір дози або поліпшення контролю артеріальної гіпертонії. Частота внутрішньочерепних кровотеч збільшується при МНВ > 3,5-4,0, в той час як при МНВ 2,0-3,0 ризик їх додатково збільшується в порівнянні з таким при більш низьких значеннях МНВ.
Розроблено різні індекси для оцінки ризику кровотеч у хворих, які отримують антикоагулянтну терапію. Всі вони передбачають виділення груп низького, середнього та високого ризику (зазвичай великих кровотеч). Можна припустити, що ризик великих кровотеч при лікуванні аспірином і антагоністами вітаміну К порівнянний, особливо у літніх людей [56]. Небезпека падінь, ймовірно, перебільшується, оскільки пацієнту необхідно падати більше 300 разів на рік, щоб ризик внутрішньочерепної кровотечі переважив користь пероральних антикоагулянтів у профілактиці інсульту.
На підставі обстеження когорти з 3978 європейців з ФП, які брали участь у EuroHeart Survey, був розроблений новий простий індекс ризику кровотечі – HAS-BLED (артеріальна гіпертонія, порушення функції нирок / печінки, інсульт, кровотечі в анамнезі або схильність до кровоточивості, лабільне МНВ, вік> 65 років, прийом ліків / алкоголю) (табл. 10) [60]. Цей індекс доцільно використовувати для оцінки ризику кровотечі у пацієнтів з ФП. Значення індексу ≥ 3 вказує на високий ризик. Однак необхідно дотримуватися обережності і регулярно контролювати стан пацієнтів, які отримують антитромботичні засоби (антагоністи вітаміну К або аспірин).
Таблиця 10. Індекс ризику кровотеч HAS-BLEED
|
Буква*
|
Клінічна характеристикаa
|
Число балів
|
|
H
|
Гіпертонія
|
1
|
|
A
|
Порушення функції печінки або нирок (по 1 балу)
|
1 або 2
|
|
S
|
Інсульт
|
1
|
|
B
|
Кровотеча
|
1
|
|
L
|
Лабільне МНВ
|
1
|
|
E
|
Вік >65 років
|
1
|
|
D
|
Ліки або алкоголь (по 1 балу)
|
1 або 2
|
|
|
|
Максимум 9 балів
|
Перші букви англійських слів
a Гіпертонія – систолічний АТ> 160 мм рт. ст., порушення функції нирок – діаліз, трансплантація нирки або сироватковий креатинін ≥200 ммоль / л, порушення функції печінки – хронічне захворювання печінки (наприклад цироз) або біохімічні ознаки серйозного ураження печінки (наприклад, рівень білірубіну принаймні вдвічі вище верхньої межі норми у поєднанні з підвищенням активності АСТ / АЛТ / лужної фосфатази більш ніж в 3 рази порівняно з верхньою межею норми і т.д.), кровотеча – кровотеча в анамнезі та / або схильність до кровотечі, наприклад, геморагічний діатез, анемія і т.д., лабільне МНВ – нестабільне / високе МНВ або недостатній термін збереження МНВ в цільовому діапазоні (наприклад, <60% часу), ліки / алкоголь – супутній прийом ліків, таких як антитромбоцитарні препарати, нестероїдні протизапальні препарати, або зловживання алкоголем. Pisters et al. [60]
4.1.5 Оптимальне міжнародне нормалізоване відношення
В даний час рівень антикоагуляції оцінюють на підставі МНВ – відносини фактичного протромбінового часу і протромбінового часу стандартизованої контрольної сироватки. При профілактиці інсульту і системних емболій у пацієнтів з неклапанною ФП оптимальне МНВ становить 2,0-3,0. Воно забезпечує баланс між зниженням ефективності при низькому МНВ і збільшенням ризику кровотечі при високому значенні показника.
Однією з багатьох проблем, що виникають при застосуванні антагоністів вітаміну К, є висока між- і інтраіндивідуальна варіабельність МНВ. Крім того, антагоністи вітаміну К взаємодіють з їжею, ліками та алкоголем. У контрольованих клінічних дослідженнях цільове МНВ в діапазоні 2,0-3,0 вдавалося підтримувати протягом 60-65% часу, проте в реальній практиці цей показник може бути нижче 50%. Якщо МНВ знаходиться нижче цільового діапазону протягом зазначеного терміну, то це може повністю нівелювати користь антагоністів вітаміну К.
Хоча у літніх людей пропонувалося підтримувати МНВ в більш низькому діапазоні (1,8-2,5), доцільність такого підходу не вивчалась у великому клінічному дослідженні. Когортні дослідження свідчать про 2-кратне збільшення ризику інсульту при МНВ 1,5-2,0. У зв'язку з цим підтримувати МНВ на рівні <2,0 не рекомендується.
Можливість збереження МНВ в цільовому діапазоні, безпечність та ефективність антагоністів вітаміну К залежать від фармакогенетичних факторів, зокрема поліморфізму гена цитохрому Р450 2C9 (CYP2C9) і гена комплексу 1 епоксид редуктази вітаміну К (VKORC1). Генотипи CYP2C9 і VKORC1 впливають на потребу в дозі варфарину, в той час як поліморфізм CYP2C9 асоціюється з ризиком кровотечі. Систематичне генотипування звичайно не потрібно, так як воно характеризується низькою ефективністю витрат у пацієнтів з неклапанною ФП, проте витрати можуть бути виправданими у пацієнтів з високим ризиком кровотеч, які починають лікування антагоністами вітаміну К.
Самостійне моніторування антикоагуляції
Самостійне моніторування можливо, якщо пацієнт здатний виконувати необхідні тести (або це може зробити його родич). Важливе значення має адекватне навчання і постійний контакт з лікарем. Прилади для самостійного моніторування повинні мати адекватну якість і бути каліброваними.
Коментар робочої групи:
4.1.5.1. Протромбіновий індекс
Для оцінки стану системи згортання крові при застосуванні АВК показник МНВ є надійнішим, ніж протромбіновий індекс ПТІ, тому що не залежить від якості реагенту. На жаль, документація, яка додається до тромбопластинів, які використовуються сьогодні в більшості українських лабораторій, не містить інформацію відносно чутливості реагенту. Тому ПТІ залишається єдиним показником, по якому може здійснюватися контроль антикоагулянтної терапії. Його традиційно розраховують по формулі: ПТІ= (контрольний протромбіновий час/ протромбіновий час пацієнта) х100%. Для профілактики інсульту і системних емболій у пацієнтів з неклапанною ФП оптимальний ПТІ складає 50-60%, що приблизно відповідає МНО 2,0-3,0.
Експрес-діагностика та регулярний самоконтроль показників зсідання крові при антикоагулянтній терапії
Можливість регулярного самоконтролю показників зсідання крові може розглядатися, якщо пацієнт надає такій методиці перевагу і є фізично та когнітивно здатним виконувати тести самоконтролю або, у випадку коли він не може виконувати такі тести сам, якщо їх може здійснювати призначена для надання пацієнту допомоги особа. Важливе належне навчання досвідченим медичним працівником, і пацієнт при здійсненні самоконтролю повинен продовжувати контактувати з цим клініцистом. Прилади, призначені для виконання таких тестів самоконтролю, також потребують належної оцінки якості та калібрування.
Перехід з антагоністів вітаміну К на НПАК
При переході пацієнтів з АВК на НПАК після прийому НПАК значення МНВ можуть бути хибно підвищені. Ці значення МНВ не можна використовувати для оцінки антикоагулянтної активності НПАК.
Терапію НПАК потрібно розпочинати негайно, коли показники МНВ нижче 2,0. Якщо показники МНВ складають 2,0 – 2,5, терапію НПАК можна розпочинати негайно або (бажано) наступного дня. Для МНВ >2.5, з метою визначення часу ймовірного зниження показників МНВ до наступних значень слід взяти до уваги фактичні показники МНВ та період напіввиведення антагоністів вітаміну К: аценокумарол t½ 8–14 годин, варфарин t½ 36–42 годин, фенпрокумон* t½ 6 днів (120-200 годин). В цей час, можна призначати вимірювання показників міжнародного нормалізованого відношення (МНВ).
* Фенпрокумон станом на 01.10.2015р. в Україні не зареєстрований як лікарський засіб.
Перехід від прийому парентеральних антикоагулянтів до нових пероральних антикоагулянтів
Нефракціонований гепарин (НФГ), що вводиться внутрішньовенно: Терапію НПАК (новими пероральними антикоагулянтами) можна розпочинати після закінчення курсу лікування НФГ (період напіввиведення ±2 години). З обережністю слід призначати лікування пацієнтам з хронічною хворобою нирок, у яких процес виведення гепарину може бути тривалішим.
Низькомолекулярний гепарин (НМГ): Терапію НПАК можна розпочинати, коли передбачена наступна доза НМГ.
Перехід від прийому нових пероральних антикоагулянтів (НПАК) до прийому антагоністів вітаміну К
Через повільне настання дії антагоністів вітаміну К, МНВ у межах терапевтичного діапазону виникає через 5-10 днів, із значною індивідуальною мінливістю.
Таким чином, для забезпечення належної антикоагуляції НПАК та антагоністи вітаміну К слід приймати одночасно до досягнення оптимальних показників МНВ, як і тоді коли пацієнти продовжують приймати НМГ під час початку лікування антагоністами вітаміну К. Не рекомендується застосовувати режим навантажувальних доз аценокумаролу та варфарину, окрім фенпрокумону.
Оскільки НПАК (особливо інгібітори фактору Ха) можуть чинити додатковий вплив на значення показника МНВ у пацієнтів, які одночасно отримують терапію НПАК та АВК, важливо щоб вимірювання МНВ здійснювалось безпосередньо перед наступним прийомом НПАК (під час супутнього застосування), та вимірюватись знову через 24 години після останнього прийому НПАК (монотерапія антагоністами вітаміну К). Рекомендується встановити ретельний моніторинг показників МНВ впродовж першого місяця до досягнення стабільних значень (тобто результати трьох послідовних вимірювань мають бути в межах 2,0 – 3,0).
Перехід від прийому нових пероральних антикоагулянтів до парентеральних антикоагулянтів
Парентеральне введення антикоагулянтів (НФГ, НМГ) можна розпочинати в той час, коли б здійснювався наступний запланований прийом НПАК.
Перехід від прийому нових пероральних антикоагулянтів до нових пероральних антикоагулянтів
Прийом альтернативного НПАК можна розпочинати замість наступної дози НПАК, що приймався перед переходом, за винятком ситуацій, коли в плазмі можуть очікуватись концентрації, що перевищують терапевтичні (наприклад у пацієнтів з порушенням ниркової функції, що приймали дабігатран). У таких ситуаціях, можна зробити довший інтервал, згідно Таблиці 11 та 16.
Таблиця 11. Визначення періоду напіввиведення НПАК і і площу під кривою “концентрація – час” на різних стадіях хронічної хвороби нирок у порівняні із здоровими особами
|
|
Дабігатран
|
Апіксабан
|
Eдоксабан
|
Ривароксабан
|
|
CrCl >60 мл/хв.
|
~14 год.
|
дані відсутні
|
~8.6 год.
|
~8.5 год. (+44%)
|
|
ХХН І та ІІ стадії
|
|
|
|
|
|
CrCl 30-60 мл/хв.
|
~18- год.
|
дані відсутні
|
~9.4 год.
|
~9 год. (+52%)
|
|
ХХН ІІІ стадії
|
|
|
|
|
|
CrCl 15-30 мл/хв.
|
~28 год.
|
дані відсутні
|
~16.9 год.
|
~9.5 год. (+64%)
|
|
ХХН IV стадії
|
|
|
|
|
|
CrCl <15 мл/хв.
|
дані відсутні mmm
|
дані відсутні
|
дані відсутні
|
дані відсутні
|
|
ХХН V стадії
|
|
|
|
|
|
ХХН – хронічна хвороба нирок, CrCl – кліренс креатиніну.
|
|
|
|
Дозування, наразі дані відсутні.
|
|
|
Перехід від прийому аспірину до нових пероральних антикоагулянтів
Прийом НПАК можна розпочати негайно, а застосування аспірину та клопідрогелю – припинити, окрім випадків, коли є необхідність у комбінованій терапії незважаючи на ризик виникнення кровотечі (див. наступні розділи).
4.1.6 Особливі ситуації
4.1.6.1 Пароксизмальная фібриляція передсердь
Ризик інсульту і тромбоемболій у пацієнтів з пароксизмальною ФП вивчений у меншій мірі. Частка таких пацієнтів у клінічних дослідженнях, в яких вивчалася ефективність тромбопрофілактики, зазвичай була нижчою 30%. Ризик інсульту у пацієнтів з пароксизмальною ФП не відрізняється від такого у пацієнтів з персистуючою або постійною ФП [12] і залежить від наявності факторів ризику (див. Розділ 4.1.1). Отже, пацієнти з пароксизмальною ФП повинні отримувати пероральні антикоагулянти відповідно до індексу ризику.
4.1.6.2 Періопераційна антикоагуляція
У пацієнтів з ФП, які отримують антикоагулянтну терапію, слід на час перервати лікування антагоністом вітаміну К перед операцією або інвазивні втручанням. Багато хірургів проводять операцію тільки, якщо МНВ становить <1,5 або навіть нормалізується. Ризик клінічно значущих кровотеч, навіть у амбулаторних пацієнтів, яким проводяться невеликі втручання, необхідно співвідносити з ризиком інсульту або тромбоемболій.
Якщо застосовується варфарин, період напіввиведення якого становить близько 36-42 год, то його слід відмінити приблизно за 5 днів до операції (приблизно 5 періодів напіввиведення варфарину), щоб забезпечити адекватне зниження МНВ. Якщо в якості антагоніста вітаміну К застосуються фенпрокумон, його слід відмінити за 10 днів до операції (період напіввиведення 96-140 год). Хірургічні та діагностичні процедури, що супроводжуються ризиком кровотечі, слід проводити на тлі субтерапевтичної антикоагуляції (протягом 48 год), не призначаючи гепарин, враховуючи низький ризик тромбоемболій в цей період. Потім лікування антагоністом вітаміну К слід відновити до звичайної підтримуючої дози (без ударної дози) ввечері в день операції (або наступного ранку) за умови адекватного гемостазу. Якщо операцію або втручання доводиться проводити на тлі підвищеного МНВ (> 1,5), можливе призначення вітаміну.
Ведення пацієнтів зі штучним клапаном серця або ФП і високим ризиком тромбоемболій може виявитися проблемним. Під час перерви в лікуванні антагоністом вітаміну К в таких випадках можливе застосування НМГ або НФГ в терапевтичних дозах.
4.1.6.3 Стабільне захворювання судин
У багатьох пацієнтів з ФП, які отримують антикоагулянти, є стабільний атеросклероз коронарних або сонних артерій та / або ураження периферичних артерій. Таким пацієнтам антагоністи вітаміну К зазвичай призначають у поєднанні з антитромбоцитарним препаратом, найчастіше аспірином. Приєднання аспірину до антагоніста вітаміна К не призводить до зниження ризику інсульту або судинних ускладнень (включаючи інфаркт міокарда), але значно збільшує частоту кровотеч.
4.1.6.4 Гострий коронарний синдром та / або черезшкірне інтракоронарне втручання
У сучасних рекомендаціях пропонується застосовувати аспірин в комбінації з клопідогрелем після ГКС і стентування (протягом 4 тижнів після установки металевого стента і 6-12 місяців після імплантації стента з лікарським покриттям). Якщо пацієнтам не призначають антагоністи вітаміну К, то це призводить до збільшення смертності та основних серцево-судинних результатів. При цьому частота кровотеч вірогідно не відрізняється у пацієнтів, які отримують і не одержують антагоністи вітаміну К. Частота великих кровотеч на тлі потрійної терапії (антагоніст вітаміну К, аспірин та клопідогрель) склала 2,6-4,6% через 30 днів і збільшилася до 7, 4-10,3% протягом 12 місяців. Таким чином, потрійна терапія характеризується прийнятним коефіцієнтом користь / ризик, якщо її продовжують протягом короткого терміну (наприклад, протягом 4 тижнів), а ризик кровотеч низький.
У документі, опублікованому робочою групою ESC по тромбозу і схваленому EHRA та Європейською асоціацією черезшкірних серцево-судинних втручань (EAPCI), рекомендовано уникати імплантації стентів з лікарським покриттям у пацієнтів з ФП і проводити потрійну терапію (антагоніст вітаміну К, аспірин та клопідогрель) протягом короткого терміну після стентування, а потім продовжувати лікування антагоністом вітаміну К в поєднанні з одним антитромбоцитарним препаратом (клопідогрелем або аспірином; табл. 11) [61]. Пацієнтам зі стабільним захворюванням судин (тобто за відсутності гострих ішемічних ускладнень або черезшкірного втручання на коронарних артеріях / стентування протягом попереднього року) показана монотерапія антагоністами вітаміну К, а одночасно призначати антитромбоцитарні засоби не слід. Опубліковані дані обґрунтовують застосування антагоністів вітаміну К для вторинної профілактики у пацієнтів з коронарною хворобою серця. Препарати цієї групи по ефективності принаймні не поступаються аспірину.
Таблиця 11. Стратегія антитромботичної терапії після стентування коронарних артерій у хворих з ФП і середнім або високим ризиком тромбоемболічних ускладнень (яким потрібна пероральна антикоагуляція)
|
Ризик кровотечі
|
Втручання
|
Стент
|
Схема антикоагуляції
|
|
Низький або середній (HAS-BLED 0-2)
|
Планове
|
Без покриття
|
1 місяць: потрійна терапія антагоністом вітаміну К (МНВ 2,0-2,5) + аспірином ≤100 мг / добу + клопідогрелем 75 мг / добу
Довічно: антагоніст вітаміну К (МНВ 2,0-3,0) у вигляді монотерапії
|
|
Планове
|
З покриттям лікарськими засобами
|
3 (-олімусf) – 6 (паклітаксел) міс: потрійна терапія антагоністом вітаміну К (МНВ 2,0-2,5) + аспірином ≤100 мг / добу + клопідогрелем 75 мг / добу.
До 12 міс: комбінована терапія антагоністом вітаміну К (МНВ 2,0-2,5) і клопідогрелем 75 мг / добу (або аспірином 100 мг / добу)
Довічно: антагоніст вітаміну К (МНВ 2,0-3,0)
|
|
ГКС
|
Стент з покриттям або без покриття
|
6 міс: потрійна терапія антагоністом вітаміну К (МНВ 2,0-2,5) + аспірином ≤100 мг / добу + клопідогрелем 75 мг / добу
До 12 міс: комбінована терапія антагоністом вітаміну К (МНВ 2,0-2,5) і клопідогрелем 75 мг / добу (або аспірином 100 мг / добу)
Довічно: антагоніст вітаміну К (МНВ 2,0-3,0)
|
|
Високий (HAS-BLED≥3)
|
Планове
|
Стент без покриттяс
|
2-4 тижні: потрійна терапія антагоністом вітаміну К (МНВ 2,0-2,5) + аспірином ≤100 мг / добу + клопідогрелем 75 мг / добу
Довічно: антагоніст вітаміну К (МНВ 2,0-3,0)
|
|
ГКС
|
Стент без покриттяс
|
4 тижні: потрійна терапія антагоністом вітаміну К (МНВ 2,0-2,5) + аспірином ≤100 мг / добу + клопідогрелем 75 мг / добу
До 12 міс: комбінована терапія антагоністом вітаміну К (МНВ 2,0-2,5) і клопідогрелем 75 мг / добу (або аспірином 100 мг / добу)
Довічно: антагоніст вітаміну К (МНВ 2,0-3,0)
|
ГКС – гострий коронарний синдром. За необхідності слід проводити гастропротекцію за допомогою інгібітора протонної помпи
a Сиролімус, еверолімус, такролімус
b Альтернативою може бути комбінована терапія антагоністом вітаміну К (МНВ 2,0-3,0) і аспірином ≤100 мг / добу (у поєднанні з інгібітором протонної помпи за необхідності)
c По можливості слід уникати імплантації стентів з покриттям лікарськими засобами; якщо встановлений подібний стент, то обгрунтована більш тривала (3-6 міс) потрійна антитромботична терапія.
Lip et al. [61]
Коментар робочої групи:
Сиролімус станом на 01.10.2015р. в Україні не зареєстрований як лікарський засіб.
Згідно з правками до рекомендацій по веденню хворих з ФП та ГКС:
1. У разі розвитку ГКС у пацієнта, що приймає НПАК з приводу ФП, негайно тимчасово припинити прийом НПАК.
2. Негайно розпочати подвійну антитромбоцитарну терапію (ДАТТ) та призначити парентеральні антикоагулянти.
3. Якщо показані нові пероральні антикоагулянти, то інгібіторам Ха фактора (таким як ривароксабан) може бути надана перевага.
4. Оскільки переваги НПАК порівняно з АВК найімовірніше зберігаються у хворих із стабільною ішемічною хворобою серця (через рік після ГКС) НПАК можуть бути безпечною та ефективною альтернативою АВК
Таблиця 11. Стратегії антитромботичної терапії після стентування коронарних артерій у пацієнтів з ФП та помірним або високим ризиком тромбоемболічних подій (тих, кому показана терапія пероральними антикоагулянтами)
|
Ризик геморагічних ускладнень
|
Клінічна ситуація
|
Імплантований стент
|
Режим антикоагулянтної терапії
|
|
Низький або помірний (наприклад, 0-2 бали за шкалою HAS-BLED)
|
Планове ЧКВ
|
Стент без покриття
|
1 місяць: потрійна антитромботична терапія – АВК (МНВ 2,0-2,5) + аспірин ≤100 мг/добу + клопідогрель 75 мг/добу
Пожиттєво: монотерапія АВК (МНВ 2,0-3,0) або НПАК
|
|
Планове ЧКВ
|
Стент з покриттям
|
Від 3 (для стентів з покриттям засобами групи «-олімус»a) до 6 (для стентів з покриттям паклітакселом) місяців: потрійна антитромботична терапія – АВК (МНВ 2,0-2,5) + аспірин 100 мг/добу + клопідогрель 75 мг/добу
До 12 місяців: комбінація АВК (МНВ 2,0-2,5) або НПАК + клопідогрель 75 мг/добуb
(або аспірин 100 мг/добу)
Пожиттєво: монотерапія АВК (МНВ 2,0-3,0) або НПАК
|
|
ГКС
|
Стент без покриття / Стент з покриттям
|
6 місяців: потрійна антитромботична терапія – АВК (МНВ 2,0-2,5) + аспірин 100 мг/добу + клопідогрель 75 мг/добу
До 12 місяців: комбінація АВК (МНВ 2,0-2,5) або НПАК + клопідогрель 75 мг/добуb
(або аспірин 100 мг/добу)
Пожиттєво: монотерапія АВК (МНВ 2,0-3,0) або НПАК
|
|
Високий (наприклад, ≥3 балів за шкалою HAS-BLED)
|
Планове ЧКВ
|
Стент без покриттяc
|
2-4 тижні: потрійна антитромботична терапія – АВК (МНВ 2,0-2,5) + аспірин 100 мг/добу + клопідогрель 75 мг/добу
Пожиттєво: монотерапія АВК (МНВ 2,0-3,0) або НПАК
|
|
ГКС
|
Стент без покриттяc
|
4 тижні: потрійна антитромботична терапія – АВК (МНВ 2,0-2,5) + аспірин 100 мг/добу + клопідогрель 75 мг/добу
До 12 місяців: комбінація АВК (МНВ 2,0-2,5) або НПАК + клопідогрель 75 мг/добуb
(або аспірин 100 мг/добу)
Пожиттєво: монотерапія АВК (МНВ 2,0-3,0) або НПАК
|
За необхідності слід зважити доцільність захисту слизової оболонки шлунку інгібітором протонної помпи (ІПП).
aСіролімус, еверолімус та такролімус.
bУ якості альтернативи може застосовуватися комбінація АВК (МНВ 2,0-3,0) + аспірин ≤100 мг/добу (з ІПП за необхідності).
cПо можливості слід уникати застосування стентів з лікарським покриттям, але, якщо вони все ж застосовуються, показана більш тривала (3-6 місяців) потрійна антитромботична терапія.
Адаптовано за даними Lip et al.61
4.1.6.5 Планове черезшкірне втручання на коронарних артеріях
При плановому черезшкірному втручанні на коронарних артеріях стенти з лікарським покриттям слід застосовувати тільки в певних клінічних та / або анатомічних ситуаціях (протяжний стеноз, ураження дрібних судин, цукровий діабет та ін.), коли вони мають достовірні переваги перед металевими стентами. Після імплантації стента з покриттям лікарським препаратом протягом 4 тижнів проводять потрійну терапію антагоністом вітаміну К, аспірином і клопідогрелем. Після імплантації металевого стента без покриття пацієнтам з ФП і стабільною коронарною хворобою серця показана тривала терапія (12 міс) пероральним антикоагулянтом у поєднанні з клопідогрелем 75 мг / добу або аспірином 75-100 мг / добу. Одночасно з аспірином призначають інгібітори протонної помпи, блокатори Н2-рецепторів або антациди. Потрійну терапію слід продовжувати мінімум протягом 1 місяця після імплантації стента без покриття і значно довше після установки стента з лікарським покриттям (≥3 міс після імплантації стента, покритого сиролімусом, еверолімусом або такролімусом, і протягом ≥6 міс після установки стента з паклітакселом). Надалі продовжують лікування пероральним антикоагулянтом у поєднанні з клопідогрелем 75 мг / добу або аспірином 75-100 мг / добу, а також інгібіторами протонної помпи, блокаторами Н2-рецепторами або антацидами.
Якщо у пацієнтів з ФП, які отримують антикоагулянтну терапію, є середній або високий ризик тромбоемболій, то при черезшкірному втручанні на коронарній артерії може виявитися бажаним не переривати антикоагуляцію. У таких випадках слід використовувати доступ через променеву артерію навіть на тлі терапевтичної антикоагуляції (МНО 2-3).
4.1.6.6 Інфаркт міокарда без підйому сегмента ST
Пацієнтам з інфарктом міокарда без підйому сегмента ST рекомендується подвійна антитромбоцитарна терапія аспірином і клопідогрелем, однак хворим з ФП і помірним або високим ризиком інсульту доцільно призначати пероральні антикоагулянти. У гострій ситуації пацієнтам часто призначають аспірин, клопідогрель, НФГ або НМГ (наприклад, еноксапарин) або бівалірудин та / або блокатор глікопротеїнових IIb / IIIa рецепторів. Стенти з покриттям лікарськими препаратами слід імплантувати тільки в зазначених вище ситуаціях (див. Табл. 11). Переважно не переривати антикоагулянтну терапію і використовувати доступ через променеву терапію.
Потрійну терапію антагоністом вітаміну К, аспірином і клопідогрелем проводять протягом 3-6 міс або триваліше у пацієнтів з низьким ризиком кровотечі. У пацієнтів з високим ризиком серцево-судинних тромботичних ускладнень (оцінюють за допомогою індексів GRACE або TIMI) можлива тривала терапія антагоністом вітаміну К в комбінації з клопідогрелем 75 мг / добу (або аспірином 75-100 мг на тлі гастропротекціі) протягом 12 міс.
4.1.6.7 Первинне черезшкірне втручання при гострому інфаркті міокарда з підйомом сегмента ST
У гостру фазу таким пацієнтам часто призначають аспірин, клопідогрель і гепарин. При наявності великої тромбу можуть бути використані бівалірудин або блокатори глікопротеїнових рецепторів. Рекомендується механічне видалення тромбу (аспірація). Враховуючи високий ризик кровотеч на фоні комбінованої терапії, блокатори глікопротеїнових рецепторів і бівалірудин не застосовують, якщо МНВ становить> 2. Потрійну терапію антагоністом вітаміну К, аспірином і клопідогрелем продовжують протягом 3-6 міс або протягом більш тривалого терміну у пацієнтів з низьким ризиком кровотечі. У подальшому проводять терапію (до 12 міс) антагоністом вітаміну К і клопідогрелем 75 мг / добу (або аспірином 75-100 мг / добу на тлі гастропротекціі).
4.1.6.8 Гострий інсульт
Гострий інсульт нерідко виявляється першим проявом ФП, враховуючи частий безсимптомний перебіг аритмії. Тактика їх ведення вивчена недостатньо. Протягом перших 2-х тижнів після кардіоемболічного інсульту відзначається найвищий ризик рецидиву інсульту, пов'язаного з повторною тромбоемболією. Однак антикоагуляція в гостру фазу інсульту може призвести до розвитку внутрішньочерепної кровотечі або геморагічної трансформації інфаркту.
У пацієнтів з ФП і гострим інсультом або ТІА перед початком антикоагулянтної терапії слід забезпечити адекватний контроль артеріальної гіпертонії і провести КТ або магнітно-резонансну томографію головного мозку, щоб виключити кровотечу. При відсутності кровотечі антикоагуляцію починають через 2 тижні, однак при наявності кровотечі призначати антикоагулянти не слід. У пацієнтів з ФП і гострої ТІА антикоагулянтну терапію починають якомога швидше, якщо відсутні церебральний інфаркт або кровотеча.
Прихований інсульт
У хворих з ФП інсульт найчастіше має походження з причини емболії, тому виявлення безсимптомних церебральних емболій дозволяє виділити пацієнтів з високим ризиком тромбоемболії. За даними КТ / МРТ, частота прихованого інсульту у хворих з ФП вища, ніж у пацієнтів з синусовим ритмом. За допомогою транскраніальної доплерографії можна ідентифікувати пацієнтів з активним джерелом емболій або хворих, які перенесли інсульт, і у яких є високий ризик його рецидиву.
Коментар робочої групи:
Бівалірудин станом на 01.10.2015р. в Україні не зареєстрований як лікарський засіб.
При інфаркті мозку терміни початку або відновлення антикоагулянтної терапії залежать від розміру інфаркту: невеликий, неінвалідізуючий інфаркт – через 3 дні; великі інфаркти – не раніше, ніж через 2 (або навіть 3) тижні після перенесеного інсульту (умовне правило «1-3-6-12 днів»). При наявності крововиливу антикоагулянтна терапія взагалі не повинна призначатися. Якщо під час прийому ривароксабану або апіксабану мав місце ішемічний інсульт, лукар може розглянути вибір замість раніше призначених препаратів, дабігатрану етексилат 150 мг двічи на день.
4.1.6.9 Тріпотіння передсердь
Ризик інсульту при тріпотінні передсердь вивчався ретроспективно у великої кількості пацієнтів літнього віку. Він виявився подібним до такого, як у пацієнтів з ФП. Отже, рекомендації щодо тромбопрофілактики у пацієнтів з тріпотінням і фібриляцією передсердь однакові.
Коментар робочої групи:
4.1.6.10 Застосування антикоагулянтів до та після процедур абляції та імплантації пристроїв.
|
|
Алгоритм дії
|
Рівень доказів
|
|
Антиагреганти
|
|
|
|
Первина профілактика інфвркта міокарда
|
Відмінити антиагреганти за 3-7 діб до процедури, в залежності від препарата.
|
Нерандомізоване дослідження, думка експкртів
|
|
Подвійна антиагрегантна терапія після стентування або гострого коронарного синдрому
|
|
Нерандомізоване дослідження, думка експертів
|
|
Період невисокого ризику
|
Продовжити тільки аспірин (невисокий ризик ускладнень)
|
|
Період високого ризику
|
Продовжити терапію в повному обсязі (високий ризик ускладнень)
|
|
Терапія варфарином
|
Відмінити варфарин за 3-6 днів до процедури, або продовжувати під контролем МНВ (нижня межа рекомендованого МНВ), вирішує лікар в залежності від оцінки ризиків
|
Міжнародний консенсус експертів
|
|
Нові пероральні антикоагулянти
|
Відмінити за 1-3 дні до процедури або продовжити в залежності з оцінкою ризику. Відновити після досягнення надійного гемостазу.
|
Консенсус експертів
|
4.1.7 Кардіоверсія
Підвищений ризик тромбоемболій після кардіоверсії добре відомий. У зв'язку з цим антикоагуляцію вважають обов'язковою перед плановою кардіоверсією, якщо ФП зберігається більше 48 год або тривалість її не відома. На підставі результатів когортних досліджень лікування антагоністами вітаміну К (МНВ 2,0-3,0) слід продовжувати протягом принаймні 3-х тижнів до кардіоверсії. Тромбопрофілактика рекомендується перед електричною або медикаментозною кардіоверсією у пацієнтів з тривалістю ФП> 48 год. Терапію антагоністами вітаміну К слід продовжувати принаймні протягом 4-х тижнів після кардіоверсії, враховуючи ризик тромбоемболій, пов'язаний з дисфункцією лівого передсердя і його вушка (так зване «оглушення передсердь»). За наявності факторів ризику інсульту або рецидиву ФП лікування антагоністами вітаміну К проводять довічно навіть при збереженні синусового ритму після кардіоверсії.
Якщо епізод ФП триває менше 48 год, то кардіоверсію можна виконати в невідкладному порядку під прикриттям внутрішньовенного введення НФГ (з наступною інфузією або підшкірним введенням НМГ. У пацієнтів з факторами ризику інсульту (див. Розділ 4.1.1) лікування пероральними антикоагулянтами починають після кардіоверсії і продовжують довічно. НФГ або НМГ застосовують до тих пір, поки не буде досягнуто терапевтичне МНВ (2,0-3,0). За відсутності факторів ризику тромбоемболій призначати пероральні антикоагулянти не слід.
У пацієнтів з ФП > 48 год і порушенням гемодинаміки (стенокардія, інфаркт міокарда, шок або набряк легенів) слід провести невідкладну кардіоверсію. Перед відновленням ритму призначають НФГ або НМГ. Після кардіоверсії призначають пероральні антикоагулянти, а лікування гепарином продовжують до тих пір, поки не буде досягнуто терапевтичне МНВ (2,0-3,0). Тривалість антикоагулянтної терапії (4 тижні або довічно) залежить від наявності факторів ризику інсульту.
Коментар робочої групи:
Дані та клінічний досвід використання НПАК при кардіоверсії обмежені результатами аналізів підгруп та досвідом практичного застосування.
Частота та наслідки асоційовані з кардіоверсією (n=375) у пацієнтів у дослідженні ROCKET AF не відрізнялися у групах пацієнтів, які отримували ривароксабан або варфарин (інсульт або системна емболія: 1,42 vs 2,45% відповідно).
Частота інсульту та системної емболії у дослідженні RE-LY протягом 30 днів після кардіоверсії складала при використанні дабігатрану у дозі 110 мг та 150 мг два рази на добу 0,77% (5/647) та 0,30% (2/672), відповідно, і 0,60% (4/664) при застосуванні варфарину.
Накопичені дані свідчать про можливість виконання процедури кардіоверсії із використанням НПАК.
Виходячи з результатів досліджень нових антикоагулянтів – ривароксабану (X-VeRT, субаналіз ROCKET AF) та дабігатрану (субаналіз RE-LY), дані препарати порівняно з варфарином, в меншому відсотку випадків асоціюються із великими кровотечами. У дослідженні X-VeRT отримано достовірні дані, що використання ривароксабану дозволяє значно скоротити терміни підготовки до кардіоверсії за рахунок відсутності необхідності підбору дози.
Ефективність та безпека використання ривароксабану при підготовці до кардіоверсії вивчені у проспективному рандомізованому дослідженні X-VeRT (n=1504). В ході дослідження пацієнтам виконували ранню (58 %) або відстрочену (42 %) кардіоверсію. Результати дослідження показали зіставну частоту первинної кінцевої точки, що включала інсульт, транзиторну ішемічну атаку, периферичну емболію, ІМ та кардіоваскулярну смерть, у пацієнтів групи ривароксабану і АВК (0,5 % vs 1,02 % відповідно). За частотою великих кровотеч достовірні відмінності між ривароксабаном і АВК були відсутні (0,61 vs 0,80 % відповідно). Також групи терапії не розрізнялися за загальною частотою несприятливих подій і важких побічних ефектів. У групі відстроченої процедури у пацієнтів, які отримували ривароксабан, середній час очікування кардіоверсії був значно коротшим, ніж у хворих, що приймали АВК (22 vs 30 днів відповідно; р<0,001), що було обумовлено труднощами з підтриманням МНО в цільовому діапазоні при прийомі АВК.
Дані та клінічний досвід використання інших НПАК при кардіоверсії обмежені результатами аналізів підгруп та досвідом практичного застосування.
Частота та наслідки, асоційовані з кардіоверсією (n=743), у пацієнтів (n=540) у дослідженні ARISTOTLE не відрізнялися у групах пацієнтів, які отримували апіксабан або варфарин: випадків інсульту або системної емболії не було зафіксовано ні в одній групі, випадки інфаркту міокарда або серйозної кровотечі були нечисленні (відповідно 0,3% проти 0,2%).
Частота інсульту та системної емболії у дослідженні RE-LY протягом 30 днів після кардіоверсії при використанні дабігатрану у дозі 110 мг та 150 мг два рази на добу становила відповідно 0,77 % (5/647) та 0,30 % (2/672) і 0,60 % (4/664) при застосуванні варфарину.
Отримані дані свідчать про можливість виконання процедури кардіоверсії із використанням НПАК.
Рекомендації щодо профілактики тромбоемболій
|
Рекомендації
|
Клас
|
Рівень
|
Джерело
|
|
Всім хворим з ФП рекомендується антитромботична терапія для профілактики тромбоемболій; виняток становлять пацієнти групи низького ризику (ізольована ФП, вік <65 років або протипоказання)
|
I
|
А
|
47,48,63
|
|
Антитромботичну терапію вибирають з урахуванням абсолютного ризику інсульту / тромбоемболій і кровотечі і коефіцієнта користь / ризик
|
I
|
А
|
47,48,50
|
|
Для початкової оцінки ризику інсульту у пацієнтів з неклапанною ФП рекомендується застосування індексу, що легко запам'ятовується CHADS2 [серцева недостатність, гіпертонія, вік, діабет, інсульт (подвоєний ризик)]
|
I
|
A
|
50
|
|
· У пацієнтів з індексом CHADS2≥2 рекомендується терапія пероральними антикоагулянтами (за відсутності протипоказань); цільовий діапазон МНВ становить 2,0-3,0 (2,5)
|
I
|
A
|
47,48,54
|
|
Для більш детальної оцінки ризику інсульту у хворих з ФП (наприклад, індекс CHADS2 0-1) необхідно враховувати основні та клінічно значущі неосновні фактори ризику
|
I
|
A
|
52
|
|
· У пацієнтів з 1 основним і ≥2 клінічно значущими неосновними факторами ризику є високий ризик, тому за відсутності протипоказань їм рекомендується антикоагулянтна терапія (при призначенні антагоністів вітаміну К цільове МНВ становить 2,0-3,0)
|
I
|
A
|
52
|
|
· У пацієнтів з 1 клінічно значущим неосновним чинником ризику є середній ризик, тому їм рекомендується антитромботична терапія
|
I
|
A/B
|
52
|
|
1. Пероральні антикоагулянти (наприклад, антагоністи вітаміну К) або
|
I
|
A
|
52
|
|
2. Аспірин 75-325 мг/добу
|
I
|
B
|
48
|
|
· За відсутності факторів ризику (в основному пацієнти віком <65 років з ізольованою ФП без будь-яких факторів ризику) є низький ризик, тому в таких випадках застосовують аспірин у дозі 75-325 мг / добу або не призначають антитромботичну терапію
|
I
|
B
|
52
|
|
У пацієнтів з ФП і штучними клапанами серця цільову інтенсивність антикоагуляції вибирають з урахуванням типу і локалізації протезу; за наявності протезу мітрального клапана цільове МНВ становить принаймні 2,5, аортального клапана – принаймні 2,0
|
I
|
B
|
63,64
|
|
Пацієнтам з тріпотінням передсердь, як і ФП, показана антитромботична терапія
|
I
|
C
|
|
|
Антитромботичну терапію вибирають на підставі однакових критеріїв незалежно від типу ФП (пароксизмальна, персистуюча або постійна)
|
IIa
|
A
|
47,48
|
|
Більшості пацієнтів з одним клінічно значущим неосновним чинником ризику показана терапія пероральними антикоагулянтами (наприклад, антагоністом вітаміну К), а не аспірином, з урахуванням ризику геморагічних ускладнень, можливість безпечної хронічної антикоагуляції і переваг пацієнта
|
IIa
|
A
|
47,48
|
|
У пацієнтів з низьким ризиком (в основному пацієнти віком <65 років з ізольованою ФП без факторів ризику) переважно відмовитися від антитромботичної терапії, а не призначати аспірин
|
IIa
|
B
|
47,48
|
|
Якщо пацієнт відмовляється від прийому пероральних антикоагулянтів, або є очевидні протипоказання до їх призначення (наприклад, нездатність адекватно контролювати антикоагуляцію), а ризик кровотеч низький, показана комбінована терапія аспірином 75-100 мг і клопідогрелем 75 мг / добу
|
IIa
|
B
|
58
|
|
Перед призначенням антитромботичних засобів (як антагоністів вітаміну К, так і аспірину) необхідно оцінювати ризик кровотеч; його слід вважати подібним при лікуванні аспірином і антагоністом вітаміну К, особливо у літніх людей
|
IIa
|
A
|
56,60,65
|
|
Для розрахунку ризику кровотечі використовують індекс HAS-BLED (гіпертонія, порушення функції нирок / печінки, інсульт, кровотечі в анамнезі або схильність до кровотечі, лабільне МНВ, вік старших за 65 років, супутній прийом ліків / алкоголю); значення індексу ≥3 вказує на високий ризик кровотечі. У таких випадках після призначення перорльних антикоагулянтів або аспірину слід дотримуватися обережності і регулярно спостерігати за пацієнтом
|
IIa
|
B
|
60
|
|
У пацієнтів з ФП, у яких відсутній штучний клапан серця або високий ризик тромбоемболій, при хірургічних та діагностичних втручаннях, що супроводжуються загрозою кровотечі, доцільно перервати терапію пероральними антикоагулянтами (субтерапевтична антикоагуляція протягом 48 год) і не призначати гепарин
|
IIa
|
C
|
|
|
У пацієнтів з ФП і штучним клапаном серця або високим ризиком тромбоемболій при хірургічних або діагностичних втручаннях доцільно перервати терапію пероральними антикоагулянтами і призначити НМГ або нефракціонований гепарин
|
IIa
|
C
|
|
|
Після оперативних втручань терапію пероральними антикоагулянтами відновлюють до звичайної підтримуючої дози (без навантажувальної дози) ввечері (або наступного дня) в день операції за умови адекватного гемостазу
|
IIa
|
B
|
|
|
Необхідно регулярно оцінювати користь, ризик і необхідність подальшої антитромботичної терапії
|
IIa
|
C
|
|
|
У пацієнтів з ФП і гострим інсультом або ТІА перед призначенням антитромботичної терапії доцільно домогтися контролю артеріальної гіпертонії і провести комп'ютерну томографію або магнітно-резонансну томографію для виключення кровотечі в головний мозок
|
IIa
|
C
|
|
|
За відсутності кровотечі терапію пероральними антикоагулянтами проводять протягом приблизно 2-х тижнів після інсульту, однак за наявності кровотечі призначати антикоагулянти не слід
|
IIa
|
C
|
|
|
За наявності великого мозкового інфаркту доцільно відкласти антикоагуляцію, враховуючи ризик геморагічної трансформації
|
IIa
|
C
|
|
|
У пацієнтів з ФП і гострою ТІА терапію пероральними антикоагулянтами слід починати якомога раніше за відсутності церебрального інфаркту або кровотечі
|
IIa
|
C
|
|
|
Деяким пацієнтам з 1 клінічно значущим неосновним факторам ризику, наприклад, жінкам у віці <65 років без інших факторів ризику, замість пероральних антикоагулянтів може бути призначений аспірин
|
IIb
|
C
|
|
|
Якщо під час хірургічного втручання доводиться переривати терапію антикоагулянтами більш ніж на 48 год у пацієнтів високого ризику, можливе застосування НФГ або підшкірно НМГ
|
IIb
|
C
|
|
|
Якщо у пацієнта з ФН на тлі звичайної антикоагулянтної терапії (МНВ 2,0-3,0) розвивається ішемічний інсульт або системна емболія, то можливе збільшення інтенсивності антикоагуляції (МНВ 3,0-3,5), а не приєднання антитромбоцитарного препарату
|
IIb
|
C
|
|
Основними вважають фактори ризику, які асоціюються з найвищим ризиком інсульту у хворих з ФП: тромбоемболії (інсульт, ТІА або системні емболії) в анамнезі, вік ≥75 років і ревматичний мітральний стеноз. Клінічно значущі неосновні фактори ризику включають в себе артеріальну гіпертонію, серцеву недостатність або помірну / виражену дисфункцію ЛШ (фракція викиду ≤40%) і цукровий діабет (рівень доказів А). Іншими клінічно значущими неосновними факторами ризику вважають жіночу стать, вік 65-74 роки, захворювання судин (інфаркт міокарда, бляшка аорти, поразка сонних і периферичних артерій). Цю схему оцінки ризику у пацієнтів з неклапанною ФП позначають акронімом CHA2DS2-VASc [серцева недостатність, гіпертонія, вік ≥75 років (подвоєння ризику), діабет, інсульт (подвоєння ризику), захворювання судин, вік 65-74 роки і жіноча стать]. Інсульту / ТІА в анамнезі і віку ≥75 років привласнюють 2 бали, а віку 65-74 роки, артеріальній гіпертонії, діабету, серцевій недостатності, захворюванню судин (інфаркт міокарда, захворювання периферичних артерій, бляшка в аорті) або жіночій статі – по 1 балу.
Рекомендації щодо антитромботичної терапії у хворого з ФП при ГКС / черезшкірному втручанні в коронарні артерії
|
Рекомендації
|
Клас
|
Рівень
|
Джерело
|
|
При плановому ЧКВ у пацієнтів з ФП і стабільною коронарною хворобою серця доцільно імплантувати стент без лікарського покриття. Застосування стентів з покриттям лікарським препаратом слід уникати. Їх доцільно імплантувати в певних клінічних та / або анатомічних ситуаціях (наприклад, стеноз великої протяжності, ураження дрібних судин, діабет і т.д.), коли вони мають значні переваги перед стентами без покриття
|
IIa
|
C
|
|
|
Після планового ЧКВ на короткий термін призначають потрійну терапію (антагоніст вітаміну К, аспірин та клопідогрель), а потім продовжують (до 1 року) лікування антагоністом вітаміну К і клопідогрелем 75 мг / добу (або аспірином 75-100 мг / добу в поєднанні з інгібітором протонної помпи, блокатором Н2-рецепторів або антацидом)
|
IIa
|
C
|
|
|
Після планового ЧКВ клопідогрель в комбінації з антагоністом вітаміну К і аспірином доцільно застосовувати протягом принаймні 1 міс після імплантації стента без покриття лікарськими препаратами і протягом більш тривалого терміну після установки стента з покриттям лікарським препаратом (принаймні 3 міс. після імплантації стента з покриттям сиролімус і принаймні 6 місяців після імплантації стента з покриттям паклітакселом); в подальшому за необхідності продовжують терапію антагоністом вітаміну К і клопідогрелем 75 мг / добу (або аспірином 75-100 мг / добу в поєднанні з інгібітором протонної помпи, блокатором Н2-рецепторів або антацидом)
|
IIa
|
C
|
|
|
Після ГКС під час ЧКВ хворим з ФП призначають потрійну терапію (антагоністом вітаміну К, аспірином, клопідогрелем) на короткий термін (3-6 міс) або більш тривалий час при низькому ризику тромбоемболії; в подальшому продовжують терапію антагоністом вітаміну К і клопідогрелем 75 мг / добу (або аспірином 75-100 мг / добу в поєднанні з інгібітором протонної помпи, блокатором Н2-рецепторів або антацидом)
|
IIa
|
C
|
|
|
У пацієнтів з дуже високим ризиком тромбоемболій, які отримують антикоагулянтну терапію, бажано не переривати лікування антагоністом вітаміну К під час ЧКВ і використовувати променевий доступ навіть на тлі терапевтичної антикоагуляції (МНВ 2-3)
|
IIa
|
C
|
|
|
Якщо антагоніст вітаміну К призначають у комбінації з клопідогрелем або аспірином у низькій дозі, необхідно ретельно контролювати інтенсивність антикоагуляції (МНВ 2,0-2,5)
|
IIb
|
C
|
|
|
Після реваскуляризації у пацієнтів з ФП протягом 12 міс може застосовуватися антагоніст вітаміну К в поєднанні з одним антитромбоцитарним препаратом, однак ця стратегія ретельно вивчалася і асоціюється з підвищеним ризиком кровотеч
|
IIb
|
C
|
|
|
У пацієнтів зі стабільним захворюванням судин (відсутність гострих подій протягом> 1 року) можлива монотерапія антагоністом вітаміну К; якщо в подальшому не розвиваються серцево-судинні події, призначати антитромбоцитарні препарати не слід
|
IIb
|
C
|
|
Рекомендації щодо антикоагуляції перед і після кардіоверсії
|
Рекомендації
|
Клас
|
Рівень
|
Джерело
|
|
Якщо тривалість нападу ФП становить ≥48 год або не відома, то протягом принаймні 3-х тижнів перед кардіоверсією і 4-х тижнів після втручання необхідно проводити терапію пероральними антикоагулянтами незалежно від методу відновлення ритму (дефібриляція або пероральне / внутрішньовенне введення антиаритмічних засобів)
|
I
|
B
|
63
|
|
Якщо пацієнту з ФП і порушеною гемодинамікою потрібна негайна кардіоверсія, то рекомендується застосування гепарину (внутрішньовенне введення у вигляді болюса і подальша інфузія) або НМГ у терапевтичній дозі
|
I
|
C
|
|
|
Якщо тривалість нападу ФП становить ≥48 год або не відома, то після невідкладної кардіоверсії рекомендується проводити терапію пероральними антикоагулянтами протягом принаймні 4-х тижнів (як і після планового відновлення синусового ритму)
|
I
|
B
|
63
|
|
Пацієнтам з тривалістю нападу ФП <48 год і високим ризиком інсульту при кардіоверсії рекомендується внутрішньовенне введення гепарину або застосування НМГ у терапевтичній дозі, а потім тривала терапія пероральними антикоагулянтами (МНВ2,0-3,0)
|
I
|
B
|
47,54,63
|
|
Якщо тривалість нападу ФП становить ≥48 год, то терапію пероральними антикоагулянтами продовжують протягом принаймні 4-х тижнів після невідкладної кардіоверсії (як і при плановому відновленні синусового ритму)
|
I
|
B
|
63
|
|
У пацієнтів з високим ризиком інсульту рекомендується тривала терапія антагоністом вітаміну К (МНВ 2,0-3,0)
|
I
|
B
|
47,54,63
|
|
Альтернативою антикоагуляції перед відновленням ритму є кардіоверсія під контролем черезстравохідної ехокардіографії, яка дозволяє виключити тромб у лівому передсерді або його вушку
|
I
|
B
|
42
|
|
Якщо під час черезстравохідної ехокардіографії не виявлено тромб, то кардіоверсію можна провести негайно після початку антикоагуляції гепарином. Протягом принаймні 4-х тижнів після антикоагуляції проводять терапію пероральними антикоагулянтами (гепарин відміняють, коли буде досягнуто цільове МНВ)
|
I
|
B
|
42
|
|
Якщо під час черезстравохідної ехокардіографії виявлено тромб, то протягом принаймні 3-х тижнів проводять лікування антагоністом вітаміну К (МНВ 2,0-3,0); потім повторюють ехокардіографію, щоб підтвердити розчинення тромба
|
I
|
C
|
|
|
При кардіоверсії у пацієнтів з тріпотінням передсердь рекомендована схема антикоагуляції відповідає такій у хворих з ФП
|
I
|
C
|
|
|
У пацієнтів з факторами ризику інсульту або рецидиву ФП терапію пероральними антикоагулянтами продовжують довічно, навіть якщо стійко зберігається синусовий ритм
|
IIa
|
B
|
63
|
|
Якщо при повторній черезстравохідній ехокардіографії виявлено розчинення тромбу, то слід провести кардіоверсію і продовжити прийом пероральних антикоагулянтів протягом 4-х тижнів або довічно (за наявності факторів ризику)
|
IIa
|
C
|
|
|
Якщо за даними черезстравохідної ехокардіографії зберігається тромб, то можна вибрати альтернативну стратегію лікування (контроль частоти серцевих скорочень)
|
IIb
|
C
|
|
|
Якщо тривалість ФП становить <48 год і відсутні фактори ризику тромбоемболій, то до і після кардіоверсії можуть бути використані гепарин в / в або НМГ у терапевтичній дозі (пероральна антикоагуляція після відновлення синусового ритму не потрібно)
|
IIb
|
C
|
|
4.1.7.1 Кардіоверсія під контролем черезстравохідної ехокардіографії
Обов'язкова 3-тижнева антикоагуляція може бути скорочена, якщо при черезстравохідній ехокардіографії не буде виявлено тромб у лівому передсерді або вушку лівого передсердя. За допомогою цього методу можна виявити не тільки тромб у вушку лівого передсердя або в інших ділянках цієї камери серця, а й спонтанні ехосигнали або бляшку в аорті. Кардіоверсія під контролем черезстравохідної ехокардіографії може служити альтернативою 3-тижневої антикоагуляції перед відновленням ритму, а також у тих випадках, коли необхідна рання кардіоверсія, антикоагуляція не можлива (відмова пацієнта або високий ризик кровотеч) або є висока ймовірність тромбу в лівому передсерді або його вушку [42]. Якщо при черезстравохідній ехокардіографії тромб у лівому передсерді не виявлений, то перед кардіоверсією призначають НФГ або НМГ, введення яких продовжують до тих пір, поки не буде досягнуто цільове МНВ на фоні прийому пероральних антикоагулянтів.
Коментар робочої групи:
Як альтернатива при проведенні кардіоверсії можливо використання НПАК (ривароксабану, дабигатрану та ін.)
За наявності тромбу в лівому передсерді або у вушку лівого передсердя слід проводити лікування антагоністом вітаміну К (МНВ 2,0-3,0) і повторити черезстравохідну ехокардіографію. При розчиненні тромбу може бути проведена кардіоверсія, після якої призначають довічну терапію пероральними антикоагулянтами. Якщо тромб зберігається, можна відмовитися від відновлення ритму на користь контролю частоти шлуночкового ритму, особливо якщо симптоми ФП контролюються, враховуючи високий ризик тромбоемболій на фоні кардіоверсії (рис. 5).
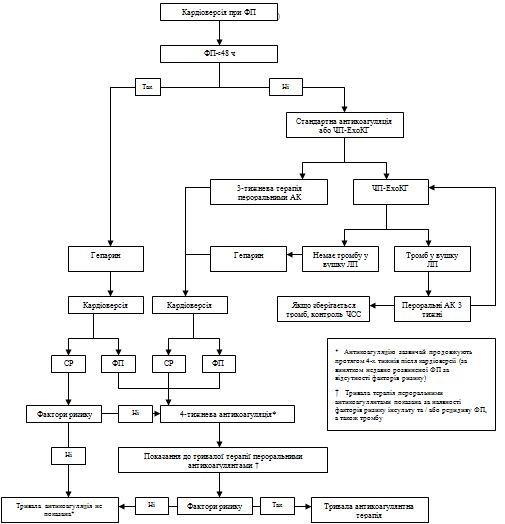
Рис. 5. Кардіоверсія у хворих з ФП і стабільною гемодинамікою. Роль кардіоверсії під контролем черезстравохідної ехокардіографії (ПП-ЕхоКГ) і стратегія подальшої антикоагуляції.
СР – синусовий ритм, АК – антикоагулянти
Коментар робочої групи:
Згідно з правками рекомендацій ESC 2012 та EHRA 2013 років
Загальні рекомендації з профілактики тромбоемболій
|
Рекомендації
|
Класa
|
Рівеньb
|
|
Антитромботична терапія з метою профілактики ТЕУ рекомендована всім пацієнтам з ФП, за винятком тих, у яких спостерігається низький ризик ТЕУ (ізольована ФП, вік <65 років незалежно від статі, або наявність протипоказань до антитромботичної терапії).
|
I
|
А
|
|
Рекомендується, щоб вибір стратегії антитромботичної терапії ґрунтувався на абсолютному ризику інсульту / ТЕУ та геморагічних ускладнень та на відносному ризику та користі для конкретного пацієнта.
|
I
|
А
|
|
Пацієнтам з ФП, які мають механічні протези клапанів серця, рекомендовано при виборі цільової інтенсивності антикоагуляції при терапії АВК враховувати тип та локалізацію протезу, підтримуючи МНВ на рівні принаймні 3,0 у випадку протезу мітрального клапану та принаймні 2,5 у випадку протезу аортального клапану.
|
I
|
В
|
|
Пацієнтам з тріпотінням передсердь рекомендована така ж стратегія антитромботичної терапії, як і пацієнтам з ФП.
|
I
|
C
|
|
Рекомендується використовувати шкалу CHA2DS2-VASc для оцінки ризику інсульту у пацієнтів з неклапанною ФП
|
I
|
А
|
|
Пацієнти, що мають за шкалою CHA2DS2-VASc 0 балів (без факторів ризику інсульту (переважно це пацієнти віком <65 років з ізольованою ФП) мають низький ризик, їм не рекомендований прийом антитромботичної терапії.
|
I
|
В
|
|
Пацієнтам з ≥2 балів за шкалою CHA2DS2-VASc рекомендована постійна терапія ПАК
• за допомогою АВК з коригованим дозуванням, спрямованим на досягнення МНВ в діапазоні 2,0-3,0, або
• прямий інгібітор фактору Ха (ривароксабан), або
• прямий інгібітор тромбіну (дабігатран),
якщо до такої терапії немає протипоказань.
|
I
|
А
|
|
Пацієнтам з 1 балом за шкалою CHA2DS2-VASc постійна терапія ПАК
• за допомогою АВК з коригованим дозуванням, спрямованим на досягнення МНВ в діапазоні 2,0-3,0, або
• прямий інгібітор фактору Ха (ривароксабан), або
• прямий інгібітор тромбіну (дабігатран),
має бути розглянута з урахуванням оцінки ризику кровотеч та особливостей пацієнта.
|
IIa
|
А
|
|
Пацієнти жіночої статі віком <65 років з ізольованою ФП без факторів ризику (що мають 1 бал за шкалою CHA2DS2-VASc відповідно їх статі) відносяться до групи низького ризику, тому слід зважити доцільність відсутності антитромботичної терапії у таких пацієнтів.
|
IIa
|
В
|
|
Вибір стратегії антитромботичної терапії повинен проводитися із врахуванням однакових критеріїв, незалежно від характеру перебігу ФП (тобто, незалежно від того, чи є ФП пароксизмальною, персистуючою чи постійною).
|
IIa
|
В
|
|
Якщо пацієнти відмовляються від будь-якої терапії ПАК (АВК або НПАК), слід розглянути доцільність застосування комбінованої антитромбоцитарної терапії аспірином 100 мг/добу і клопідогрелем 75 мг/добу (за умови низького ризику геморагічних ускладнень), або менш ефективної монотерапії аспірином 100-325 мг/добу
|
IIa
|
В
|
|
Через регулярні інтервали часу показано проводити переоцінки користі антитромботичної терапії, пов'язаних з нею ризиків та потреби у ній.
|
IIa
|
C
|
Рекомендації з профілактики тромбоемболій з використанням НПАК
|
Якщо у пацієнтів з ФП неможливе використання АВК (МНВ 2,0-3,0) внаслідок складностей у підтриманні терапевтичного діапазону МНВ, розвитку побічних ефектів на АВК у минулому, або неможливості регулярного моніторингу МНВ, один з НПАК:
• прямий інгібітор фактора Ха (ривароксабан), або
• прямий інгібітор тромбіну (дабігатран)
має бути рекомендований.
|
I
|
В
|
|
Більшості пацієнтів з неклапанною ФП, яким рекомендована антикоагулянтна терапія, слід віддавати перевагу будь-якому НПАК:
• прямому інгібітору фактора Ха (ривароксабану), або
• прямому інгібітору тромбіну (дабігатрану)
перед АВК з коригованим дозуванням (МНВ 2,0-3,0)
|
IIa
|
А
|
|
Коли показане застосування ривароксабану, дозування 20 мг один раз на добу має бути рекомендоване більшості пацієнтів за виключенням випадків, коли доцільне застосування дози 15 мг один раз на добу:
• високий ризик кровотеч (бал за шкалою HAS-BLED ≥3),
• ниркова недостатність середнього ступеня (кліренс креатиніну 15-49 мл/хв).
|
IIa
|
С
|
|
Коли показане застосування дабігатрану, дозування 150 мг два рази на добу має бути рекомендоване більшості пацієнтів за виключенням випадків, коли доцільне застосування дози 110 мг два рази на добу:
• пацієнти віком ≥80 років,
• сумісне застосування препаратів, що можуть взаємодіяти (напр., верапаміл та ін.),
• високий ризик кровотеч (бал за шкалою HAS-BLED ≥3),
• ниркова недостатність середнього ступеня (кліренс креатиніну 30-49 мл/хв).
|
IIa
|
С
|
|
Початкове та подальше регулярне обстеження функції нирок (за кліренсом креатиніну) рекомендується пацієнтам, які починають антикоагулянтну терапію будь-яким НПАК. При кліренсі креатиніну 50 мл/хв та вище пацієнт повинен спостерігатися у лікаря кожні півроку, при кліренсі креатиніну 30 – 49 мл/хв – кожні 3 місяці.
|
ІІа
|
С
|
|
При кліренсі креатиніну менш 30 мл/хв призначення НПАК не рекомендоване.
|
ІІІ
|
А
|
Рекомендації з профілактики тромбоемболій – кровотечі та «bridging»-терапія
|
Рекомендоване проведення оцінки ризику геморагічних ускладнень при призначенні антитромботичної терапії (незалежно від того, призначається АВК, НПАК або аспірин)
|
I
|
А
|
|
Для оцінки ризику геморагічних ускладнень показане використання шкали HAS-BLED (враховує наявність артеріальної гіпертензії, дисфункції нирок/печінки, інсульту, геморагічних ускладнень в анамнезі або схильності до геморагічних ускладнень, лабільне МНВ, похилий вік [>65 років], одночасне застосування інших лікарських засобів / зловживання алкоголем), де ≥3 балів вказують на «високий ризик» і вимагають особливої обережності та регулярного перегляду ризику пацієнта після початку застосування антитромботичної терапії, незалежно від того, проводиться вона ПАК або аспірином.
|
IIa
|
А
|
|
Фактори ризику кровотеч, що можуть бути модифіковані (неконтрольована артеріальна гіпертензія, лабільне МНВ, якщо пацієнт на АВК, сумісне застосування ліків (НПЗЗ та ін.), алкоголю та ін.) мають бути відкореговані.
|
ІІа
|
В
|
|
Шкала HAS-BLED повинна використовуватися для ідентифікації факторів ризику кровотеч, на які потрібно вплинути, але не повинна використовуватися для прийняття рішення щодо призначення або не призначення антитромботичної терапії
|
ІІа
|
В
|
|
Ризик геморагічних ускладнень на фоні застосування антитромботичної терапії (комбінація аспірину з клопідогрелем та особливо у літніх пацієнтів, а також монотерапія аспірином) повинен розглядатися як подібний до такого ризику на фоні застосування ПАК.
|
IIa
|
В
|
|
У пацієнтів з ФП без механічних протезів клапанів серця або без високого ризику ТЕУ, яким показане хірургічне втручання або інвазивна діагностична процедура, що обумовлює ризик кровотечі, слід розглянути доцільність тимчасового припинення прийому ПАК (із субтерапевтичною антикоагуляцією протягом періоду до 48 год), без заміни гепарину у якості «перехідної» антикоагулянтної терапії.
|
IIa
|
C
|
|
У пацієнтів з механічними протезами клапанів серця або з ФП з високим ризиком ТЕУ, яким показане хірургічне втручання або інвазивна діагностична процедура, слід зважити доцільність проведення «перехідної» антикоагулянтної терапії терапевтичними дозами або НМГ, або нефракціонованого гепарину при тимчасовому припиненні прийому терапії ПАК.
|
IIa
|
C
|
|
Після проведеного оперативного втручання слід зважити доцільність відновлення терапії ПАК у «звичайній» підтримуючій дозі (без застосування навантажувальної дози) ввечері того дня, коли було проведене втручання (або наступного ранку), за умови адекватного гемостазу.
|
IIa
|
В
|
|
Якщо у пацієнтів високого ризику хірургічне втручання вимагає тимчасового припинення терапії ПАК на період, більший за 48 год, може бути призначений нефракціонований гепарин або підшкірне введення НМГ.
|
IIb
|
C
|
Рекомендації з вторинної профілактики тромбоемболій
|
У пацієнтів з ФП, у яких розвивається гострий інсульт або ТІА, перед початком антитромботичної терапії показане належне лікування неконтрольованої артеріальної гіпертензії, і для виключення крововиливу у мозок проводиться нейровізуалізаційне дослідження (комп’ютерна томографія або магнітно-резонансна томографія).
|
IIa
|
C
|
|
За умови відсутності крововиливу у мозок слід зважити доцільність призначення терапії ПАК через ~2 тижні після інсульту, але при наявності крововиливу у мозок антикоагулянтна терапія не показана.
|
IIa
|
C
|
|
При наявності великого інфаркту головного мозку слід зважити доцільність відкладення початку антикоагулянтної терапії, беручи до уваги ризик геморагічної трансформації інфаркту.
|
IIa
|
C
|
|
У пацієнтів з ФП та гострою ТІА слід зважити доцільність призначення терапії ПАК якомога раніше, за умови відсутності інфаркту головного мозку або крововиливу у мозок.
|
IIa
|
C
|
|
У пацієнтів з ФП, у яких на фоні терапії АВК із звичайною інтенсивністю антикоагуляції (МНВ 2,0-3,0) розвинувся ішемічний інсульт або системний емболізм, може бути зважена доцільність підвищення інтенсивності антикоагуляції до максимальних цільових рівнів МНВ (3,0-3,5), а не додавання до схеми лікування антитромбоцитарного засобу.
|
IIb
|
C
|
aКлас рекомендації.
bРівень доказовості.
Ризик-орієнтований підхід до оцінки ризику при неклапанній ФП може бути відображений у вигляді акроніма CHA2DS2-VASc (шкала оцінки ризику, що враховує наявність серцевої недостатності, артеріальної гіпертензії, вік ≥75 років [два бали], наявність цукрового діабету, інсульту [два бали], судинних захворювань, вік 65–74 років та стать [жіноча]). Ця схема оцінки ризику ґрунтується на бальній системі, при якій по 2 бали призначаються за інсульт або ТІА в анамнезі та за вік ≥75 років і по 1 балу призначається за наявність у пацієнта артеріальної гіпертензії, цукрового діабету, серцевої недостатності, атеросклеротичного ураження судин (інфаркту міокарда, захворювання периферичних артерій, ускладненої аортальної атеросклеротичної бляшки) та за приналежність до жіночої статі.
Рекомендації з антитромботичної терапії на фоні ФП та ГКС/ЧКВ
|
Рекомендації
|
Класa
|
Рівеньb
|
|
При виконанні планового ЧКВ у пацієнтів з ФП та стабільним коронарним атеросклерозом слід зважити доцільність імплантації стенту без покриття (СБП), а застосування стентів з покриттям слід уникати або суворо обмежувати його деякими клінічними ситуаціями та/або анатомічними особливостями пацієнта (наприклад, ураження досить великих фрагментів артерій, ураження дрібних судин, наявність цукрового діабету та _н..), коли від застосування таких стентів очікуються суттєві переваги у порівнянні із СБП.
|
Iia
|
C
|
|
Після планового ЧКВ слід зважити доцільність призначення потрійної антитромботичної терапії (АВК, аспірин, клопідогрель) на короткий період часу, після чого показане застосування тривалої антитромботичної терапії (тривалістю до 1 року) ПАК у комбінації з клопідогрелем 75 мг/добу (або, у якості альтернативи, з аспірином ≤100 мг/добу, плюс гастропротективний лікарський засіб – ІПП).
|
IIa
|
C
|
|
Після планового ЧКВ слід зважити доцільність призначення застосування клопідогрелю у комбінації з ПАК і аспірином протягом принаймні 1 місяця після імплантації СБП і на більш тривалий період часу після імплантації стенту з покриттям (протягом принаймні 3 місяців після імплантації стенту з покриттям сиролімусом і протягом принаймні 6 місяців після імплантації стенту з покриттям паклітакселом); після чого за необхідності слід зважити доцільність призначення ПАК та клопідогрелю 75 мг/добу (або, у якості альтернативи, з аспірином ≤100 мг/добу, плюс гастропротективний лікарський засіб – ІПП).
|
IIa
|
C
|
|
Після ГКС з або без ЧКВ у пацієнтів з ФП слід зважити доцільність призначення потрійної антитромботичної терапії (АВК, аспірин, клопідогрель) на короткий період часу (3-6 місяців) або на довший термін у окремих пацієнтів з низьким ризиком геморагічних ускладнень, після чого показана тривала терапія ПАК та клопідогрелем 75 мг/добу (або, у якості альтернативи, з аспірином ≤100 мг/добу, плюс гастропротективний лікарський засіб – ІПП).
|
IIa
|
C
|
|
У пацієнтів з дуже високим ризиком ТЕУ, які отримують антикоагулянтну терапію, слід надавати перевагу безперервній терапії ПАК та застосування процедури ЧКВ з радіальним доступом у якості втручання першого вибору навіть на фоні терапевтичної антикоагуляції АВК (МНВ 2-3).
|
IIa
|
C
|
|
При застосуванні АВК у комбінації з клопідогрелем або низькими дозами аспірину можна зважити доцільність обережного коригування інтенсивності антикоагуляції в межах діапазону МНВ 2,0-2,5.
|
IIb
|
C
|
|
Після реваскуляризаційного втручання у пацієнтів з ФП може бути зважена доцільність застосування ПАК з одним із антитромбоцитарних засобів у перші 12 місяців після втручання, але на сьогоднішній день ця стратегія не вивчена ретельно та асоційована з підвищеним ризиком геморагічних ускладнень.
|
IIb
|
C
|
|
У пацієнтів із стабільним атеросклеротичним ураженням судин (наприклад, що триває протягом >1 року без гострих подій) може бути зважена доцільність монотерапії ПАК, і супутня антитромбоцитарна терапія при цьому може не призначатися за умови відсутності у подальшому серцево-судинних подій. Перевагу в цьому разі доцільно віддавати інгібітору фактора Ха (ривароксабану та ін.).
|
IIb
|
C
|
aКлас рекомендації.
bРівень доказовості.
Рекомендації з антикоагулянтної терапії при проведенні кардіоверсії
|
Рекомендації
|
Класa
|
Рівеньb
|
|
Для пацієнтів з ФП, епізод якої триває протягом 48 год або довше, або якщо
тривалість епізоду ФП невідома, рекомендована терапія ПАК (при застосуванні АВК
МНВ 2,0–3,0 або ривароксабану) протягом принаймні 3 тижнів перед кардіовер-
сією та 4 тижнів після неї, незалежно від методу кардіоверсії (електрична або
фармакологічна за допомогою пероральних / внутрішньовенних засобів)
|
I
|
В
|
|
Пацієнтам, яким планується проведення відстроченої кардіоверсії, рекомендується від-
давати перевагу ривароксабану перед АВК, зважаючи на скорочення строків підготовки
до кардіоверсії. І в пацієнтів з ФП, епізод якої триває протягом 48 год або довше, або
якщо тривалість епізоду ФП невідома, можливе використання НПАК (дабігатрану або
апіксабану), при дотриманні режиму прийому, протягом принаймні 3 тижнів перед
кардіоверсією та 4 тижнів після неї, незалежно від методу кардіоверсії (електрична або
фармакологічна за допомогою пероральних / внутрішньовенних засобів)
|
I
|
С
|
|
Після негайної / невідкладної кардіоверсії у пацієнтів з ФП, епізод якої триває протягом 48 год або довше, або якщо тривалість епізоду ФП невідома, рекомендована терапія ПАК протягом принаймні 4 тижнів, як і у пацієнтів, яким кардіоверсія проводиться у плановому порядку.
|
I
|
В
|
|
Для пацієнтів з ФП, епізод якої триває <48 год, з високим ризиком інсульту, при проведенні кардіоверсії в перипроцедурному періоді рекомендоване застосування гепарину в/в або відкоригованої в залежності від маси тіла пацієнта терапевтичної дози НМГ, після чого призначається тривала терапія ПАК або НПАК.
|
I
|
В
|
|
Якщо епізод ФП триває ≥48 год, після негайної / невідкладної кардіоверсії рекомендована терапія ПАК протягом принаймні 4 тижнів, як і у пацієнтів, яким кардіоверсія проводиться у плановому порядку.
|
I
|
В
|
|
У пацієнтів з високим ризиком інсульту рекомендовано продовжувати тривалу терапію ПАК.
|
I
|
В
|
|
У якості альтернативи кардіоверсії з попередньою антикоагулянтною терапією рекомендована кардіоверсія під контролем ТЕ-ЕхоКГ, яка дозволить виключити наявність тромбу у лівому передсерді або вушку лівого передсердя.
|
I
|
В
|
|
У пацієнтів, яким проводиться кардіоверсія під контролем ТЕ-ЕхоКГ за умов відсутності ознак тромбу, виконання процедури кардіоверсії рекомендується негайно після антикоагуляції гепарином. Далі введення гепарину слід продовжувати до того часу, доки не буде досягнуто адекватної антикоагуляції ПАК, яка має призначатися протягом принаймні 4 тижнів після кардіоверсії.
|
I
|
В
|
|
У пацієнтів, у яких в ході контролю ТЕ-ЕхоКГ було виявлено тромб, рекомендоване застосуванні АВК (МНВ 2,0-3,0) або НПАК протягом принаймні 3 тижнів, після чого проводиться повторна ТЕ-ЕхоКГ для того, щоб впевнитися у зникненні тромбу.
|
I
|
С
|
|
У пацієнтів, у яких в ході контролю ТЕ-ЕхоКГ було виявлено феномен спонтанного контрастування 3+-4+, рекомендоване застосуванні АВК (МНВ 2,0-3,0) або НПАК протягом принаймні 3 тижнів.
|
I
|
C
|
|
У пацієнтів з тріпотінням передсердь, яким проводиться кардіоверсія, антикоагулянтна терапія проводиться за тими ж принципами, що і у пацієнтів з ФП.
|
I
|
С
|
|
У пацієнтів з факторами ризику інсульту або рецидиву ФП терапія ПАК має проводитися пожиттєво, незважаючи на явне підтримання синусового ритму після кардіоверсії.
|
IIa
|
В
|
|
Якщо при повторній ТЕ-ЕхоКГ отримане підтвердження зникнення тромбу, слід виконати кардіоверсію, після чого необхідно зважити доцільність терапії ПАК протягом 4 тижнів або пожиттєво (якщо є фактори ризику).
|
IIa
|
C
|
|
Якщо при повторній ТЕ-ЕхоКГ виявлено, що тромб не зник, може бути зважена доцільність застосування альтернативної стратегії ведення пацієнта (наприклад, контролю частоти серцевих скорочень).
|
IIb
|
C
|
|
Для пацієнтів, у яких епізод ФП триває явно <48 год та які не мають факторів ризику тромбоемболічних ускладнень, при проведенні кардіоверсії в перипроцедурному періоді може бути зважена доцільність в/в введення гепарину або відкоригованої в залежності від маси тіла пацієнта терапевтичної дози НМГ без необхідності застосування ПАК після кардіоверсії.
|
IIb
|
C
|
aКлас рекомендації.
bРівень доказовості.
Лікування геморрагічних ускладнень НПАК
Наразі специфічні антидоти для різник НПАК відсутні, а методи пригнічення антикоагулянтних ефектів мають деякі обмеження. Пригнічення ефекту антагоністів вітаміну К шляхом застосування вітаміну К відбувається дуже повільно (щонайменше 24 години), проте введення свіжезамороженої плазми або факторів коагуляції швидше відновлює процеси згортання крові. При застосуванні НПАК, високі концентрації препарату в плазмі крові також можуть блокувати нещодавно введені фактори коагуляції крові. З іншого боку, відновлення процесу коагуляції крові не обов'язково гарантує гарні клінічні результати. Дослідження вказують на меншу тяжкість кровотеч, особливо внутрішньочерепних та інших небезпечних для життя кровотеч, при застосуванні НПАК ніж при застосуванні варфарину. Незважаючи на це, із збільшенням кількості пацієнтів, що прийматимуть один з НПАК, кількість кровотеч ймовірно чисельно збільшиться.
Лікування кровотеч, що не є небезпечними для життя
Окрім виконання стандартних заходів (таких як механічна компресія, оперативний гемостаз, відновлення об'єму плазми та інші заходи щодо підтримки гемодинаміки), з огляду на відносно короткий період напіввиведення, найважливішим антидотом НПАК є час (див. Таблицю 6 та схему на[AR1] малюнку 5 )
Після закінчення лікування, відновлення гемостазу слід очікувати протягом 12 – 24 годин після останнього прийому препарату, зважаючи на те, що період напіввиведення більшості НПАК з плазми крові становить близько 12 годин. У зв'язку з цим недооцінюється важливість інформації щодо режиму дозування, точного часу прийому препаратів, факторів, які впливають на концентрацію у плазмі крові (Р-глікопротеїн, хронічна хвороба нирок та ін.), та інших факторів, які впливають на систему гемостазу (супутнє застосування протитромботичних засобів).
Період виведення препарату з організму значною мірою залежить від стану нирок у пацієнтів, що отримують лікування дабігатраном (див. також Таблиці 4). У разі виникнення кровотечі у пацієнтів, що приймають дабігатран, слід підтримувати адекватний діурез. Незважаючи на те, що дабігатран може виводитись шляхом діалізу, слід взяти до уваги, що існує лише обмежений досвід застосування діалізу у такому випадку. Крім того, слід зважити ризик виникнення кровотечі у місці проколу для діалізу та ризик від очікування. У відкритому дослідженні, в якому дабігатран у дозі 50 мг вводився шести пацієнтам з термінальною стадією хвороби нирок, яким роблять гемодіаліз, середня доля препарату, виведеного шляхом діалізу склала 62% протягом 2 годин та 68% протягом 4 годин. Можливість посиленого виведення дабігатрану з плазми крові за допомогою гемоперфузії через вугільний фільтр наразі вивчається. На цей час останні не можна рекомендувати пацієнтам.
На противагу дабігатрану, діаліз не рекомендується пацієнтам, що отримують лікування будь-якими інгібіторами фактору Ха, оскільки у зв'язку із здатністю більшості інгібіторів фактору Ха значною мірою зв'язуватись з білками плазми крові, не спостерігається значного їх виведення шляхом діалізу.
Лікування небезпечних кровотеч
На основі обмежених експериментальних даних та беручи до уваги те, що ефективність факторів згортання крові у пацієнтів з активними кровотечами не була чітко визначена (тобто не визначена їх здатність зменшувати втрату крові та поліпшувати результат), можливе застосування КПК (концентрат факторів протромбінового комплексу, КПК; такі бренди як Cofact, Confidex, Octaplex та Beriplex) або аКПК (aКПК, тобто подібні до КПК, проте з активованим фактором VIIa; зареєстрована назва Feiba) у пацієнтів з небезпечними кровотечами у разі необхідності термінової підтримки системи гемостазу. До отримання більшої кількості даних щодо клінічної ефективності цих методик, їх вибір може залежати від їх наявності та досвіду лікувально-дослідного центру. На основі досліджень з використанням КПК у клінічних зразках та у здорових добровольців, введення можна розпочинати у дозі 25 одиниць/кг та повторювати за наявності клінічних показань. Подальші дослідження можуть дати більше інформації щодо дозування та необхідності у пристосуванні дози до НПАК, що приймаються.
Можливе застосування активованих концентратів протромбінового комплексу (Feiba, 50 МО/кг, з максимум 200 МО/кг/день), за наявності їх у лікарні.
Роль активованого рекомбінантного фактору VIIa (NovoSevenw, 90 мг/кг) потребує подальшого дослідження.
Можливе застосування інших прокоагулянтів, таких як антифібринолітики (транексамової кислоти або амінокапронової кислоти) або десмопресин (особливо у випадках коагулопатії або тромбопатії), хоча клінічні дані стосовно їх ефективності при кровотечах, спричинених НПАК майже відсутні. Крім того застосування інших прокоагулянтів не відміняє заходи, зазначені вище. Свіжозаморожена плазма не інгібує процес антикоагуляції, проте може призначатись для наповнення об'єму плазми крові у пацієнтів, які потребують значного переливання крові. За відсутності дефіциту вітаміну К або лікування антагоністами вітаміну К, застосування вітаміну К* не впливає на лікування кровотечі, що виникла внаслідок прийому НПАК. Подібним чином, протамін інгібує антикоагулянтний ефект гепарину, проте не відіграє жодної ролі у кровотечі, спричиненої застосуванням НПАК. Рекомендується проконсультуватись у кардіологів, спеціалістів з порушення гемостазу та лікарів невідкладної допомоги для визначення методики лікування кровотечі.
*МНН вітаміну К – менадіон.
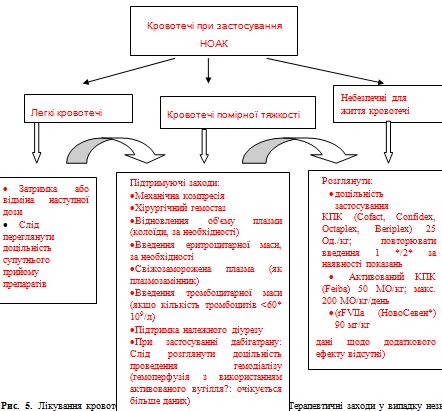
Рис. 5. Лікування кровотечі у пацієнтів, які приймають НПАК. Терапевтичні заходи у випадку незначних або тяжких кровотеч у пацієнтів, що отримують терапію НПАК.
* НовоСевен – торгова назва, МНН – Ептаког альфа (активований).
Пацієнти, що потребують запланованого хірургічного втручання
або лікування шляхом абляції
Коли слід припинити прийом нових пероральних антикоагулянтів?
При хірургічних втручаннях або інвазивних процедурах, пов'язаних з ризиком виникнення кровотеч, прийом НПАК слід тимчасово припинити. За результатами досліджень, одна чверть пацієнтів, які потребують антикоагулянтної терапії, мають тимчасово припинити застосування препарату протягом 2 років. Необхідно взяти до уваги характеристики пацієнтів (функція нирок, вік, геморагічні ускладнення в анамнезі, супутня терапія) та хірургічні фактори ризику з метою прийняття рішення про те, коли слід припинити та відновити прийом препарату, згідно з Таблицею 7.
«Бриджинг-терапія» є доцільною у пацієнтів з фібриляцією передсердь, які мали високий ризик розвитку тромбоемболічних ускладнень та отримують лікування антагоністами вітаміну К, проте у такому шунтуванні може не бути особливої необхідності у пацієнтів, які отримують терапію НПАК, оскільки застережні заходи, пов'язані з антикоагуляційним ефектом препаратів, вимагають лише короткочасного припинення та подальшого відновлення терапії НПАК перед та після операції[AR2] .
У випадку, коли хірургічне втручання не передбачає клінічно значущого ризику кровотечі і/або за можливості досягнення місцевого гемостазу, як при деяких стоматологічних процедурах або операції з видалення катаракти або глаукоми, його можна провести з використанням мінімальної концентрації НПАК (тобто через 12 або 24 години після останнього прийому залежно від дозування – один або два рази на добу), проте не при пікових концентраціях в плазмі крові.
Таким чином, більш практичним було б запланувати хірургічні процедури через 18 24 години після останнього прийому, а потім відновити терапію через 6 годин (тобто після досягнення гемостазу). В будь-якому випадку пацієнт може залишити клініку лише після повної впевненості у відсутності кровотечі. Крім того його слід повідомити про післяопераційний курс лікування та заходи у випадку виникнення кровотечі, а саме повідомити лікаря або стоматолога, якщо кровотеча не зупиняється сама по собі. У такому випадку лікар або дантист (або інший медичний персонал, що володіє ситуацією) мають бути на зв'язку з пацієнтом. При проведенні стоматологічних процедур, пацієнти можуть обережно прополоскати ротову порожнину 10 мл 5% транексамової кислоти чотири рази на день протягом 5 днів.
При проведенні операцій у пацієнтів з нормальною функцією нирок з мінімальним ризиком кровотеч (деякі з яких було перелічено у Таблиці 7) прийом НПАК рекомендується припинити за 24 години до проведення планової операції (Таблиця 6). У випадку проведення процедур у пацієнтів з нормальною функцією нирок, що можуть викликати значні кровотечі, останню дозу НПАК рекомендується приймати за 48 годин до втручання.
У пацієнтів, що приймають ривароксабан як із помірним, так і з тяжким порушенням функції нирок (кліренс креатиніну >30 мл/хв.) рекомендується припинити прийом ривароксабану раніше ніж за 24 години при хірургічних втручаннях із низьким ризиком та за 48 годин при хірургічних втручаннях із високим ризиком кровотечі.
У пацієнтів, що приймають ривароксабан з кліренсом креатиніну 15 – 30 мл/хв рекомендується припинити прийом ривароксабану за ≥36 годин та ≥48 годин при хірургічних втручаннях із низьким ризиком та високим ризиком кровотечі відповідно.
При застосуванні дабігатрану рекомендується припинення прийому перед хірургічним втручанням з низьким та високим ризиком виникнення кровотечі та залежно від функції нирки, див. Таблицю 6.
Спінальна анестезія, епідуральна анестезія та люмбарна пункція можуть потребувати досягнення повного гемостазу та відносяться до категорії втручань «високого ризику кровотечі».
|
Таблиця 6. Останній прийом препарату перед хірургічним втручанням
|
|
|
Дабігатран
|
Апіксабан
|
Eдоксабан
|
Ривароксабан
|
|
|
Ризик кровотечі незначний і/або можлива підтримка місцевого гемостазу: при мінімальному рівні препарату в крові (>12 годин або 24 годин після останнього прийому)
|
|
|
низький ризик
|
високий ризик
|
низький ризик
|
високий ризик
|
низький ризик
|
високий ризик
|
низький ризик
|
високий ризик
|
|
CrCl> 80 мл/хв.
|
≥24 год.
|
≥48 год.
|
≥24 год.
|
≥48 год.
|
дані відсутні
|
дані відсутні
|
≥24 год.
|
≥48 год.
|
|
CrCl 50-80 мл/хв.
|
24-48год
|
48-72год.
|
≥24 год.
|
≥48 год
|
дані відсутні
|
дані відсутні
|
≥24 год.
|
≥48 год.
|
|
CrCl30-50 мл/хв.b
|
≥48 год.
|
≥96 год.
|
≥24 год.
|
≥48 год
|
дані відсутні
|
дані відсутні
|
≥24 год.
|
≥48 год.
|
|
CrCl 15-30 мл/хв.
|
Показань немає
|
Показань немає
|
≥36 год.
|
≥48 год
|
дані відсутні
|
дані відсутні
|
≥36 год.
|
≥48 год.
|
|
|
|
CrCl
<15 мл/хв.
|
Немає офіційних показань до застосування
|
|
Показники, виділені жирним шрифтом, відхиляються від загального правила зупинки дослідження при низькому ризику >24 год., високому ризику >48 год.
bБагато з цих пацієнтів можуть отримувати лікування дабігатраном у низьких дозах (110 мг 2 рази/добу) або апіксабаном (25 мг 2 рази/добу), або низькими дозами ривароксабану (15 мг 1 раз/добу). Низький ризик = операція з низьким ризиком виникнення кровотечі: високий ризик = операція з високим ризиком виникнення кровотечі. див. також Таблицю 10.
CrCl кліренс креатині ну
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Не рекомендується застосування НПАК при нейроаксіальній анестезії. Хоча АЧТЧ та ПТЧ можуть забезпечити напівкількісну оцінку ефективності дабігатрану та інгібіторів фактору Ха, відповідно, методика, що включає нормалізацію АЧТЧ та ПТЧ до планових/невідкладних операцій не була валідована.
Коли слід відновлювати курс лікування новими пероральними антикоагулянтами?
При досягненні повного гемостазу, прийом НПАК можна відновити через 6-8 годин після процедури. Те ж саме стосується застосування після атравматичної спінальної/епідуральної анестезії або люмбарної пункції (без домішок крові).
Однак, відновлення прийому антикоагулянтів у повній дозі протягом 48-72 годин після анестезії або пункції під час хірургічних втручань може сприяти ризику виникнення кровотеч, що може переважати над ризиком розвитку кардіоемболії. Слід взяти до уваги відсутність специфічного антидоту у випадку виникнення кровотечі і/або необхідності у хірургічному втручанні. Для процедур, пов'язаних з іммобілізацією, вважається доцільним розпочати профілактику венозного тромбозу або введення проміжної дози НМГ через 6-8 годин після операції у разі досягнення гемостазу, при цьому слід зважити доцільність затриманого відновлення прийому НПАК на 48-72 години після інвазивного втручання. Максимальний антикоагуляційний ефект НПАК досягається через 2 години після прийому таблетки.
Відсутні дані щодо безпеки та ефективності післяопераційного застосування зменшеної дози НПАК (таких які, застосовуються для попередження ВТЕ (венозної тромбоемболії) після протезування стегнового/колінного суглоба) у пацієнтів з фібриляцією передсердь, які потребують хірургічного втручання.
Таблиця 7. Класифікація планових хірургічних втручань за ризиком виникнення кровотечі
|
Хірургічні втручання, що не потребують обов'язкової відміни антикоагулянтів
Стоматологічні операції
Видалення 1 – 3 зубів
Пародонтальна хірургія
Розріз абсцесу
Установка імпланту
Офтальмологія
Операції з видалення катаракти або глаукоми
Ендоскопія без хірургічного втручання
Хірургія поверхневих тканин (розріз абсцесу, незначні дерматологічні видалення ...)
|
|
Хірургічні втручання з низьким ризиком виникнення кровотечі
Ендоскопія з біопсією
Біопсія простати або сечового міхура
Електрофізілолгічне дослідження або радіочастотна катетерна абляція надшлуночкової тахікардії (включаючи лівосторонню абляцію методом взяття транссептальної пункції)
Ангіографія
Імплантація електрокардіостимулятора або кардіовертердефібрилятора (окрім випадків анатомічних ускладнень, таких як вроджена вада серця)
|
|
Хірургічні втручання з високим ризиком виникнення кровотечі
Складна лівостороння абляція (ізоляція легеневих вен, абляція вогнища шлуночкової тахікардії)
Спінальна або епідуральна анестезія, діагностика за допомогою люмбарної пункції
Хірургія органів грудної клітини
Хірургія органів черевної порожнини
Ортопедична хірургія
Біопсія печінки
Трансуретральна резекція простати
Біопсія нирки
|
|
Окремі фактори, які можуть впливати на виникнення кровотечі та розвиток тромбоемболічних явищ, слід взяти до уваги та обговорити з хірургом
|
4.1.8 Нефармакологічні методи профілактики інсульту
Тромбоутворення в передсердях найчастіше відбувається у вушку лівого передсердя. Оклюзія його отвору може перешкоджати утворенню тромбу і розвитку інсульту у хворих з ФП. Слід зазначити, що частота неповної оклюзії може досягати 40%. Неповну оклюзію вважають фактором ризику розвитку інсульту. Кандидатами на оклюзію вушка лівого передсердя можуть бути пацієнти, у яких є протипоказання до хронічної антикоагуляції. У дослідженні PROTECT AF (WATCHMAN Left Atrial Appendage System for Embolic PROTECTion in Patients with Atrial Fibrillation) [62] були рандомізовані 707 пацієнтів, яким проводили черезшкірне закриття вушка лівого передсердя (за допомогою пристрою WATCHMAN) з подальшою відміною варфарину (основна група; n = 463) або терапію антагоністом вітаміну К (МНВ 2-3; контрольна група; n = 244). За ефективністю у профілактиці інсульту, серцево-судинної смерті і системних емболій втручання не поступалося антикоагулянтній терапії (відносний ризик 0.62; 95% ДІ 0.35-1.25). Частота небажаних явищ (в основному ускладнень втручання) була вищою в основній групі.
4.2 Контроль частоти серцевих скорочень і ритму
4.2.1 Контроль частоти серцевих скорочень і ритму під час гострої фази
Цілями лікування хворих з ФП під час гострої фази є профілактика тромбоемболій та покращення функції серця. Рішення щодо невідкладного відновлення синусового ритму (у пацієнтів з вираженими порушеннями гемодинаміки) або зниженні частоти шлуночкового ритму (у більшості інших пацієнтів) залежить від вираженості симптомів ФП.
4.2.1.1 Контроль частоти шлуночкового ритму
Висока частота і нерегулярність шлуночкового ритму можуть бути причиною симптомів і важких порушень гемодинаміки у пацієнтів з ФП. У пацієнтів з тахісистолією зазвичай необхідно швидко знизити частоту серцевих скорочень. Якщо стан пацієнта стабільний, можливо пероральне застосування бета-блокаторів або недигідропіридинових антагоністів кальцію. У пацієнтів з тяжким порушенням гемодинаміки внутрішньовенне введення верапамілу або метопрололу дозволяє швидко сповільнити проведення через атріовентрикулярний вузол. У гострій ситуації цільова частота шлуночкового ритму зазвичай становить 80-100 за хвилину. У частині випадків може застосовуватися аміодарон, особливо за наявності значно зниженою функції ЛШ. Пацієнти з брадисистолічною формою ФП можуть відповісти на внутрішньовенне введення атропіну (0,5-2 мг), однак за наявності симптомів у багатьох випадках потрібні невідкладне відновлення ритму або тимчасова електрокардіостимуляція (електрод вводять в правий шлуночок). Після швидкого зниження частоти шлуночкового ритму зазвичай проводять тривалу терапію, спрямовану на контроль частоти серцевих скорочень; інформація щодо препаратів та їх доз міститься в розділі 4.3.2.
4.2.1.2 Медикаментозна кардіоверсія
У багатьох випадках синусовий ритм відновлюється спонтанно протягом перших декількох годин або днів. За наявності тяжких порушень гемодинаміки, збереженні симптомів, незважаючи на адекватний контроль частоти серцевих скорочень, а також у тих випадках, коли планується антиаритмічна терапія, може бути проведена медикаментозна кардіоверсія шляхом введення антиаритмічних засобів у вигляді болюса.
Частота відновлення синусового ритму при застосуванні антиаритмічних препаратів нижче, ніж при дефібриляції, проте в першому випадку не потрібні седація або анестезія і полегшується вибір антиаритмічного препарату для тривалої профілактики рецидивів ФП. Більшість пацієнтів, яким проводиться медикаментозна кардіоверсія, повинні перебувати під наглядом (включаючи моніторування ЕКГ) під час і після введення препарату (зазвичай протягом половини періоду напіввиведення), щоб своєчасно виявити аритмогенну дію (наприклад шлуночкові аритмії), зупинку синусового вузла або атріовентрикулярну блокаду. Самостійна кардіоверсія за допомогою пероральних антиаритмічних засобів («таблетка в кишені») [67] можлива у частини амбулаторних пацієнтів, якщо безпека подібного втручання була встановлена раніше. Для медикаментозної кардіоверсії можуть бути використані різні препарати (табл. 12).
Таблиця 12. Препарати, призначені для медикаментозної кардіоверсії у хворих з нещодавно розвинутим нападом ФП, і їх дози
|
Препарат
|
Доза
|
Наступна доза
|
Ускладнення
|
|
Аміодарон
|
5 мг/кг в/в впродовж 1 год
|
50 мг/год
|
Флебіт, гіпотонія. Уповільнює шлуночковий ритм. Повільне відновлення синусового ритму
|
|
Флекаінід
|
2 мг/кг в/в впродовж 10 хв або 200-300 мг перорально
|
Не призначається
|
Не можна призначати пацієнтам з серйозним захворюванням серця. Викликає подовження QRS і, відповідно, інтервалу QT. Може викликати збільшення частоти шлуночкового ритму внаслідок трансформації в тріпотіння передсердь з проведенням 1: 1
|
|
Ібутілід
|
1 мг в/в впродовж 10 хв
|
1 мг в/в впродовж 10 хв через 10 хв
|
Може викликати подовження QT і розвиток шлуночкової тахікардії типу|”пірует”. Контролювати зубці Т-U або подовження QT. Уповільнює шлуночковий ритм
|
|
Пропафенон
|
2 мг/кг в/в впродовж 10 хв або 450-600 мг перорально
|
|
Не можна призначати пацієнтам з серйозним захворюванням серця. Може викликати подовження QRS. Дещо уповільнює частоту шлуночкового ритму, але може викликати її збільшення внаслідок трансформації в тріпотіння передсердь з проведенням 1: 1
|
|
Вернакалант
|
3 мг/кг в/в впродовж 10 хв
|
Вторая инфузия 2 мг/кг в/в впродовж 10 хв через 15 хв
|
Вивчався тільки в клінічних дослідженнях. Нещодавно дозволений до застосування.68-70 а
|
a Вернакалант недавно зареєстрований Європейським агентством з ліків для відновлення синусового ритму у дорослих пацієнтів з ФП, що нещодавно розвинулась (≤7 днів у нехірургічних пацієнтів; ≤3 днів у хірургічних пацієнтів) [68,69]. У прямому порівняльному дослідженні AVRO (проспективне, рандомізоване, подвійне сліпе дослідження вернакаланта і аміодарону у пацієнтів з нещодавно розвинутим нападом ФП) вернакалант по ефективності перевершував аміодарон (відновлення ритму у 51,7% і 5,7% пацієнтів, відповідно, протягом 90 хвилин після початку лікування; p <0,0001) [70]. Вернакалант вводять внутрішньовенно (3 мг / кг протягом 10 хвилин). За необхідності через 15 хвилин проводять другу інфузію (2 мг / кг протягом 10 хвилин). Протипоказання до призначення вернакаланта: систолічний АТ <100 мм рт. ст., тяжкий аортальний стеноз, серцева недостатність III-IV функціонального класу, ГКС протягом попередніх 30 днів або подовження інтервалу QT. Перед призначенням вернакаланта слід провести адекватну гідратацію. Необхідно контролювати ЕКГ і показники гемодинаміки. За необхідності після введення вернакаланта може бути виконана електрична кардіоверсія. Препарат не протипоказаний пацієнтам зі стабільною коронарною хворобою серця, гіпертонічним ураженням серця та легкою серцевою недостатністю. Роль препарату в клінічній практиці поки не встановлена, проте він швидше за все буде застосовуватися для швидкого відновлення ритму у пацієнтів з нападом ізольованої ФП, що нещодавно розвинувся або ФП, що асоціюється з артеріальною гіпертонією, коронарною хворобою серця або легкою чи помірною серцевою недостатністю (I-II функціонального класу по NYHA).
Внутрішньовенне введення флекаїніду характеризується доведеною ефективністю (67-92% через 6 год) у пацієнтів з нетривалим (особливо <24 год) епізодом ФП. Звичайна доза становить 2 мг / кг протягом 10 хвилин. У більшості пацієнтів синусовий ритм відновлюється протягом першої години після внутрішньовенного введення. Препарат мало ефективний у пацієнтів з тріпотінням передсердь і персистуючою ФП.
При недавно розвиненому епізоді ФП може бути ефективним пероральне застосування флекаїніду. Рекомендовані дози становлять 200-400 мг (див. Нижче). Флекаїнід не слід призначати пацієнтам із захворюванням серця, що супроводжується порушенням функції ЛШ та ішемією.
У декількох плацебо-контрольованих рандомізованих дослідженнях була встановлена здатність пропафенона відновлювати синусовий ритм у пацієнтів з епізодом ФП, що нещодавно розвинувся. Після внутрішньовенного введення препарату в дозі 2 мг / кг протягом 10-20 хвилин частота відновлення ритму становила від 41 до 91%, а у пацієнтів групи плацебо – 10-29%. Пропафенон характеризується обмеженою ефективністю у пацієнтів з персистуючою ФП і тріпотінням передсердь. Як і флекаїнід, пропафенон не слід призначати пацієнтам з порушеною функцією ЛШ та ішемією міокарда. Крім того, пропафенон має слабкі бета-блокуючі властивості, тому доцільно уникати його застосування у пацієнтів з тяжким обструктивним захворюванням легень. Ритм відновлюється протягом від 30 хвилин до 2 год. Пропафенон дає також ефект при прийомі перорально (відновлення ритму через 2-6 год).
Після введення аміодарону кардіоверсія відбувається на кілька годин пізніше, ніж після застосування флекаініду і пропафенону. Протягом 24 год частота кардіоверсії у групах плацебо становила приблизно 40-60%, а в групах аміодарону вона збільшувалася до 80-90%. Протягом короткого терміну після введення аміодарону ритм не відновлюється. Через 24 год аміодарон по ефективності перевершував контроль в деяких, але не у всіх рандомізованих дослідженнях.
У пацієнтів з епізодом ФП, що недавно розвинувся, одна або дві (з інтервалом 10 хвилин) інфузії ібутиліда в дозі 1 мг (протягом 10 хвилин) забезпечували відновлення синусового ритму протягом 90 хвилин приблизно у 50% пацієнтів у кількох адекватно спланованих рандомізованих дослідженнях. Частота кардіоверсії у групі плацебо або контрольній групі була низькою. Ритм відновлювався приблизно протягом 30 хвилин. Найбільш важливим побічним ефектом є поліморфна шлуночкова тахікардія. Вона часто нестійка, проте може знадобитися дефібриляція. Після введення ібутиліда інтервал QT зазвичай збільшується приблизно на 60 мс. У пацієнтів з тріпотінням передсердь ефективність ібутиліда вище, ніж при ФП.
Інші засоби (див. примітку а до табл. 12)
В одному дослідженні порівнювали ефективність плацебо і соталола в двох дозах. Частота відновлення ритму склала 14% (2/14), 11% (2/11) і 13% (2/16), відповідно (різниця не достовірна).
В одному неконтрольованому дослідженні синусовий ритм після внутрішньовенного введення бета-блокатора (метопрололу) відновився у 13% з 79 пацієнтів. Повідомлень про ефективність атенололу, карведілолу, бісопрололу, пропранололу, тимололу або есмололу не опубліковано.
Адекватні рандомізовані плацебо-контрольовані дослідження верапамілу не опубліковані. У порівняльних дослідженнях з флекаїнідом, есмололом або пропафеноном частота відновлення синусового ритму при введенні верапамілу склала 6%, 12% і 14% у 17, 24 і 29 пацієнтів, відповідно.
Дигоксин не ефективний при нападі ФП. В одному дослідженні у 239 пацієнтів з ФП тривалістю <7 днів частота відновлення ритму через 16 год склала 46% в групі плацебо і 51% в групі дигоксину. У двох інших дослідженнях у 40 і 82 пацієнтів частота відновлення синусового ритму (плацебо і дигоксин) склала 40% vs. 47% і 14% vs. 32%, відповідно.
Таким чином, результати досліджень підтвердили, що дигоксин не здатний відновити синусовий ритм. Наявні дані вказують також на неефективність верапамілу. В одному дослідженні соталол виявився неефективним, а результатів досліджень аймаліну немає. Одне дослідження не підтвердило ефективність метопрололу, в той час як інші бета-блокатори не вивчались.
Порівняльні дослідження
У кількох дослідженнях порівнювали флекаїнід і пропафенон, проте тільки в одному дослідженні була продемонстрована більш висока частота кардіоверсії після введення флекаїніду (90 і 64%, відповідно). Застосування ібутиліду і пропафенону призвело до відновлення ритму у 71% і 49% пацієнтів, відповідно, однак у 10% хворих групи ібутиліду розвинулася нестійка шлуночкова тахікардія. На підставі цих досліджень не можна зробити чіткі висновки з приводу можливої різниці частоти кардіоверсії при застосуванні цих препаратів. Відповідно, вибирати антиаритмічний препарат слід на підставі протипоказань, побічних ефектів та / або вартості.
Таким чином, у пацієнтів з ФП, що нещодавно розвинулась (зазвичай тривалістю <48 год) можлива медикаментозна кардіоверсія за допомогою внутрішньовенного введення флекаїніду і пропафенону (за відсутності серйозного органічного захворювання серця) або аміодарону (за наявності ураження серця) (рис. 6). Очікувана частота кардіоверсії становить ≥50% протягом 15-120 хвилин. Ібутилід також ефективний, проте необхідно враховувати ризик аритмогенної дії [2].
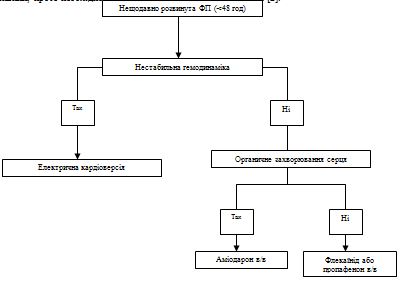
Рис. 6. Електрична і медикаментозна кардіоверсія у пацієнтів з ФП, що нещодавно розвинувся
Рекомендації щодо медикаментозної кардіоверсії
|
Рекомендації
|
Клас
|
Рівень
|
Джерело
|
|
Якщо планується медикаментозна кардіоверсія за відсутності серйозного захворювання серця у пацієнта з нападом ФП, що нещодавно розвинувся, переважно внутрішньовенне введення флекаїніду або пропафенону
|
I
|
А
|
71-73
|
|
Пацієнтам з нападом ФП, що нещодавно розвинувся і органічним захворюванням серця рекомендується внутрішньовенне введення аміодарону
|
I
|
A
|
74-76
|
|
У підібраних пацієнтів з епізодом ФП, що нещодавно розвинувся, які не страждають серйозним захворюванням серця, можливий прийом флекаїніду або пропафенону перорально у високій дозі («таблетка в кишені»), якщо безпека цього підходу була раніше підтверджена в стаціонарі
|
IIa
|
B
|
67
|
|
У пацієнтів з епізодом ФП, що нещодавно розвинувся і органічним захворюванням серця, але без гіпотонії або застійної серцевої недостатності можливе застосування ібутиліду. Сироваткові рівні електролітів і інтервал QT повинні бути в межах норми. Пацієнти повинні перебувати під постійним наглядом під час і протягом 4-х годин після інфузії, враховуючи ризик аритмогенної дії
|
IIb
|
A
|
71,77
|
|
Дигоксин (рівень доказів А), верапаміл, соталол, метопролол (рівень доказів В), інші бета-блокатори і аймалін (рівень доказів С) не ефективні, тому їх не рекомендується застосовувати для відновлення синусового ритму у пацієнтів з ФП, що нещодавно розвинулася
|
III
|
A B C
|
|
Коментар робочої групи:
Флекаінід (Флекаїнід), Ібутілід, Вернакалант та Аймалін в Україні станом на 01.10.2015р. не зареєстровані як лікарські засоби.
4.2.1.3 «Таблетка в кишені»
У стаціонарі після перорального прийому пропафенону ритм відновився у 55 (45%) з 119 пацієнтів протягом 3 год, а після прийому плацебо – у 22 (18%) з 121 пацієнта. У невеликих дослідженнях пропафенон і флекаїнід давали подібний ефект.
За даними одного дослідження, пероральне застосування пропафенону (450-600 мг) або флекаїніду (200-300 мг) було безпечним (в 1 з 569 випадків відзначено розвиток тріпотіння передсердь з швидким проведенням) і ефективним (94%; 534 з 569 епізодів) в амбулаторних умовах [67].
Цей підхід може бути корисним у підібраних пацієнтів з нечастими рецидивами (від 1 разу на місяць до 1 разу на рік) ФП, що супроводжуються вираженими симптомами. Перш ніж рекомендувати подібну тактику лікування, слід оцінити показання та протипоказання, а також ефективність і безпеку пероральної терапії в стаціонарі. Пацієнтам рекомендують приймати флекаїнід або пропафенон при появі симптомів ФП.
4.2.1.4 Кардіоверсія прямим електричним струмом
Дефібриляція – це ефективний метод відновлення ритму у пацієнтів з ФП.
Процедура
Якщо пацієнту не проводилася адекватна антикоагуляція протягом 3-х тижнів або тривалість ФП не перевищувала 48 год, то перед кардіоверсією слід провести черезстравохідну ехокардіографію для виключення тромбу в лівому передсерді (рис. 5). У випадку розвитку асистолії або брадикардії може знадобитися електрокардіостимуляція. Критерієм ефективності дефібриляції вважають припинення ФП, що підтверджується наявністю принаймні двох послідовних зубців Р. Двофазні зовнішні дефібрилятори характеризуються більш високою ефективністю в порівнянні з монофазним. Дослідження показали більш високу частоту відновлення синусового ритму при застосуванні двухфазного розряду.
В даний час існують два стандартних варіанти накладення електродів. У кількох дослідженнях було показано, що при передньо-задньому їх накладенні ефективність кардіоверсії вище, ніж при передньо-бічному [78]. Якщо дефібриляція виявляється неефективною, то слід змінити положення електродів і повторити дефібриляцію.
В амбулаторних умовах дефібриляція можлива за відсутності порушень гемодинаміки і важкого захворювання серця. Після дефібриляції необхідно протягом принаймні 3-х год проводити моніторування ЕКГ та показників гемодинаміки.
Внутрішня кардіоверсія можлива в особливих ситуаціях, наприклад, під час інвазивних втручань, коли для введення катетера для дефібриляції може використовуватися той же судинний доступ. Однак цей підхід практично не використовується (виключаючи наявність імплантованого дефібрилятора).
Ускладнення
Кардіоверсія може ускладнитися тромбоемболіями і аритміями; крім того, можуть спостерігатися ускладнення загальної анестезії. Частота тромбоемболій після дефібриляції становить 1-2%. Її можна знизити за допомогою адекватної антикоагуляції перед плановою кардіоверсією або шляхом виключення тромбозу лівого передсердя. Частим ускладненням є опіки шкіри. У пацієнтів з дисфункцією синусового вузла, особливо у літніх людей з органічним захворюванням серця, може розвинутися тривала зупинка синусового вузла. Небезпечні аритмії, такі як шлуночкова тахікардія і фібриляція шлуночків, можуть спостерігатися за наявності гіпокаліємії, інтоксикацій серцевими глікозидами або неадекватної синхронізації. Седація може супроводжуватися гіпоксією або гіповентиляцією, проте артеріальна гіпертонія і набряк легенів зустрічаються рідко.
Кардіоверсія у пацієнтів з імплантованими водіями ритму і дефібрилятором
Електрод повинен знаходитися на відстані принаймні 8 см від батарейки водія ритму. Рекомендується накладати електроди в передньо-бічному положенні. Переважно використання двофазного дефібрилятора, так як в цьому випадку для купіювання ФП потрібнен розряд меншою енергії. У пацієнтів з водієм ритму можна очікувати збільшення порогу стимуляції. Такі пацієнти повинні перебувати під ретельним наглядом. Після кардіоверсії слід перевірити прилад, щоб забезпечити його нормальну функцію.
Рецидив після кардіоверсії
Рецидиви після електричної кардіоверсії виникають в 3 фази:
(1) Негайний рецидив, що розвивається протягом перших кількох хвилин після дефібриляції.
(2) Ранній рецидив, що виникає в перші 5 днів після кардіоверсії.
(3) Пізній рецидив, що розвивається більш ніж через 5 днів.
Фактори, що призводять до рецидиву ФП, включають вік, тривалість ФП перед кардіоверсією, число попередніх рецидивів, збільшення розміру лівого передсердя або зниження його функції, наявність коронарної хвороби серця, захворювання легенів або мітрального пороку серця. Передсердні екстрасистоли, що виникають з різними інтервалами, більш висока частота серцевих скорочень і варіабельність проведення в передсердях також підвищують ризик рецидиву ФП.
Лікування антиаритмічними препаратами, такими як аміодарон, ібутилід, соталол, флекаїнід і пропафенон, перед кардіоверсією збільшує ймовірність відновлення синусового ритму [79-81]. Деякі пацієнти з нечастими нападами ФП (наприклад, один або два рази на рік), що супроводжуються вираженими симптомами, надають перевагу повторній кардіоверсії тривалої антиаритмічної терапії та терапії, спрямованій на контроль частоти шлуночкового ритму.
Рекомендації щодо електричної кардіоверсії
|
Рекомендації
|
Клас
|
Рівень
|
Джерело
|
|
Невідкладна дефібриляція рекомендується, якщо медикаментозні засоби не ефективні у пацієнта з тахісистолічною ФП і ішемією міокарда, що зберігається, артеріальною гіпотонією, стенокардією або серцевою недостатністю
|
I
|
С
|
|
|
Невідкладна дефібриляція рекомендується пацієнтам з ФП і синдромом передчасного збудження шлуночків за наявності вираженої тахікардії або нестабільної гемодинаміки
|
IIa
|
B
|
82
|
|
Планова дефібриляція може бути виконана перед тривалою антиаритмічною терапією у пацієнтів з ФП
|
IIa
|
B
|
46,78,83
|
|
Щоб підвищити ефективність електричної кардіоверсії і попередити рецидиви ФП, перед втручанням можуть застосовуватися аміодарон, флекаїнід, пропафенон, ібутилід або соталол
|
IIa
|
B
|
79-81
|
|
За наявності виражених симптомів, які зберігаються незважаючи на лікування, може проводитися повторна дефібриляція
|
IIb
|
C
|
|
|
Для контролю частоти серцевих скорочень перед дефібриляцією можуть застосовуватися бета-блокатори, дилтіазем або верапаміл, хоча їх здатність покращувати результати кардіоверсії або ефективність у профілактиці ранніх рецидивів ФП не встановлені
|
IIb
|
C
|
|
|
Дефібриляція протипоказана пацієнтам з інтоксикацією серцевими глікозидами
|
III
|
C
|
|
4.3 Довготривала терапія
Загальні підходи
Виділяють 5 основних цілей лікування хворих з ФП:
(1) Профілактика тромбоемболій.
(2) Купіювання симптомів.
(3) Оптимальне лікування супутніх серцево-судинних захворювань.
(4) Контроль частоти серцевих скорочень.
(5) Корекція порушення ритму.
Ці цілі не є взаємовиключними. Початкова стратегія лікування може відрізнятися від віддаленої мети ведення пацієнта. У пацієнтів з ФП, що супроводжується клінічними симптомами і зберігається протягом декількох тижнів, на першому етапі можуть бути використані антикоагулянти і засоби, що уповільнюють ритм, в той час як в більш пізні терміни метою буде відновлення синусового ритму. Якщо контроль частоти серцевих скорочень не дозволяє домогтися адекватного симптоматичного ефекту, то очевидно, що метою лікування має відновлення синусового ритму. Швидка кардіоверсія обгрунтована, якщо ФП викликає артеріальну гіпотонію або наростання серцевої недостатності. Навпаки, зменшення симптомів на тлі контролю частоти шлуночкового ритму у літнього пацієнта може служити підставою для відмови від спроб відновлення синусового ритму.
4.3.1 Контроль ритму або частоти серцевих скорочень
На першому етапі пацієнтам з ФП слід завжди призначати антитромботичні препарати та засоби, що уповільнюють шлуночковий ритм. Якщо кінцевою метою лікування є відновлення та утримання синусового ритму, то доцільно продовжувати прийом засобів, що уповільнюють шлуночковий ритм, за винятком тих випадків, коли у пацієнтів постійно зберігається синусовий ритм. Ці засоби застосовують для того, щоб забезпечити адекватний контроль частоти шлуночків ритму при рецидиві ФП.
Залежно від перебігу захворювання спочатку обрана стратегія може виявитися недостатньою, тому вона може бути замінена антиаритміками або втручаннями. Якщо ФП зберігається протягом тривалого терміну, то стійке відновлення синусового ритму може виявитися скрутним [23,84-85], однак клінічні дані, що підтверджують користь раннього контролю ритму, відсутні. Проте, очевидно, що на ранньому етапі розвитку ФП існує «вікно можливості», коли можна добитися стійкого відновлення синусового ритму.
Клінічні дослідження, в яких порівнювали стратегії контролю ритму і частоти серцевих скорочень
Результати рандомізованих досліджень, в яких порівнювали результати стратегій контролю ритму і частоти серцевих скорочень у хворих з ФП наведено в табл. 13 і 14 [86-92]. У дослідженні AFFIRM не було виявлено достовірної різниці загальної смертності (первинна кінцева точка) або частоти інсульту між двома стратегіями [86]. У дослідженні RATE стратегія контролю частоти шлуночкового ритму не поступалася стратегії контролю ритму по ефективності в профілактиці серцево-судинної смертності та захворюваності (комбінована кінцева точка) [87]. У дослідженні AF-CHF серцево-судинна смертність (первинна кінцева точка) не відрізнялася у рандомізованих хворих з фракцією викиду ЛШ ≤35%, симптомами застійної серцевої недостатності та ФП в анамнезі, яким проводили контроль частоти шлуночкового ритму або контроль ритму. Частота вторинних результатів, включаючи смерть будь-якої природи або наростання серцевої недостатності, також була зіставною [90].
Таблиця 13. Дослідження, в яких вивчалися стратегії контролю ритму і частоти серцевих скорочень у хворих з ФП [86-92]
|
Дослідження
|
Джерело
|
Число пацієн-тів
|
Середній вік (років)
|
Середня трив. спостереження (років)
|
Критерії включення
|
Первинний критерій ефективності
|
Число пацієнтів, які досягли первинної кінцевої точки
|
|
Контроль ЧСС
|
Контроль ритма
|
P
|
|
PIAF (2000)
|
92
|
252
|
61,0
|
1,0
|
Персистуюча ФП (7-360 днів)
|
Симптоматический эффект
|
76/125 (60,8%)
|
70/127 (55,1%
|
0,32
|
|
AFFIRM (2002)
|
86
|
4060
|
69.7
|
3.5
|
Пароксизмальна або персистиуюча ФП, вік> 65 років або ризик інсульту або смерті
|
Загальна смертність
|
310/2027 (25.9%)
|
356/2033 (26.7%)
|
0.08
|
|
RACE (2002)
|
87
|
522
|
68.0
|
2.3
|
Персистуючі ФП або тріпотіння протягом <1 року і 1-2 кардіоверсії протягом 2 років + пероральна антикоагуляція
|
Комбінована кінцева точка: серцево-судинна смерть, серцева недостатність, тяжка кровотеча, імплантація водія ритму, тромбоемболічні ускладнення, тяжкі небажані ефекти антиаритмічних препаратів
|
44/256 (17.2%)
|
60/266 (22.6%)
|
0.11
|
|
STAF (2003)
|
88
|
200
|
66.0
|
1.6
|
Персистуюча ФП (> 4 тижнів і менше 2-х років), розмір лівого передсердя> 45 мм, серцева недостатність II-IV, фракція викиду <45%
|
Комбінована кінцева точка: загальна смертність, цереброваскулярні ускладнення, серцево-легенева реанімація, емболічні ускладнення
|
10/100 (10.0%)
|
9/100 (9.0%)
|
0.99
|
|
HOT CAFÉ (2004)
|
89
|
205
|
60.8
|
1.7
|
Вперше виявлена персистуюча ФП (≥7 днів і <2 років), вік 50-75 років
|
Комбінована кінцева точка: смерть, тромбоемболічні ускладнення, внутрішньочерепна / велика кровотеча
|
1/101 (1.0%)
|
4/104 (3.9%)
|
>0.71
|
|
AF-CHF (2008)
|
90
|
1376
|
66
|
3.1
|
Фракція викиду ≤35%, серцева недостатність, ФП (≥6 год і дефібриляція протягом попередніх 6 міс)
|
Серцево-судинна смертність
|
175/1376 (25%)
|
182/1376 (27%)
|
0.59
|
|
J-RHYTHM (2009)
|
91
|
823
|
64.7
|
1.6
|
Пароксизмальна ФП
|
Комбінована кінцева точка: загальна смертність, церебральний інфаркт, системні емболії, велика кровотеча, госпіталізація з приводу серцевої недостатності або інвалідизація (фізична чи психологічна)
|
89/405 (22.0%)
|
64/418 (15.3%)
|
0.012
|
AFFIRM – Atrial Fibrillation Follow-up Investigation of Rhythm Management; HOT CAFE´ – How to Treat Chronic Atrial Fibrillation; J-RHYTHM – Japanese Rhythm Management Trial for Atrial Fibrillation; PIAF – Pharmacological Intervention in Atrial Fibrillation; RACE – RAte Control versus Electrical cardioversion for persistent atrial fibrillation; STAF – Strategies of Treatment of Atrial Fibrillation.
Таблица 13. Порівняння небажаних результатів у клінічних дослідженнях, в яких порівнювали стратегії контролю ритму і частоти серцевих скорочень у пацієнтів з ФП
|
Дослідження
|
Джерело
|
Загальна
смертність (контроль ЧСС/ритму)
|
Серцево-судинна смертність
|
Смертність з інших причин
|
Інсульт
|
Тромбоемболійні ускладнення
|
Кровотечі
|
|
PIAF (2000)
|
92
|
4
|
1/1
|
1а
|
ND
|
ND
|
ND
|
|
AFFIRM (2002)
|
86
|
666 (310/356)
|
167/164
|
113/165
|
77/80
|
ND
|
107/96
|
|
RACE (2002)
|
87
|
36
|
18/18
|
ND
|
ND
|
14/21
|
12/9
|
|
STAF (2003)
|
88
|
12 (8/4)
|
8/3
|
0/1
|
1/5
|
ND
|
8/11
|
|
HOT CAFÉ (2004)
|
89
|
4 (1/3)
|
0/2
|
1/1
|
0/3
|
ND
|
5/8
|
|
AF-CHF (2008)
|
90
|
228/217
|
175/182
|
53/35
|
11/9
|
ND
|
ND
|
а Загальне число пацєнтів не вказано. ND – не визначали. AFFIRM – Atrial Fibrillation Follow-up Investigation of Rhythm Management; HOT CAFE´ – HOw to Treat Chronic Atrial Fibrillation; PIAF – Pharmacological Intervention in Atrial Fibrillation; RACE – RAte Control versus Electrical cardioversion for persistent atrial fibrillation; STAF – Strategies of Treatment of Atrial Fibrillation.
Індивідуалізована терапія
Можливість приєднання антиаритмічних препаратів необхідно оцінювати індивідуально і обговорювати з пацієнтом перед початком лікування ФП. Перш ніж вибрати контроль частоти серцевих скорочень як єдину стратегію ведення пацієнтів з ФП, лікар повинен визначити, який вплив постійна аритмія може здійснити на пацієнта в майбутньому і яка ймовірна ефективність стратегії контролю ритму (рис. 7). Симптоми ФП мають важливе значення для вибору стратегії ведення (їх можна оцінити за допомогою індексу EHRA; табл. 6); вони доповнюють фактори, що впливають на успіх антиаритмічної терапії. Останні включають тривалий анамнез ФП, похилий вік, більш тяжкі серцево-судинні захворювання, інші супутні захворювання і розмір лівого передсердя.
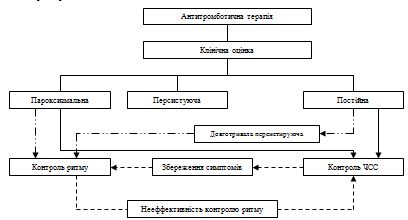
Рис. 7. Вибір стратегії контролю частоти серцевих скорочень або ритму. Контроль частоти шлуночкового ритму необхідний більшості пацієнтів з ФП за винятком тих випадків, коли вона низька. Антиаритмічні препарати можуть бути додані до засобів, що уповільнюють ритм, якщо симптоми зберігаються, незважаючи на адекватний контроль частоти серцевих скорочень, або обрана стратегія контролю ритму з урахуванням виражених симптомів, більш молодого віку або високої фізичної активності. При постійній ФП застосовують засоби, що уповільнюють ритм. Якщо прийнято рішення відновити синусовий ритм, то ФП називають тривалою персистуючою. При пароксизмальній ФП частіше вибирають стратегію контролю ритму, особливо якщо аритмія супроводжується вираженими симптомами і відсутнє серйозне захворювання серця. Суцільними лініями позначені методи першої лінії, суцільними лініями з точками – альтернативні методи. Пунктирні лінії – тактика лікування при неефективності обраного методу.
Ефекти на якість життя
У дослідженнях AFFIRM, RACE, PIAF і STAF не було виявлено різниці якості життя при порівнянні стратегій контролю ритму і частоти серцевих скорочень. Якість життя значно погіршується у пацієнтів з ФП у порівнянні зі здоровими людьми. Результати аналізу (ретроспективного) post hoc свідчать про те, що утримання синусового ритму може поліпшити якість життя і виживання пацієнтів.
Методи оцінки якості життя у хворих з ФП далекі від ідеалу. Найчастіше застосовують опитувальник SF-36, який дозволяє виміряти загальну якість життя, але не симптоми, пов'язані з ФП. Розроблені нові інструменти, більш специфічні для ФП (шкала тяжкості ФП Університету Торонто і шкала тяжкості ФП Канадського товариства серцево-судинних хвороб; остання дуже нагадує індекс EHRA [3,41]. У клінічних дослідженнях вивчаються і інші методи оцінки якості життя і симптомів ФП. Ці методи можуть виявитися більш інформативними, однак вони не використовувалися у великих дослідженнях.
Ефекти на серцеву недостатність і функцію лівого шлуночка
Частота розвитку серцевої недостатності не відрізнялася при виборі стратегій контролю частоти серцевих скорочень або ритму в дослідженнях AFFIRM, RACE або AF-CHF [86-87,90]. Результати субдосліджень, що проводилися в рамках дослідження RACE, і ехокардіографії у пацієнтів з серцевою недостатністю, яким проводилася катетерна абляція з приводу ФП, показали, що функція ЛШ погіршується в меншій мірі або навіть поліпшується на тлі стратегії контролю ритму [93,94], однак цей ефект не був підтверджений при ехокардіографії в дослідженні AFFIRM. Серцева недостатність може розвинутися або наростає на тлі будь-якої стратегії лікування ФП внаслідок прогресування основного захворювання серця, неадекватного контролю частоти шлуночкового ритму при рецидиві ФП або токсичності антиаритмічних препаратів. Відповідно, хоча у частини пацієнтів можливе поліпшення функції ЛШ при антиаритмічній терапії, вибирати стратегію контролю ритму слід індивідуально.
Ефекти на смертність і частоту госпіталізацій
Ні в одному порівняльному дослідженні не було підтверджено поліпшення смертності на тлі контролю ритму у хворих з ФП, хоча цей ефект очікувався перед початком досліджень [86-87,90]. При аналізі post-hoc дослідження AFFIRM було висловлено припущення, що несприятливі ефекти антиаритмічних препаратів (збільшення смертності на 49%) нівелюють користь відновлення синусового ритму (зниження смертності на 53%), в той час як аналіз бази даних RACE свідчить про те, що основне захворювання серця погіршує прогноз більшою мірою, ніж сама ФП.
Значення результатів порівняльних досліджень стратегій контролю ритму і частоти серцевих скорочень
Існує очевидна невідповідність між несприятливістю прогнозу у пацієнтів з ФП у порівнянні з таким у пацієнтів з синусовим ритмом і передбачуваною користю утримання синусового ритму, з одного боку (див. Розділ 2.1), і результатами фактично всіх порівняльних досліджень стратегій контролю частоти серцевих скорочень і ритму, з іншого боку [86,87,90].
Результати дослідження ATHENA (плацебо-контрольованого, подвійного сліпого дослідження в паралельних групах, в якому вивчалася ефективність дронедарона в дозі 400 мг двічі на день в профілактиці серцево-судинних госпіталізацій і смерті від будь-яких причин у пацієнтів з фібриляцією / тріпотінням передсердь; див. Розділ 4.3.5.1) вперше показали, що безпечне утримання синусового ритму дозволяє попередити несприятливі результати у хворих з ФП [95], проте результати цього дослідження самі по собі не дозволяють усунути існуюче протиріччя.
Можна зробити висновок, що контроль частоти шлуночкового ритму – це обгрунтована стратегія ведення літніх людей, у яких симптоми ФП представляються прийнятними (індекс EHRA = 1). Контроль ритму дозволяє купіювати симптоми, але не є підставою для припинення антитромботичної терапії, контролю частоти серцевих скорочень або лікування основного захворювання серця. Очевидна необхідність проведення контрольованих досліджень для порівняння ефективності катетерної абляції або нових безпечних антиаритмічних препаратів і стратегії контролю частоти шлуночкового ритму в профілактиці важких серцево-судинних результатів.
Рекомендації щодо контролю частоти серцевих скорочень і ритму у пацієнтів з ФП
|
Рекомендації
|
Клас
|
Рівень
|
Джерело
|
|
Лікування слід починати з контролю частоти серцевих скорочень у літніх пацієнтів з ФП і легко вираженими симптомами (індекс EHRA 1)
|
I
|
A
|
86-87,90
|
|
На тлі антиаритмічної терапії слід продовжувати прийом засобів, що уповільнюють частоту серцевих скорочень, щоб забезпечити адекватний контроль частоти шлуночкового ритму при рецидивах ФП
|
I
|
A
|
86
|
|
Контроль ритму рекомендується, якщо симптоми ФП (індекс EHRA≥2) зберігаються незважаючи на адекватний контроль частоти серцевих скорочень
|
I
|
B
|
3,46,93-94,96
|
|
Якщо ФП супроводжується серцевою недостатністю, обґрунтована стратегія контролю ритму для купіювання симптомів
|
IIa
|
B
|
93,94,97
|
|
Лікування слід починати з контролю ритму у молодих пацієнтів, у яких не виключається можливість катетерної абляції
|
IIa
|
C
|
|
|
Стратегія контролю ритму обгрунтована у пацієнтів із вторинною ФП, у яких вдалося усунути тригер або субстрат аритмії (наприклад, ішемія, гіпертиреоз)
|
IIa
|
C
|
|
Рекомендації щодо контролю частоти серцевих скорочень під час гострої фази
|
Рекомендації
|
Клас
|
Рівень
|
Джерело
|
|
У гострій ситуації за відсутності синдрому передчасного збудження для уповільнення шлуночкового ритму у пацієнтів з ФП рекомендується внутрішньовенне введення бета-блокаторів або недигідропіридинових антагоністів кальцію; необхідно дотримуватися обережності у пацієнтів з гіпотонією і серцевою недостатністю
|
I
|
А
|
100
|
|
Для контролю частоти серцевих скорочень в гострій ситуації у пацієнтів з ФП і серцевою недостатністю або артеріальною гіпотонією рекомендується внутрішньовенне введення серцевих глікозидів або аміодарону
|
I
|
B
|
101
|
|
У пацієнтів з синдромом передчасного збудження препаратами вибору є антиаритмічні препарати I класу або аміодарон
|
I
|
C
|
|
|
За наявності синдрому передчасного збудження і ФП бета-блокатори, недигідропіридинові антагоністи кальцію, дигоксин і аденозин протипоказані
|
III
|
C
|
|
Рекомендації щодо довготривалого контролю частоти серцевих скорочень
|
Рекомендації
|
Клас
|
Рівень
|
Джерело
|
|
Контроль частоти серцевих скорочень (бета-блокатори, недигідропіридинові антагоністи кальцію, серцеві глікозиди або їх комбінація) рекомендується пацієнтам з пароксизмальною, персистуючою або постійною ФП. Препарат вибирають індивідуально. Дозу слід підбирати, щоб уникнути брадикардії
|
I
|
В
|
100
|
|
Якщо симптоми ФП виникають при фізичному навантаженні, то необхідно оцінити адекватність контролю частоти серцевих скорочень за допомогою проби з фізичним навантаженням. Доцільно модифікувати терапію, щоб забезпечити фізіологічну хронотропну відповідь і уникнути брадикардії
|
I
|
C
|
|
|
У пацієнтів з ФП і синдромом передчасного збудження для контролю частоти серцевих скорочень переважно застосування пропафенону або аміодарону
|
I
|
C
|
|
|
На початковому етапі лікування слід домагатися менш жорсткого контролю частоти серцевих скорочень (<110 за хвилину)
|
IIa
|
B
|
98
|
|
Якщо симптоми зберігаються або розвивається тахікардіоміопатія, слід знижувати частоту серцевих скорочень до більш низьких значень (<80 за хвилину в спокої і <110 за хвилину при фізичному навантаженні). Коли буде досягнуто контролю частоти серцевих скорочень, слід провести добове моніторування ЕКГ
|
IIa
|
B
|
98
|
|
Для контролю частоти серцевих скорочень у пацієнтів з непостійною ФП можна застосовувати дронадерон (за винятком пацієнтів з серцевою недостатністю III-IV функціонального класу або нестабільною серцевою недостатністю)
|
IIa
|
B
|
95,99, 103
|
|
Дигоксин показаний пацієнтам із серцевою недостатністю і дисфункцією ЛШ, а також людям, які ведуть малорухливий спосіб життя
|
IIa
|
C
|
|
|
Якщо інші засоби неефективні або протипоказані, для контролю частоти серцевих скорочень можна застосовувати аміодарон перорально
|
IIb
|
C
|
|
|
Пацієнтам з пароксизмальною ФП не слід застосовувати одні серцеві глікозиди для контролю частоти серцевих скорочень
|
III
|
B
|
104
|
4.3.2 Довготривалий контроль частоти шлуночкового ритму
Нерегулярний ритм і висока частота серцевих скорочень у хворих з ФП можуть викликати серцебиття, задишку, стомлюваність і запаморочення. Адекватний контроль частоти шлуночкового ритму дозволяє зменшити симптоми і поліпшити гемодинаміку внаслідок збільшення часу наповнення шлуночкового і профілактики тахікардіоміопатіі.
Інтенсивність контролю частоти серцевих скорочень
Оптимальний рівень контролю частоти шлуночкового ритму з точки зору зменшення захворюваності, смертності, поліпшення якості життя і симптомів не встановлений. У попередніх рекомендаціях пропонувалося домагатися жорсткого контролю частоти шлуночкового ритму (частота серцевих скорочень 60-80 за хвилину в спокої і 90-115 за хвилину при помірному фізичному навантаженні) з урахуванням результатів дослідження AFFIRM [86]. У цьому дослідженні для жорсткого контролю частоти серцевих скорочень 147 (7,3%) пацієнтам довелося імплантувати водія ритму внаслідок брадикардії, в той час як більш висока частота серцевих скорочень у спокої не супроводжувалася погіршенням прогнозу. У нещодавно опублікованому дослідженні RACE II жорсткий контроль частоти шлуночкового ритму не мав переваг перед менш суворим контролем частоти серцевих скорочень у 614 рандомізованих пацієнтів [98]. Критерієм менш суворого контролю частоти шлуночкового ритму була частота серцевих скорочень у спокої <110 за хвилину, а більш жорсткого контролю – частота серцевих скорочень у спокої <80 за хвилину і адекватне її збільшення при помірному фізичному навантаженні [98]. Первинна кінцева точка була досягнута у 81 пацієнта (38 – менш суворий контроль частоти шлуночкового ритму та 43 – суворий контроль). Симптоми, небажані явища та якості життя були подібними у двох групах. На тлі менш суворого контролю частоти шлуночкового ритму було відзначено зниження частоти госпіталізацій. Дослідження показало, що менш суворий контроль частоти шлуночкового ритму обгрунтований у пацієнтів, яких включали у дослідження RACE II (пацієнти без виражених симптомів, пов'язаних з високою частотою серцевих скорочень).
4.3.3 Медикаментозний контроль частоти шлуночкового ритму
Препарати, що використовуються для контролю частоти шлуночкового ритму
Основними детермінантами частоти шлуночкового ритму під час нападу ФП є провідність і рефрактерність атріовентрикулярного вузла і тонус симпатичної і парасимпатичної системи. Для уповільнення шлуночкового ритму зазвичай застосовують бета-блокатори, недигідропіридинові антагоністи кальцію та серцеві глікозиди. Підходи до лікування під час гострої фази описані в розділі 4.2.1. Може виявитися необхідною комбінована терапія. Дронедарон також ефективно знижує частоту серцевих скорочень при рецидивах ФП. При неефективності інших засобів в деяких випадках можна застосовувати аміодарон. У пацієнтів з серцевою недостатністю обґрунтована терапія бета-блокатором і серцевим глікозидом.
Засоби для уповільнення шлуночкового ритму (табл. 15):
† Застосування бета-блокаторів найбільш виправдане за наявності підвищеного тонусу адренергічної системи та ішемії міокарда на тлі ФП. Ефективність та безпека тривалої терапії бета-блокаторами встановлені в декількох порівняльних дослідженнях з плацебо і дигоксином. У дослідженні AFFIRM бета-блокатори часто застосовували для жорсткого контролю частоти шлуночкового ритму. Дози бета-блокаторів вказані в табл. 15.
† Недигідропіридинові антагоністи кальцію (верапаміл і дилтіазем) можуть застосовуватися для контролю частоти шлуночкового ритму в гостру фазу і для тривалого лікування. Ці препарати роблять негативну інотропну дію, тому їх не слід призначати пацієнтам з систолічною серцевою недостатністю.
† Дигоксин і дигітоксин ефективно контролюють частоту шлуночкового ритму в спокої, але не під час фізичного навантаження. У комбінації з бета-блокатором вони можуть бути ефективними у пацієнтів, які страждають і не страждають серцевою недостатністю. Дигоксин може викликати (загрозу для життя) небажані ефекти, тому його слід застосовувати обережно. Можлива взаємодія з іншими препаратами.
† Тривала терапія дронедарона значно знижує частоту серцевих скорочень у спокої і при фізичному навантаженні. Дронедарон надає адитивної дії з іншими засобами, що уповільнюють серцевий ритм. Він ефективно знижує частоту серцевих скорочень при рецидивах ФП [99], але поки не зареєстрований для лікування постійної ФП.
Коментар робочої групи:
Дигітоксин в Україні станом на 01.10.2015р. не зареєстрований як лікарський засіб.
Дронедарон, згідно з рекомендаціями комітету із лікарських засобів для застосування у людини (СНМР) Європейського агентства лікарських засобів, в даний час не рекомендовано його застосування для контролю частоти серцевих скорочень у хворих із постійною формою ФП. Також дронедарон не показаний хворим з нестабільним гемодинамичним станом, серцевою недостатністю в анамнезі або на даний момент, чи систолічною дисфункцією ЛШ.
† Аміодарон – це ефективний препарат, що уповільнює серцевий ритм. Внутрішньовенне введення аміодарону було ефективним і добре переносилося у пацієнтів з порушенням гемодинаміки. Аміодарон можна застосовувати при неефективності інших засобів, проте він може викликати важкі екстракардіальні ефекти, включаючи дисфункцію щитовидної залози і брадикардію. Аміодарон, який спочатку використовували для контролю ритму, може застосовуватися для контролю частоти серцевих скорочень при трансформації ФП в постійну форму. Показанням до лікування аміодароном є неефективність інших більш безпечних препаратів.
Антиаритмічні препарати I класу не придатні для контролю частоти шлуночкового ритму. Соталол не слід застосовувати тільки для контролю частоти серцевих скорочень, однак його негативний хронотропний ефект може бути корисним при застосуванні препарату для контролю серцевого ритму.
Таблиця15. Засоби для контролю частоти серцевих скорочень
|
|
Внутрішньовенно
|
Підтримуюча пероральна доза
|
|
Бета-блокатори
|
|
|
|
Метопролол CR/XL
|
2,5-5 мг
|
100-200 мг один раз на день (ER)
|
|
Бісопролол
|
N/A
|
2,5-10 мг один раз на день
|
|
Атенолол
|
N/A
|
25-100 мг один раз на день
|
|
Есмолол
|
10 мг
|
N/A
|
|
Пропранолол
|
1 мг
|
10-40 мг тричі на день
|
|
Карведілол
|
N/A
|
3,125-25 мг двічі на день
|
|
Недигідропіридинові антагоністи кальцію
|
|
Верапаміл
|
5 мг
|
40 мг двічі на день – 360 мг один раз на день (ER)
|
|
Дилтіазем
|
N/A
|
60 мг тричі на день – 360 мг один раз на день (ER)
|
|
Серцеві глікозиди
|
|
|
|
Дигоксин
|
0.5–1 мг
|
0.125-0,5 мг один раз на день
|
|
Дигітоксин
|
0.4–0.6 мг
|
0.05-0,1 мг один раз на день
|
|
Інші
|
|
|
|
Аміодарон
|
5 мг/кг впродовж 1 год, підтримуюча доза 50 мг/год
|
100-200 мг один раз на день
|
|
Дронедаронa
|
N/A
|
400 мг двічі на день
|
аТільки у пацієнтів з непостійною формою ФП
Як домогтися контролю частоти шлуночкового ритму
Дослідження RACE II і попередні нерандомізовані дослідження свідчать про те, що на початковому етапі слід домагатися зниження частоти шлуночкового ритму в спокої менше 110 на хвилину. За необхідності, можна збільшити дози засобів, що уповільнюють ритм або призначити комбіновану терапію. При збереженні симптомів, особливо якщо вони пов'язані з високою частотою або нерегулярністю шлуночкового ритму, доцільно забезпечити більш жорсткий контроль частоти шлуночкового ритму. Її слід знижувати до тих пір, поки симптоми не зникнуть або суттєво не зменшаться, або з'ясується, що вони в основному пов'язані з основним захворюванням, а не порушенням ритму.
Якщо планується жорсткий контроль частоти шлуночкового ритму (частота серцевих скорочень <80 на хвилину в спокої і <110 на хвилину при помірному фізичному навантаженні), необхідно провести добове моніторування ЕКГ, щоб оцінити наявність пауз і брадикардії. Якщо симптоми пов'язані з фізичною активністю, може бути виконана проба з фізичним навантаженням (рис. 8). Вибір засобів, що уповільнюють ритм, залежить від віку, захворювання серця і цілі терапії (рис. 9). Якщо на тлі контролю частоти шлуночкового ритму зберігаються симптоми, може бути призначена антиаритмічна терапія.
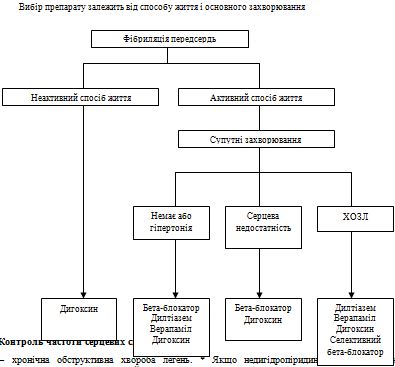
Рис. 9. Контроль частоти серцевих скорочень
ХОЗЛ – хронічна обструктивна хвороба легень. * Якщо недигідропіридинові антагоністи кальцію та дигоксин не забезпечують адекватний контроль частоти серцевих скорочень, можуть бути призначені селективні бета 1 адреноблокатори в невеликих дозах. У пацієнтів, які не відповіли на серцеві глікозиди, бета-блокатори або недигідропіридинові антагоністи кальцію, застосовують також аміодарон. Дронедарон може застосовуватися для контролю частоти серцевих скорочень у пацієнтів з рецидивуючими епізодами ФП
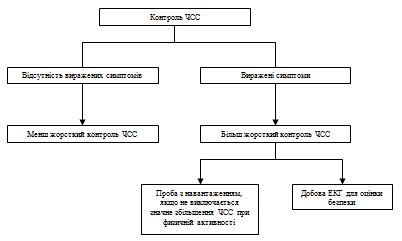
Рис. 8. Оптимальний контроль частоти серцевих скорочень
4.3.4 Абляція і модифікація атріовентрикулярного вузла
Абляція атріовентрикулярного вузла забезпечує високо ефективний контроль шлуночкового ритму у пацієнтів з ФП. Повну поперечну блокаду викликають шляхом катетерної деструкції атріовентрикулярного вузла або пучка Гіса за допомогою радіочастотного випромінювання. Абляція атріовентрикулярного вузла – це паліативне втручання, проте ефект його незворотний. Відповідно, втручання обгрунтовано в тих випадках, коли виявилися неефективними засоби, що уповільнюють ритм (у тому числі комбінована терапія), антиаритмічна терапія і / або абляція лівого передсердя. У таких хворих абляція атріовентрикулярного вузла поліпшує якість життя, в той час як смертність після втручання порівнянна з такою у загальній популяції.
Вибір пристроїв для імплантації (VVI, DDD, ресинхронізація; водій ритму або імплантований кардіовертер-дефібрилятор) залежить від типу ФП (пароксизмальна, персистуюча або постійна форми), наявності та тяжкості серцево-судинного захворювання, фракції викиду ЛШ та наявності та тяжкості серцевої недостатності. Можна припустити, що пацієнтам зі зниженою функцією ЛШ після абляції атріовентрикулярного вузла потрібна двокамерна кардіостимуляція, щоб попередити подальше погіршення функції цієї камери серця. У пацієнтів без дисфункції ЛШ доцільність двокамерної кардіостимуляції не встановлена. Результати деяких досліджень свідчать про сприятливий її ефект [105], однак інші дані вказують на порівнянну користь стимуляції правого шлуночка.
Рекомендації щодо абляції атріовентрикулярного вузла у пацієнтів з ФП
|
Рекомендації
|
Клас
|
Рівень
|
Джерело
|
|
Абляція атріовентрикулярного вузла для контролю частоти серцевих скорочень може бути виконана, якщо частота шлуночкового ритму контролюється медичними засобами і не вдається попередити рецидиви ФП за допомогою антиаритмічних препаратів або останні викликають серйозні побічні ефекти, а катетерна або хірургічна абляція ФП не показана або виявилася неефективною
|
IIa
|
В
|
106,107
|
|
Абляція атріовентрикулярного вузла можлива у пацієнтів з постійною ФП і показаннями до ресинхронізації серця (серцева недостатність III-IV функціонального класу незважаючи на оптимальну медикаментозну терапію, фракція викиду ≤35%, QRS ≥130 мс)
|
IIa
|
B
|
105,108-110
|
|
Абляція атріовентрикулярного вузла можлива у пацієнтів, які не відповіли на ресинхронізацію, у яких ФП не дозволяє проводити ефективну бівентрикулярну стимуляцію, а аміодарон не ефективний або протипоказаний
|
IIa
|
C
|
|
|
У пацієнтів з будь-якою формою ФП, різко зниженою функцією ЛШ (фракція викиду ≤35%) і тяжкою серцевою недостатністю (III-IV функціонального класу) після абляції атріовентрикулярного вузла показана бівентрикулярна стимуляція
|
IIa
|
C
|
|
|
Абляція атріовентрикулярного вузла для контролю частоти серцевих скорочень може бути проведена, якщо передбачається тахікардіоміопатія, частота шлуночкового ритму контролюється медичними засобами, а пряма абляція ФП не показана або виявилася неефективною
|
IIb
|
C
|
|
|
Абляція атріовентрикулярного вузла з подальшою ресинхронізацією обгрунтована у пацієнтів з постійною ФП, фракцією викиду ≤35% і серцевою недостатністю I-II функціонального класу на тлі оптимальної терапії, якщо медичні засоби, що уповільнюють ритм, недостатньо ефективні або викликають побічні реакції
|
IIb
|
C
|
|
|
Катетерну абляцію атріовентрикулярного вузла для контролю ФП та / або частоти серцевих скорочень у пацієнтів з ФП слід проводити тільки при неефективності медикаментозної терапії або неефективності чи неможливості катетерної абляції ФП
|
III
|
C
|
|
Рекомендації щодо імплантації водія ритму після абляції атріовентрикулярного вузла
|
Рекомендації
|
Клас
|
Рівень
|
Джерело
|
|
У пацієнтів з будь-яким типом ФП, помірно зниженою функцією ЛШ (фракція викиду ≤45%) і легкими симптомами серцевої недостатності (II функціональний клас) після абляції атріовентрикулярного вузла можлива імплантація ресинхронізуючого водія ритму
|
IIb
|
C
|
|
|
Пацієнтам з пароксизмальною ФП та нормальною функцією ЛШ після абляції атріовентрикулярного вузла може бути імплантований двокамерний водій ритму з функцією перемикання режиму (DDD)
|
IIb
|
C
|
|
|
Пацієнтам з персистуючою або постійною ФП та нормальною функцією ЛШ після абляції атріовентрикулярного вузла може бути імплантований однокамерний водій ритму (VVIR)
|
IIb
|
C
|
|
Модифікація атріовентрикулярного вузла
Невеликі попередні дослідження показали, що катетерна радіочастотна модифікація провідних властивостей атріовентрикулярного вузла викликає зменшення частоти шлуночкового ритму і симптомів ФП. Однак критерії успіху втручання не визначені, а абляція атріовентрикулярного вузла та імплантація водія ритму представляються більш ефективними методами лікування. У зв'язку з цим модифікація атріовентрикулярного вузла без імплантації постійного водія ритму проводиться рідко.
4.3.5 Довготривалий контроль ритму
4.3.5.1 Антиаритмічні засоби, що використовуються для стримування синусового ритму
Основним аргументом на користь стратегії контролю ритму є купіювання симптомів ФП. Навпаки, за відсутності симптомів (у тому числі на тлі адекватного контролю частоти серцевих скорочень) пацієнтам зазвичай не слід призначати антиаритмічні засоби. Нижче перераховані основні принципи антиаритмічної терапії у хворих з ФП:
(1) Підставою для антиаритмічної терапії є зменшення симптомів ФП.
(2) Ефективність антиаритмічних засобів, які використовують для контролю синусового ритму, скромна.
(3) Ефективна антиаритмічна терапія зазвичай призводить до зменшення, а не до повного припинення рецидивів ФП.
(4) Якщо антиаритмічний препарат виявляється неефективним, то пацієнт може відповісти на інший препарат.
(5) Часто відзначаються аритмогенні або екстракардіальні побічні ефекти.
(6) Вибір антиаритмічного препарату повинен в першу чергу визначатися безпекою, а не ефективністю.
Нижче обговорюються окремі антиаритмічні препарати, а їх основні недоліки перераховані в табл. 16.
Таблиця 16. Рекомендовані дози і основні недоліки антиаритмічних препаратів
|
Препарати
|
Доза
|
Основні протипоказання і запобіжні заходи
|
Зміни на ЕКГ, що є підставою для зниження дози або відміни
|
Уповільнення атріовентрикулярного проведення
|
|
Дизопірамід
|
100-250 мг тричі на день
|
Протипоказаний при систолічній серцевій недостатності. Застосовувати обережно у поєднанні із засобами, які подовжують QT
|
Інтервал QT >500 мс
|
Немає
|
|
Флекаїнід
Флекаїнід XL
|
100-200 мг двічі на день
200 мг 1 раз на день
|
Протипоказаний при кліренсі креатиніну <50 мл / хв, коронарній хворобі серця, зниженій фракції викиду ЛШ. Дотримуватися обережності при порушенні провідності
|
Збільшення тривалості QRS> 25% порівняно з вихідною
|
Немає
|
|
Пропафенон
Пропафенон SR
|
150-300 мг тричі на день
225-425 мг двічі на день
|
Протипоказаний при коронарній хворобі серця, зниженій фракції викиду ЛШ. Дотримуватися обережності при порушенні провідності і порушенні функції нирок
|
Збільшення тривалості QRS> 25% порівняно з вихідною
|
Незначне
|
|
d,l-Соталол
|
80-160 мг двічі на день
|
Протипоказаний при вираженій гіпертрофії ЛШ, систолічній серцевій недостатності, подовженні QT, гіпокаліємії, кліренсі креатиніну <50 мг / мл. При помірній дисфункції нирок слід ретельно підбирати дозу
|
Інтервал QT>500 мс
|
Подібний ефект з бета-блокаторами у великих дозах
|
|
Аміодарон
|
600 мг/добу 4 тижні, 400 мг/добу 4 тижні, потім 200 мг 1 раз на день
|
Застосовувати обережно у поєднанні із засобами, які подовжують QT, при серцевій недостатності. Слід знизити дози антагоністів вітаміну К і дигоксину / дигітоксину
|
Інтервал QR>500 мс
|
10-12 за хвилину у пацієнтів з ФП
|
|
Дронедарон
|
400 мг двічі на день
|
Протипоказаний при серцевій недостатності III-IV функціонального класу і нестабільній серцевій недостатності, терапії засобами, що подовжують QT, потужними інгібіторами CYP 3A4, при кліренсі креатиніну <30 мг / мл. Дозу дигітоксину / дигоксину слід знизити. Часто відзначається підвищення сироваткового креатиніну на 0,1-0,2 мг / дл, яке не вказує на зниження функції нирок
|
Інтервал QR>500 мс
|
10-12 за хвилину у пацієнтів з ФП
|
Рекомендації щодо вибору антиаритмічних препаратів для контролю ФП
|
Рекомендації
|
Клас
|
Рівень
|
Джерело
|
|
Наступні антиаритмічні препарати рекомендується застосовувати для контролю ритму у пацієнтів з ФП з урахуванням наявності захворювання серця:
|
|
|
|
|
· Аміодарон
· Дронедарон
· Флекаїнід
· Пропафенон
· d,l-соталол
|
I
I
I
I
I
|
A
A
A
A
A
|
46,111, 125
95,99
111,127
111,125
46,83, 111
|
|
Аміодарон більш ефективно утримує синусовий ритм, ніж соталол, пропафенон, флекаїнід (за аналогією) або дронедарон (рівень доказів А), однак через токсичність його слід застосовувати, якщо інші засоби виявилися неефективними або протипоказані (рівень доказів С)
|
I
|
A/C
|
46,111, 121, 125
|
|
У пацієнтів з тяжкою серцевою недостатністю (III-IV функціонального класу) або нестабільною серцевою недостатністю II функціонального класу (декомпенсація протягом попереднього місяця) аміодарон є препаратом вибору
|
I
|
B
|
126
|
|
У пацієнтів без серйозного органічного захворювання серця антиаритмічну терапію слід починати з дронедарону, флекаїніду, пропафенону і соталолу
|
I
|
A
|
95,99, 111, 125-127
|
|
Бета-блокатори рекомендується застосовувати для профілактики адренергічної ФП
|
I
|
C
|
|
|
Якщо один антиаритмічний препарат не знижує частоту рецидивів ФП до прийнятного рівня, то слід призначити інший антиаритмічний препарат
|
IIa
|
C
|
|
|
Дронедарон може застосовуватися для зниження частоти серцево-судинних госпіталізацій у пацієнтів з непостійною ФП і серцево-судинними факторами ризику
|
IIa
|
B
|
95,99
|
|
У пацієнтів з першим епізодом ФП для контролю ритму (і частоти серцевих скорочень) можна спробувати застосовувати бета-блокатори
|
IIa
|
C
|
|
|
Пацієнтам з ФП, обумовленої активністю блукаючого нерва, може бути призначений дизопірамід
|
IIb
|
B
|
111,118, 119
|
|
Дронедарон не рекомендується призначати пацієнтам із серцевою недостатністю III-IV функціонального класу або нестабільною серцевою недостатністю II функціонального класу (декомпенсація протягом попереднього місяця)
|
III
|
B
|
117,122
|
|
Антиаритмічні препарати не рекомендується застосовувати для утримання синусового ритму у пацієнтів з вираженою дисфункцією синусового або атріовентрикулярного вузла, якщо їм не імплантований водій ритму
|
III
|
C
|
|
Ефективність антиаритмічних препаратів в профілактиці рецидивів ФП
Бета-блокатори мають скромну ефективність в профілактиці рецидивів ФП (винятком є тиреотоксикоз і ФП, що виникає при фізичному навантаженні). У рандомізованому дослідженні у 394 пацієнтів частота рецидивів ФП при лікуванні метопрололом склала 47,7%, а в контрольній групі – 59,9% (P = 0.005). «Антиаритмічний ефект» може також пояснюватися поліпшенням контролю частоти серцевих скорочень, на тлі якого розвиваються приховані рецидиви ФП (див. Розділ 3.5).
За даними мета-аналізу 44-х рандомізованих контрольованих досліджень, в яких антиаритмічні препарати порівнювали з плацебо або відсутністю лікування [111], швидко (дизопірамід, хінідин) або повільно (флекаїнід, пропафенон) дисоціюють блокатори натрієвих каналів, «чисті» блокатори калієвих каналів (дофетилід), препарати, що блокують калієві канали і бета-адренорецептори (соталол), і блокатори різних іонних каналів, що мають антиадренергетичну активність (аміодарон), знижували частоту рецидивів ФП.
В цілому ймовірність утримання синусового ритму при застосуванні антиаритмічних засобів збільшується приблизно вдвічі [112]. Аміодарон за ефективністю перевершував препарати I класу і соталол. Число пацієнтів, яких необхідно пролікувати протягом 1 року (NNT), склало 2-9. Частота припинення лікування внаслідок небажаних ефектів була невисокою (1 з 9-27 пацієнтів). Всі препарати, за винятком аміодарону та пропафенону, надавали аритмогенну дію [111]. Число пацієнтів, яких необхідно пролікувати, щоб розвинувся несприятливий ефект (NNH), склало 17-119. У більшість досліджень включали пацієнтів без тяжких супутніх захворювань серця. Хоча смертність у всіх дослідженнях була низькою (0-4.4%), лікування швидко дисоціює блокаторами натрієвих каналів асоціювалося зі збільшенням смертності (відношення шансів 2.39; 95% ДІ 1.03-5.59; P = 0.04; NNH = 109].
Флекаїнід, пропафенон, соталол і аміодарон часто застосовують у більшості європейських країн. Частота застосування хінідину (першого зареєстрованого блокатора натрієвих каналів) в останні роки знизилася, оскільки він викликає подовження інтервалу QT і збільшує ризик розвитку поліморфної шлуночкової тахікардії типу пірует. Дизопірамід також призначають рідко (винятком є ФП, пов'язана зі збільшенням тонусу блукаючого нерва). Сібензолін і гідрохінідин дозволені до застосування тільки в декількох країнах Європи. Дронедарон – це новий антиаритмічний препарат, який спеціально розроблений для лікування ФП. Він зареєстрований у багатьох країнах Європи, Північної Америки та інших країнах.
Флекаїнід приблизно вдвічі збільшує ймовірність утримання синусового ритму. Його ефективність спочатку вивчали при пароксизмальній ФП, проте його також можна застосовувати для контролю синусового ритму після дефібриляції. Препарат безпечний у пацієнтів без серйозного органічного захворювання серця, проте його не слід призначати пацієнтам з коронарною хворобою серця або зі зниженою фракцією викиду ЛШ. Необхідно дотримуватися обережності при лікуванні флекаїнідом у хворих з порушенням внутрішньошлуночкової провідності, особливо з блокадою лівої ніжки пучка Гіса. Після початку лікування цим препаратом рекомендується моніторування ЕКГ. Збільшення тривалості інтервалу QRS принаймні на 25% у порівнянні з вихідним вказує на ризик аритмогенного дії; в таких випадках слід зменшити дозу або відмінити препарат. При збільшенні дози флекаїніду також необхідно моніторування тривалості інтервалу QRS. Рекомендується супутня блокада атріовентрикулярного вузла (див. Розділ 4.3.1), так як флекаїнід і пропафенон можуть викликати трансформацію ФП в тріпотіння передсердь з швидким проведенням збудження на шлуночки.
Пропафенон попереджає рецидиви ФП. Крім того, він володіє слабкими бета-блокуючими властивостями. Препарат безпечний у пацієнтів без серйозного органічного захворювання серця. За аналогією з флекаїнідом, його не слід призначати пацієнтам з коронарною хворобою серця або зниженою фракцією викиду ЛШ. При лікуванні пропафеноном доцільно дотримуватися тих же заходів безпеки, що і при застосуванні пропафенону.
Хінідин був одним з перших серцево-судинних препаратів, який вивчався в проспективних клінічних дослідженнях. У контрольованих дослідженнях він сприяв збереженню синусового ритму. Однак при мета-аналізі було показано, що хінідин збільшує смертність, ймовірно, за рахунок аритмогенної дії, пов'язаної з подовженням інтервалу QT (ризик розвитку поліморфної шлуночкової тахікардії типу пірует). В даний час застосовується рідко.
Аміодарон перевершує пропафенон і соталол по ефективності в профілактиці рецидивів ФП. NNT склало 3 при застосуванні аміодарону, 4 – флекаїніду, 5 – дофетиліду і пропафенону і 8 – соталола [111]. Аміодарон може бути з успіхом використаний у пацієнтів з частими рецидивами ФП, незважаючи на терапію іншими антиаритмічними препаратами. На відміну від більшості інших засобів, його можна призначати пацієнтам з органічним захворюванням серця, включаючи серцеву недостатність [113]. Ризик розвитку поліморфної шлуночкової тахікардії типу пірует при лікуванні аміодароном нижче, ніж при застосуванні «чистих» блокаторів калієвих каналів, що можливо пов'язано з блокадою різних іонних каналів. Однак при лікуванні аміодароном відзначали аритмогенний ефект [114], тому рекомендується контролювати інтервал QT.
Соталол за ефективністю в профілактиці рецидивів ФП виявився порівнянним з комбінацією хінідину та верапамілу у фіксованих дозах [83], але поступався аміодарону. У дослідженні SAFE-T ефективність соталолу і аміодарону в профілактиці нападів ФП була порівнянною у пацієнтів з ішемічною хворобою серця (р = 0.53) [46]. Аритмогенна дія соталола пов'язана з подовженням інтервалу QR [115] та / або брадикардією. Необхідне ретельне моніторування тривалості інтервалу QT [115] і патологічних зубців TU [114]. Якщо інтервал QT збільшується до понад 500 мс, слід скасувати соталол або знизити його дозу. Ризик аритмогенної дії підвищений у жінок, пацієнтів з вираженою гіпертрофією ЛШ, важкою брадикардією, шлуночковими аритміями, дисфункцією нирок або гіпокаліємією і гіпомагніємією [45].
Дронедарон – це блокатор натрієвих, калієвих і кальцієвих каналів, який володіє неконкурентною антиадренергічною активністю. Як і соталол, пропафенон і флекаїнід, за ефективністю в профілактиці рецидивів ФП він поступається аміодарону [116]. У дослідженні DIONYSOS (рандомізоване подвійне сліпе дослідження, в якому порівнювали ефективність і безпеку дронедарону в дозі 400 мг двічі на день і аміодарону в дозі 600 мг / добу протягом 28 днів, а потім 200 мг / добу протягом принаймні 6 міс ) у 504 пацієнтів з персистуючою ФП дронадерон був менш ефективний, ніж аміодарон, але рідше викликав небажані явища. Частота комбінованої первинної кінцевої точки (рецидив ФП і скасування досліджуваного препарату) склала 75% і 59% в групах дронедарону і аміодарону, відповідно (відношення шансів 1.59; 95% ДІ 1.28-1.98; P <0.0001]. Рецидиви ФП при лікуванні дронедароном розвивалися частіше, ніж при застосуванні аміодарону (36.5% vs. 24.3%). Однак частота дострокового припинення лікування була дещо нижчою у групі дронедарону (10.4% vs. 13.3%). Частота певних небажаних явищ, передбачених протоколом, склала 39,3% і 44,5% у групах дронедарону і аміодарону, відповідно (відношення шансів 0.80; 95% ДІ 0.60-1.07; P = 0.129). У групі дронедарону рідше зустрічалися небажані явища з боку щитовидної залози, нервової системи, шкіри та органу зору.
Безпека дронедарона має важливе значення для пацієнтів без органічного захворювання серця і хворих зі стабільним захворюванням серця. Дронедарон має слабку аритмогенну дію [95,99]. У двох великих дослідженнях дронадерон перевершував плацебо за ефективністю в профілактиці рецидивів ФП [99]. За даними мета-аналізу двох досліджень, медіана часу до першого епізоду ФП склала 53 дні у групі плацебо і 116 днів у групі дронедарону (відношення шансів 0.75; ДІ 0.65-0.87; P <0.0001). Дронедарон значно знижував частоту шлуночкового ритму при першому рецидиві ФП або тріпотіння передсердь.
Дослідження ANDROMEDA у хворих з синусовим ритмом і тяжкою серцевою недостатністю було припинено достроково внаслідок збільшення смертності в групі дронедарону [117]. У цьому дослідженні вивчали ефективність дронедарону у пацієнтів з серцевою недостатністю II-IV функціонального класу, у яких була тяжка дисфункція ЛШ і принаймні одноразово відзначалася госпіталізація з приводу серцевої недостатності III-IV функціонального класу за останній місяць. Випадки смерті в групі дронедарону були в основному наслідком наростання серцевої недостатності; ознак аритмогенної дії і збільшення частоти раптової смерті не виявили.
У дослідження ATHENA (плацебо-контрольоване, подвійне сліпе дослідження, в якому вивчалася ефективність дронедарона в дозі 400 мг два рази на день в профілактиці серцево-судинних госпіталізацій і смерті від будь-яких причин у пацієнтів з фібриляцією / тріпотінням передсердь) [95] були включені 4628 пацієнтів з пароксизмальною або персистуючою ФП або тріпотінням передсердь у поєднанні з серцево-судинними факторами ризику, яким призначали дронадерон в дозі 400 мг два рази на день і плацебо. Частота первинної кінцевої точки (смерть від будь-яких причин або серцево-судинна госпіталізація) склала 31,9% (734) в групі дронедарону і 39,4% (917) у групі плацебо (відношення шансів 0.76; 95% ДІ 0.69-0.84; P <0.0001). Лікування дронедароном призвело до недостовірного зниження смертності (відношення шансів 0.84; 95% ДІ 0.66-1.08; P = 0.18). Серцево-судинна смертність також була нижчою в групі дронедарону (2.7% vs. 3.9%; відношення шансів 0.71; 95% ДІ 0.51-0.98). Смертність від серцевої недостатності не відрізнялася між групами (відношення шансів 0.95; 95% ДІ 0.49-1.85; P = 0.89). При аналізі post-hoc було виявлено зниження ризику інсульту у хворих, які отримували дронедарон, яка не залежала від супутньої антитромботичної терапії. Результати лікування в декількох підгрупах (наприклад, у пацієнтів з серцевою недостатністю або коронарною хворобою серця) були схожими з такими у всій вибірці.
Коментар робочої групи:
Дизопірамід, хінідин, дофетилід, сібензолін та гідрохінідин в Україні станом на 01.10.2015р. не зареєстровані як лікарські засоби.
Етацизин дозволяє запобігти виникненню ФП у 58,8-84,2% пацієнтів. Небажані ефекти (запаморочення, головний біль, порушення зору), як правило, носять дозозалежний характер, проходять самостійно через декілька днів і лише в рідкісних випадках вимагають скасування препарату. Важкі проаритмогенні ускладнення спостерігаються в 3,1% випадків. Антиаритмічний ефект при прийомі всередину проявляється швидко (на першу-другу добу). Тривалість курсу лікування Етацизином підбирається індивідуально; препарат не накопичується (не кумулює) в органах і тканинах, що дозволяє проводити його призначення нескінченно довго. Є препаратом вибору при аритміях у поєднанні з псоріазом.
Хворим, що приймають аміодарон, згідно протоколу Американської асоціації щитоподібної залози, обов’язкові визначення рівню скринингу гормонів щитоподібної залози (рисунок10).
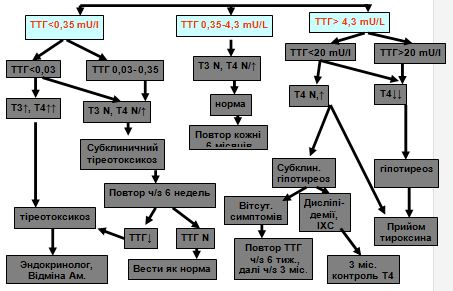
Вибір антиаритмічних препаратів
Антиаритмічну терапію у хворих з рецидивуючою ФП бажано починати з більш безпечних (хоча можливо і менш ефективних) препаратів. У подальшому за необхідності можна перейти на терапію більш ефективними і менш безпечними антиаритміками. Пацієнтам, які не страждають серйозним серцево-судинним захворюванням, можна призначати практично будь-які антиаритмічні препарати, які зареєстровані для лікування ФП. У більшості пацієнтів з ФП на початковому етапі лікування застосовують бета-блокатори для контролю частоти серцевих скорочень. Аміодарон доцільно призначати при неефективності інших антиаритмічних препаратів або наявності серйозного органічного захворювання серця.
Пацієнти з ізольованою ФП.
Якщо захворювання серця відсутнє або легко виражене, то профілактику рецидивів ФП логічно починати з бета-блокаторів, якщо аритмія чітко пов'язана з психічною або фізичною напругою (адренергічна ФП). Бета-блокатори менш ефективні у багатьох інших пацієнтів з ізольованою ФП, тому їм зазвичай призначають флекаїнід, пропафенон, соталол або дронедарон. Дизопірамід, що має виражену антихолінергічну активність, може застосовуватися при ФП, опосередкованою підвищеною активністю блукаючого нерва (рис. 10) [118,119].
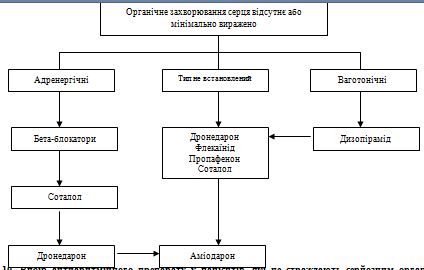
Рис. 10. Вибір антиаритмічного препарату у пацієнтів, які не страждають серйозним органічним захворюванням серця. Препарат першої лінії можна вибрати з урахуванням характеру аритмії (адренергічна або обумовлена активністю блукаючого нерва). Антиаритмічні препарати перераховані в алфавітному порядку
Пацієнти із захворюванням серця. Виділяють різні патофізіологічні варіанти ураження серця: гіпертрофія, ішемія і застійна серцева недостатність (рис. 11). У кожному з цих випадків рекомендується уникати застосування певних препаратів. У клінічних дослідженнях у хворих з ФП та іншими аритміями продемонстрована досить висока токсичність флекаїніду і пропафенону, яку пов'язували з аритмогенною дією і / або негативним ефектом. Соталол подовжує інтервал QT і може викликати поліморфну шлуночкову тахікардію типу пірует у чутливих пацієнтів, у тому числі страждають вираженою гіпертрофією ЛШ і серцевою недостатністю. Результати досліджень у пацієнтів, які перенесли інфаркт міокарда, показали відносну безпеку соталола при коронарній хворобі серця. У більшості хворих з серйозними органічними захворюваннями серця, особливо серцевою недостатністю та гіпертрофією ЛШ, в Європі було дозволено застосування тільки аміодарону (у Північній Америці в таких випадках застосовують також дофетилід). Висловлюються сумніви в безпеці тривалої терапії аміодароном у пацієнтів з серцевою недостатністю III функціонального класу [120].
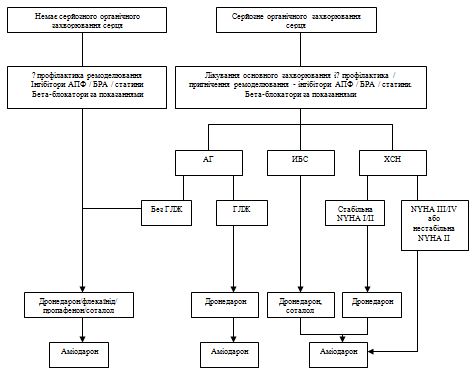
Рис. 11. Вибір антиаритмічного препарату з урахуванням основного захворювання. ХСН – хронічна серцева недостатність, АГ – артеріальна гіпертонія, ГЛШ – іпертрофія лівого шлуночка. Нестабільна – декомпенсація протягом попередніх 4-х тижнів. Антиаритмічні препарати перераховані в алфавітному порядку. ? – Ефективність додаткових коштів у профілактиці ремоделювання передсердь залишається спірною
Дати рекомендації з приводу вибору між аміодароном і дронедароном у пацієнтів з органічним захворюванням серця складно. Перевагою аміодарону є багаторічний досвід застосування, який підтвердив відсутність у препарату явної кардіотоксичності. З іншого боку, аміодарон часто викликає інші токсичні ефекти у високих дозах, хоча частота їх нижча при застосуванні доз ≤200 мг / добу. Аміодарон не вивчався у великих плацебо-контрольованих дослідженнях, схожих з ATHENA, проте в декількох мета-аналізах [111,113,121,122] і за допомогою моделювання [123] не підтверджений його сприятливий ефект на серцево-судинні наслідки. Враховуючи більш високу безпеку і можливість поліпшення результатів, дронадерон представляється кращим в якості препарату першої лінії, принаймні у пацієнтів з ФП і серцево-судинним захворюванням. При неефективності дронедарону може знадобитися призначення аміодарону.
Дронедарон може безпечно застосовуватися у пацієнтів з ГКС, хронічною стабільною стенокардією, гіпертонічним ураженням серця і стабільною серцевою недостатністю I-II функціонального класу. Його не слід призначати пацієнтам з серцевою недостатністю III-IV функціонального класу або нестабільною серцевою недостатністю. У клінічних дослідженнях ефективність і безпечність дронедарону у хворих з гіпертрофією лівого шлуночка або гіпертрофічною кардіоміопатією спеціально не вивчалися.
Пацієнти з гіпертрофією лівого шлуночка. У хворих з гіпертрофією лівого шлуночка соталол частіше надає аритмогенну дію. Можуть бути використані флекаїнід і пропафенон, однак викликає занепокоєння ризик аритмогенної дії, особливо пацієнтів з вираженою гіпертрофією лівого шлуночка (товщина стінки ЛШ ≥1,4 см відповідно до попередніх рекомендацій) і супутньою коронарною хворобою серця. Безпека та добра переносимість дронедарону були встановлені у великому дослідженні, що включало пацієнтів з гіпертонією і можливою гіпертрофією лівого шлуночка, тому його можна призначати таким пацієнтам. Застосування аміодарону доцільно, якщо рецидиви ФП продовжують чинити негативний вплив на якість життя пацієнтів.
Пацієнти з коронарною хворобою серця. Пацієнтам з коронарною хворобою серця не слід призначати флекаїнід [124] або пропафенон. Препаратами першої лінії є соталол і дронедарон. Дронедарон може бути кращим препаратом, враховуючи його безпеку. Аміодарон в таких випадках застосовують на останньому етапі лікування, враховуючи ризик екстракардіальних побічних ефектів.
Пацієнти з серцевою недостатністю. Дронедарон і аміодарон в Європі вважають єдиними засобами, які можуть безпечно застосовуватися у пацієнтів зі стабільною серцевою недостатністю I-II функціонального класу. Дронедарон протипоказаний хворим на серцеву недостатність III-IV функціонального класу і пацієнтам, яких протягом попередніх 4-х тижнів госпіталізували з приводу декомпенсації серцевої недостатності [117]. Таким хворим призначають аміодарон.
Результати останніх досліджень, особливо ATHENA, призвели до появи нової парадигми лікування хворих з ФП. У дослідженні ATHENA було показано, що профілактика повторних госпіталізацій може бути більш важливою для пацієнта і лікаря, ніж утримання синусового ритму як такого, особливо якщо паралельно проводиться інша терапія (антикоагулянти, контроль частоти серцевих скорочень, лікування супутніх захворювань), що має значення з прогностичної точки зору. Наявність симптомів ФП не була обов'язковим критерієм включення в дослідження ATHENA, проте вони, ймовірно, були у багатьох пацієнтів. Дослідження не дозволяє судити про ефективність дронедарону за відсутності симптомів. Дронедарон не порівнювали з іншими антиаритмічними препаратами або засобами, що уповільнюють ритм, у безсимптомних пацієнтів, тому наявні дані не дозволяють рекомендувати його широке застосування у таких хворих.
4.3.5.2 Катетерна абляція лівого передсердя
Метою розробки методів абляції було «лікування» ФП в певних вибірках пацієнтів. Результати тривалого спостереження таких хворих свідчать про те, що після абляції синусовий ритм більш стійкий, ніж на фоні антиаритмічної терапії, хоча пізні рецидиви розвиваються нерідко [128]. У більшість досліджень включали пацієнтів з пароксизмальною ФП і мінімальними ознаками органічного ураження серця.
Показання
В цілому катетерна абляція показана пацієнтам, у яких симптоми зберігаються, незважаючи на оптимальну медикаментозну терапію, що включають себе засоби для контролю частоти серцевих скорочень і ритму. При оцінці доцільності абляції слід брати до уваги наступні факти:
(1) Стадія захворювання передсердь (тип ФП, розмір лівого передсердя, анамнез аритмії).
(2) Наявність і тяжкість основного захворювання серця.
(3) Можливі альтернативи (антиаритмічні засоби, контроль частоти серцевих скорочень).
(4) Уподобання пацієнта.
Складна процедура абляції, яка може призвести до тяжких ускладнень, повинна бути адекватно обгрунтована у конкретного пацієнта з ФП. Важливе значення при виборі цього методу лікування має досвід лікаря, який виробляє процедуру. В опублікованих дослідженнях абляція практично завжди проводилася високо кваліфікованим фахівцями, які працюють в спеціалізованих лікувальних установах, в той час як у звичайній клінічній практиці вона може виконуватися менш кваліфікованими лікарями в закладах різного профілю.
Катетерну абляцію зазвичай проводять хворим з пароксизмальною ФП, яка резистентна принаймні до одного з антиаритмічних препаратів. Подібна практика обґрунтовується результатами численних рандомізованих досліджень, що проводилися в одному центрі, і багатоцентрових проспективних досліджень, в яких абляція приводила до поліпшення контролю ритму у порівнянні з антиаритмічними засобами (табл. 18). При мета-аналізі досліджень переважно у пацієнтів з пароксизмальною ФП також були продемонстровані переваги катетерної абляції перед антиаритмічною терапією [96,131-135]. Однак у більшість досліджень включали пацієнтів, резистентних до антиаритмічних препаратів, а тривалість спостереження була відносною короткою.
Таблиця 18. Рандомізовані дослідження, в яких порівнювали катетерну абляцію і антиаритмічну терапію або відсутність лікування у пацієнтів з ФП
|
Дослідження
|
Джерело
|
n
|
Вік, років
|
Тип ФП
|
Число ААП
|
Техніка абляції
|
Повторна абляція
|
Проведена абляція в групі ААП
|
Відсутність ФП через 1 рік
|
|
Абляція
|
ААП
|
|
Krittayaphong et al. 2003
|
Online
|
30
|
55±10 (абляція) 47±15 (ААП)
|
Пароксизмальна , персистуюча
|
≥1а
|
ІЛВ+ЛП+ КВП+ПП
|
Не вказано
|
Не вказано
|
79%
|
40%
|
|
Wazni et al. 2005 (RAAFT)
|
134
|
70
|
53±8 (аблація) 54±8 (ААП)
|
В основному пароксизмальна
|
Немає
|
ІЛВ
|
12%b
|
49%c
|
87%
|
37%
|
|
Stabile et al. 2005 (CACAF)d
|
Online
|
245
|
62±0 (абляція) 62±10 (ААП)
|
Пароксизмальна, персистуюча
|
≥2
|
ІЛВ+ЛП±КВП
|
Немає даних
|
57%
|
56%
|
9%
|
|
Oral et al. 2006e
|
Online
|
245
|
57±9
|
Персистуюча
|
≥1 (2,1±1,2)
|
Кругова абляція ЛВ
|
26% для ФП і 6% для тріпотіння
|
77%
|
74%
|
4%
|
|
Pappone et al. 2006 (APAF)
|
135
|
198
|
55±10 (абляція) 57±10 (ААП)
|
Пароксизмальна
|
≥2 (2±1)
|
Кругова абляція ЛВ + КВП
|
6% для ФП і 3% для передсердної тахікардії
|
42%
|
86%
|
22%
|
|
Jais et al. 2008 (дослідження A4)
|
133
|
112
|
51±11
|
Пароксизмальна
|
≥1
|
ІЛВ+ЛП+КТП
|
1,8±0,2, медіана 2 на пацієнта
|
63%
|
89%
|
23%
|
|
Forleo et al. 2008f
|
Online
|
70
|
63±9 (абляція) 65±6 (ААП)
|
Пароксизмальна, персистуюча
|
≥1
|
ІЛВ+ЛП+КТП
|
Не вказано
|
Не вказано
|
80%
|
43%
|
|
Wilber et al. 2010 (Thermocool)g
|
96
|
167
|
55,5 (абляція) 56,1 (ААП)
|
Пароксизмальна
|
≥1 (в середньому м 1,3)h
|
ІЛВ+ЛП+КТП+ПП
|
12,6% впродовж 80 днів після першої процедуриi
|
59%с
|
66%
|
16%
|
|
Packer et al. 2010
(STOP-AF)j
|
Online
|
245
|
56,7 (абляція) 56,4 (ААП)
|
Пароксизмальна
|
≥1b
|
Кріо-ІЛВ+ЛП
|
19% впродовж 90 днів після першої процедури
|
79%
|
69,9%
|
7,3%
|
a Аміодарон не застосовувався, проте пацієнти отримували бета-блокатори, антагоністи кальцію та серцеві глікозиди крім препаратів IA і IC класів.
b Виключаючи аміодарон. c Через 1 рік; не допускалось впродовж 1 року спостереження
d Всі пацієнти, яким проводилася абляція, отримували антиаритмічні препарати
e Пацієнти контрольної групи отримували аміодарон; за необхідності їм могли бути виконані дві електричні кардіоверсії протягом перших 3 міс. Аміодарон скасовували, якщо через 3 міс зберігався синусовий ритм. f Цукровий діабет 2 типу g Спостереження протягом 9 міс
h Пацієнтів, які отримували аміодарон протягом попередніх 6 міс, виключали
i Вважали ознакою неефективності лікування j Представлено на конференції Американської колегії кардіологів у 2010 році
A4 – Atrial Fibrillation Ablation versus Antiarrhythmic Drugs; APAF – Ablation for Paroxysmal Atrial Fibrillation study; CACAF – Catheter Ablation for the Cure of Atrial Fibrillation study; RAAFT 1- Radiofrequency Ablation Atrial Fibrillation Trial; STOP-AF – Sustained Treatment Of Paroxysmal Atrial Fibrillation. Online: www.escardio.org/guidelines).
ІЛВ – ізоляція легеневих вен, ЛП – ліве передсердя, ПП – праве передсердя, КТП – кавотрикуспідальний перешийок
Результати досліджень, в яких прямо порівнювали антиаритмічні засоби або катетерну абляцію в якості методів першої лінії у пацієнтів з пароксизмальною ФП, обмежені [134], проте наявні дані вказують на більш високу ефективність абляції [131]. Враховуючи високу ймовірність контролю ритму за допомогою катетерної абляції у хворих з пароксизмальною ФП і мінімальними ознаками ураження серця і відносну безпеку цього методу (якщо процедура виконується досвідченим фахівцем), абляція може розглядатися як метод лікування першої лінії у деяких пацієнтів (рис. 12).
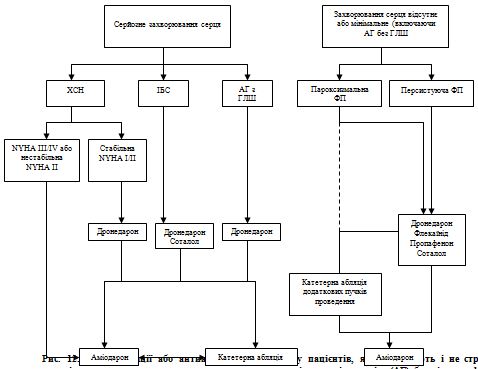
Рис. 12. Вибір абляції або антиаритмічної терапії у пацієнтів, які страждають і не страждають органічним захворюванням серця, включаючи артеріальну гіпертонію (АГ) без гіпертрофії лівого шлуночка (ГЛШ).
† Може знадобитися більш поширена абляція ЛП. * Звичайно проводять ізоляцію легеневих вен (ІЛВ). ХСН – хронічна серцева недостатність. Антиаритмічні препарати перераховані в алфавітному порядку. Абляція ЛП – метод вибору (пунктирна лінія; рекомендація IIb класу) у пацієнтів з пароксизмальною ФП при збереженні виражених симптомів незважаючи на адекватний контроль частоти серцевих скорочень у пацієнтів без серйозного захворювання серця, які відмовляються від антиаритмічної терапії.
Коментар робочої групи:
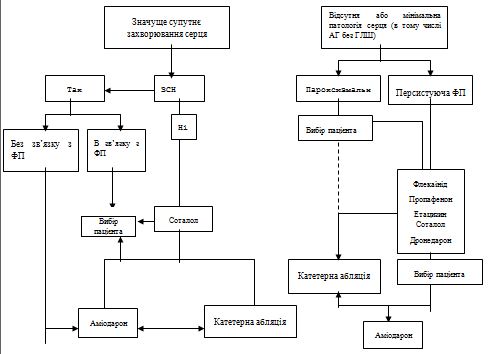
Рисунок 13. Вибір між абляцією та лікуванням протиаритмічними препаратами у пацієнтів з органічними ураженнями серця і без них. Запропонована інтеграція протиаритмічного препарату та катетерної абляції ФП у пацієнтів із значущою супутньою патологією серця та у тих, у яких відсутня або мінімальна патологія серця, в тому числі артеріальна гіпертензія (АГ) без гіпертрофії лівого шлуночка (ГЛШ). †Може знадобитися більш поширена абляція ЛП; *зазвичай достатньо проведення ІЛВ. ФП = фібриляція передсердь; ІХС = ішемічна хвороба серця; ЗСН = застійна серцева недостатність; АГ = артеріальна гіпертензія; ГЛШ = гіпертрофія лівого шлуночка; NYHA = Нью-Йоркська асоціація кардіологів [New York Heart Association]; ІЛВ = ізоляція легеневих вен. У кожному підрозділі протиаритмічні препарати наведені у алфавітному порядку. Будь ласка, зауважте, що застосування абляції лівого передсердя (ЛП) у якості терапії першої лінії (пунктирна лінія) є рекомендацією класу IIb для пацієнтів за пароксизмальною ФП та відсутньою або мінімальною патологією серця, які залишаються у значній мірі симптомними, незважаючи на контроль частоти серцевих скорочень, та які відмовляються від терапії протиаритмічними препаратами.
У пацієнтів з персистуючою або тривалої персистуючої ФП, які не страждають серйозним органічним захворюванням серця, стратегія лікування і коефіцієнт користь / ризик катетерної абляції остаточно не встановлені. Таким пацієнтам може знадобитися поширена або повторна абляція. Можливість цього втручання слід обговорювати тільки при неефективності антиаритмічних засобів.
Аміодарон може викликати серйозні небажані ефекти, особливо при тривалому лікуванні, тому катетерна абляція може служити альтернативою аміодарону у пацієнтів молодшого віку.
У пацієнтів з пароксизмальною і персистуючою ФП і серйозним органічним захворюванням серця перед абляцією рекомендується проводити антиаритмічну терапію. У таких випадках домогтися ефективної абляції важче. Підставою для втручання повинні бути виражені симптоми, пов'язані з аритмією. Результати абляції при персистуючій і довготривалій персистуючій ФП були варіабельними, але обнадійливими, проте в таких випадках часто доводиться вживати кілька спроб абляції. Ці втручання технічно складні і асоціюються з більш високим ризиком ускладнень, ніж ізоляція легеневих вен. Питання про те, чи слід призначити аміодарон або провести катетерну абляцію за неефективності менш токсичних антиаритмічних препаратів, слід вирішувати індвідуально. При цьому враховують вік пацієнта, тип і тяжкість ураження серця, розмір лівого передсердя, супутні захворювання і переваги пацієнта. Є дані, що підтверджують користь первинної абляції у пацієнтів з ФП і супутніми захворюваннями; наприклад, у пацієнтів з серцевою недостатністю після абляції було відзначено поліпшення фракції вибору і толерантності до фізичного навантаження [93,94]. При безсимптомному перебігу ФП користь абляції не встановлена.
Обстеження перед абляцією
Перед абляцією всім пацієнтам слід провести ЕКГ у 12 відведеннях та / або холтерівське моніторування, а також ехокардіографію для виключення органічного захворювання серця. Додаткові методи дослідження, такі як МРТ і КТ, дозволяють вивчити тривимірну геометрію передсердь і кількісно оцінити ступінь фіброзу передсердь. Щоб знизити ризик тромбоемболічних ускладнень під час абляції, слід виключити тромбоз лівого передсердя (найчастіше у вушку). Між черезстравохідною ехокардіографією і процедурою (рекомендований час ≤48 год) доцільно проводити адекватну антикоагуляцію.
Елімінація тригера шляхом ізоляції легеневих вен
Вивчення ролі осередкової активності в області гирл легеневих вен у розвитку епізодів ФП послужило основою для розробки методу електричної ізоляції цих тригерів від тканини передсердь. Для цього в гирла легеневих вен вводять циркулярний картуючий катетер, за допомогою якого проводиться сегментарна абляція з'єднувальних волокон. Характерний потенціал в легеневих венах визначається також за наявності синусового ритму, тому процедура абляції може бути виконана за відсутності критичної активності. Сегментарну абляцію волокон, що з'єднують ліве передсердя і легеневі вени, виробляє поблизу гирл судин, що підвищує ризик розвитку їх стенозу та / або оклюзії. Причинами рецидивів ФП можуть бути як відновлення проведення збудження між передсердям і легеневими венами, так і вогнища критичної активності при більш дистальній ізоляції легеневих вен.
Лінійна ізоляція легеневих вен і циркулярна абляція легеневих вен
Щоб полегшити процедуру і знизити ризик стенозу легеневих вен, було запропоновано проводити абляцію в області передсердя навколо однієї або обох легеневих вен. Раніше було показано, що антрум легеневих вен може бути субстратом для збереження ФП. В даний час переконливо доведено, що легеневі вени і антрум мають ключове значення для збереження ФП, тому виділення «тригера» і «субстрату» не дозволяє адекватно пояснити роль легеневих вен. Після ізоляції легеневих вен у 54% пацієнтів не розвиваються стійкі епізоди ФП. Це свідчить про те, що у значної частини хворих з пароксизмальною ФП легеневі вени є субстратом для збереження ФП.
Кругова абляція легеневої вени – це суто анатомічний підхід, що не припускає оцінки порушення зв'язку з відповідною ділянкою. Одночасне дослідження тканини легеневої вени не проводиться, тому необхідна тільки пункція перегородки. Після успішної ізоляції вичікування не потрібно, що скорочує тривалість втручання. При використанні даного методу до 45% легеневої вени не ізолюється, проведення між легеневою веною і лівим передсердям повністю не блокується, а легенева вена зберігає потенційну аритмогенність. Крім того, після такої абляції частіше зустрічаються «організовані» аритмії. Нещодавно було показано, що неповна ізоляція дозволяє передбачити їх розвиток. Ці дані є доказом на користь повної абляції.
Критерії ефективності ізоляції легеневих вен
На думку експертів, методи абляції, які передбачають ізоляцію легеневих вен та / або гирла легеневих вен, є основою більшості подібних втручань. Метою процедури повинна бути повна електрична ізоляція легеневих вен [33]. Загальноприйнятим критерієм успіху втручання вважають повну ізоляцію всіх легеневих вен. Додатковим обґрунтуванням доцільності ізоляції легеневих вен служать дослідження, в яких вивчалися рецидиви ФП після абляції. Було встановлено, що вони розвиваються у випадку відновлення зв'язку між передсердям і легеневою веною. Ефективність повторної ізоляції легеневих вен в найближчому і більш віддаленому періоді досягала 90% у підібраних пацієнтів.
Незважаючи на усунення тригерів ФП, більшості пацієнтів з персистуючою або тривалою персистуючою ФП може знадобитися додаткова модифікація субстрату. Концептуальною основою цього підходу є теорія множинних дрібних хвиль (див. Розділ 2.2.2). Пацієнтам проводять лінійну абляцію, щоб попередити появу вогнищ циркуляції збудження. Вивчалися різні конфігурації лінійної абляції, проте вибір відповідної лінії у конкретного пацієнта залишається важким завданням. Щоб домогтися повної блокади проведення, лінійна абляція повинна бути трансмуральною, проте забезпечити таку абляцію часто складно.
Альтернативні методи абляції
Щоб подолати обмеження послідовної абляції і уникнути ризику неповної ізоляції, розроблені пристрої, що дозволяють ізолювати легеневі вени за допомогою одного (або кількох) розряду. Ці пристрої вивчалися переважно у пацієнтів з пароксизмальною ФП, які не страждають органічним захворюванням серця або вираженою дилатацією лівого передсердя. Для втручання в основному використовуються радіочастотні хвилі, хоча існують і альтернативні джерела енергії, такі як Кріотерм, ультразвук і лазерне випромінювання. Рандомізовані дослідження поки не проводилися, що не дозволяє судити про переваги цих методів перед стандартною послідовною абляцією. Враховуючи можливість надмірного пошкодження навколишніх тканин, наприклад, формування свищів між передсердям і стравоходом, необхідно довести, що нові пристрої є простими і безпечними.
Альтернативні методи модифікації субстрату
Робилися спроби абляції передсердної тканини, генеруючої складні фракційні електрограми, без ізоляції легеневих вен. Хоча результати, отримані в окремих центрах, виявилися обнадійливими, в проспективних рандомізованих дослідженнях ефективність втручання не була підтверджена. Цікаво відзначити, що рецидиви аритмії після подібних процедур пов'язані з активністю легеневих вен. Деякі автори проводили радіочастотну абляцію гангліонарного сплетення на додаток до ізоляції легеневих вен. Користь цього методу не встановлена.
Ускладнення
Катетерна абляція супроводжується різними ускладненнями (табл. 17) [129-131]. Найбільш серйозними вважають ускладнення, які призводять до незворотних змін або смерті, вимагають втручання або госпіталізації (або збільшення її тривалості). Слід зазначити можливість більш рідкісних ускладнень з серйозними наслідками, особливо якщо замість радіочастотного випромінювання використовуються інші джерела енергії.
Таблиця 17. Ускладнення катетерної абляції ФП
|
Тип
|
Типові симптоми
|
Частота
|
Методи лікування і наслідки
|
Як знизити ризик?
|
|
Тромбоемболії
ТІА
Інсульт
|
Неврологічний дефіцит, що залежить від локалізації ураження
|
0,93%
0,2% (0,6%)
0,3% (0,28%)
|
Обговорити можливість лізису
|
Використовувати катетер з кінчиком, що промивається. Контролювати АВС кожні 30 хв і коригувати шляхом в / в введення гепарину
|
|
Стеноз/оклюзія легеневої вени
|
Кашель, задишка при навантаженні, пневмонія, кровохаркання
|
Залежно від місця абляції по відношенню до гирла легеневої вени. До 10% при фокальній абляції легеневої вени, <5% при сегментарній абляції
|
Дилатація / реканалізація легеневої вени та імплантація стенту. Часто розвивається рестеноз стенту
|
Уникати абляції всередині легеневої вени
|
|
Утворення передсердно-стравохідного свища
|
Непояснена лихоманка, дисфагія, судоми
|
<1%
|
Негайна операція
|
Уникати пошкодження задньої стінки лівого передсердя
|
|
Тампонада
В гострому періоді
Пізня (через декілька днів)
|
Гіпотонія, зупинка серця
|
0,8%
до 6%
Не відома
|
Терміновий перикардіоцентез
|
Уникати механічного пошкодження під час пункції перегородки і надмірного натискання
|
|
Пошкодження діафрагмального нерва (в основному праворуч)
|
Параліч діафрагми із задишкою при навантаженні і в спокої
|
Може бути минущим
|
Вичікування
|
Встановити локалізацію пошкодження діафрагмального нерва по відношенню до гирла легеневої вени шляхом стимуляції. Уникати розтягування гирла легеневої вени (в основному при використанні балонного катетера)
|
|
пошкодження стравоходу
|
Кишкові симптоми (здуття і т.д.)
|
Може бути минущим. Розвивається через кілька годин або днів після втручання. 1% у 367 пацієнтів
|
За неохідності дилатація пілоруса, введення ботуліна
|
Невідомі
|
|
Артеріо-венозна фістула
|
Біль у місці пункції
|
0,43%
|
Компресія. Хірургічне втручання потрібне рідко
|
Обережно виконувати пункцію
|
|
формування аневризми
|
Біль у місці пункції
|
0,5-0,53%
|
Вичікування. Введення тромбіну
|
Обережно виконувати пункцію
|
|
променеве ушкодження
|
Біль і почервоніння в місці опромінення
|
Розвивається у віддаленому періоді. Гостре ураження відзначається дуже рідко
|
Лікування як при опіках
|
Уникати зайвого опромінення і використовувати техніку ALARA. Застосування 3D картування і пульс-флюороскопії. Вибір оптимальної тривалості флюороскопії
|
|
Пошкодження мітрального клапана
|
Утворення надлишкової рубцевої тканини після абляції тканини клапану
|
дуже рідко
|
Обережне видалення катетера. хірургічне втручання
|
Визначення анатомії лівого передсердя / легеневої вени в 3D режимі. Моніторування сигналів при маніпуляції катетером
|
|
Гостре ураження коронарної артерії
|
Біль у грудях, підйом сегмента ST, гіпотонія
|
Дуже рідко. У 1 з 356 пацієнтів
|
Стандартне черезшкірне втручання з приводу гострої коронарної оклюзії
|
Уникати надмірного впливу розряду на коронарні артерії. По можливості уникати абляції інтракоронарного синуса
|
|
повітряна емболія
|
Гостра ішемія, гіпотонія, атріовентрикулярна блокада, зупинка серця
|
|
Аспірація повітря, спостереження і вичікування, стимуляція, за необхідності серцево-легенева реанімація
|
Ретельна аспірація всіх провідників. Постійний позитивний тиск в області трансептального провідника
|
|
Гематома в місці пункції
|
Біль, набрякання, зміна кольору шкіри
|
Часто
|
Компресія. У рідкісних випадках оперативне втручання. Видалення провідника після нормалізації АЧЗ
|
Обережна компресія. Видалення провідника після нормалізації АЧЗ
|
|
Смертність
|
0,7%
|
|
|
|
АЧЗ – активований час згортання, ALARA = якнайнижче
Спостереження
Антикоагуляція. Безпосередньо після абляції застосовують НМГ або НФГ внутрішньовенно, щоб створити «міст» до відновлення антикоагуляції, яку продовжують принаймні протягом 3-х місяців [136], хоча деякі центри не переривають антикоагулянтну терапію під час втручання. Доцільність подальшої терапії пероральними антикоагулянтами оцінюють з урахуванням ризику інсульту (див. Розділ 4.1). Скасовувати варфарин після абляції зазвичай не рекомендують пацієнтам з високим ризиком інсульту (див. Розділ 4.1), так як ФП – це хронічна і прогресуюча аритмія.
Моніторування рецидивів ФП. Методи оцінки середньострокових і довгострокових результатів абляції ФП продовжують обговорюватися. Може бути достатнім контроль симптомів, купіювання яких є основною метою абляції ФП. Щоб визначити ефективність різних втручань і поліпшити техніку абляції, необхідно проводити систематичне стандартизоване моніторування ЕКГ [3]. На думку експертів, пацієнта слід обстежити через 3 місяці після втручання, а потім кожні 6 місяців протягом принаймні 2-х років [33]. Істинна частота рецидивів буде значно заниженою (див. Розділ 3.4).
Результати мета-аналізу і рандомізованих досліджень, в яких порівнювали абляцію та антиаритмічні засоби
Хоча лікарські засоби залишаються основою лікування ФП, в останні роки зростає роль катетерної абляції. За даними нещодавно проведеного мета-аналізу, ефективність катетерної абляції і антиаритмічної терапії склала 77% і 52%, відповідно [131]. Схожі результати були отримані в інших мета-аналізах [134,140,141], в одному з яких ізоляція легеневих вен у хворих з пароксизмальною або персистуючою ФП супроводжувалася значним збільшенням вірогідності відсутності нападів аритмії через 1 рік (відношення шансів 9.74; 95% ДІ 3.98-23.87; P <0.001) [140]. У декількох проспективних багатоцентрових дослідженнях була підтверджена більш висока ефективність катетерної абляції в порівнянні з антиаритмічною терапією. Багатьом пацієнтам проводили повторні втручання, що вказує на обмеження цього методу лікування. Крім відновлення зв'язку між ізольованими легеневими венами з тканиною передсердь основною причиною аритмій, що виникають після абляції, є ятрогенна передсердна тахікардія за механізмом re-entry. У випадку розвитку аритмії може знадобитися повторна абляція. Очікуються результати триваючих багатоцентрових досліджень в певних підгрупах пацієнтів, наприклад, з ФП і застійною серцевою недостатністю (CASTLE-AF, AMICA). Поки немає даних, що підтверджують ефективність успішної абляції ФП в профілактиці смертності, проте це питання вивчається у великому проспективному міжнародному дослідженні CABANA. Можна припустити, що абляція ФП в рамках стратегії контролю ритму найбільш ефективна і корисна на ранньому етапі розвитку захворювання [23]. Клінічна ефективність раннього контролю ритму вивчається в дослідженні EAST. Очікується, що обидва дослідження будуть завершені в 2015 році.
Рекомендації щодо абляції лівого шлуночка
|
Рекомендації
|
Клас
|
Рівень
|
Джерело
|
|
Абляція тріпотіння передсердя рекомендується в рамках процедури абляції ФП, якщо тріпотіння було виявлено до абляції або з'явилося під час абляції ФП
|
I
|
B
|
33
|
|
Катетерна абляція пароксизмальної ФП обгрунтована, якщо симптоми зберігаються незважаючи на антиаритмічну терапію
|
IIa
|
A
|
96,131,132,133, 135,137,138
|
|
Абляція можлива при персистуючій ФП, рефрактерної до антиаритмічної терапії
|
IIa
|
B
|
33
|
|
Перед поновленням терапії пероральними антикоагулянтами (продовжують мінімум протягом 3 міс) після абляції можливе призначення НМГ або в/в введення НФГ. При оцінці доцільності подальшої антикоагуляції враховують індивідуальні фактори ризику інсульту
|
IIa
|
C
|
|
|
Продовження антикоагулянтної терапії рекомендується пацієнтам з 1 основним фактором ризику або ≥2 клінічно значущими неосновними факторами ризику (CHA2DS2-VAS ≥2)
|
IIa
|
B
|
136
|
|
Катетерна абляція у пацієнтів з ФП і серцевою недостатністю можлива, якщо антиаритмічна терапія, включаючи аміодарон, що не зменшує симптоми
|
IIb
|
B
|
93,94
|
|
У пацієнтів з пароксизмальною ФП, які не страждають серйозним захворюванням серця, Катетерна абляція перед антиаритмічною терапією можлива, якщо симптоми зберігаються незважаючи на адекватний контроль частоти серцевих скорочень
|
IIb
|
B
|
131
|
|
Катетерна абляція можлива у пацієнтів з тривалою персистуючою ФП, рефрактерною до антиаритмічних препаратів
|
IIb
|
C
|
|
4.3.5.3 Хірургічна абляція
ФП – це незалежний фактор ризику несприятливих результатів після операцій на серці. Вона асоціюється з більш високою періопераційною смертністю, особливо у пацієнтів з фракцією викиду менше 40% [139]. Наявність ФП перед реконструктивною операцією на мітральному клапані свідчить про підвищений ризик оперативного втручання і дозволяє прогнозувати розвиток пізніх ускладнень з боку серця та інсульту. Хоча незалежний вплив ФП на виживаність у віддаленому періоді не встановлено, відновлення синусового риму покращує результати [139]. Хірургічна абляція в порівнянні з катетерною дозволяє домогтися повної ізоляції вогнищ критичної активності, а також вушка лівого передсердя.
Техніка операції
Метод хірургічної абляції є операція "лабіринт". Ефективність оперативного втручання (тобто відсутність ФП) протягом 15 років досягає 75-95%. У хворих з вадою мітрального клапана операція на клапані сама по собі не знижує ризик розвитку рецидивів ФП або інсульту, проте операція «лабіринт» призводить до поліпшення результатів і сприяє відновленню скорочувальної функції передсердь. Операція складна і супроводжується підвищеним ризиком смерті і серйозних ускладнень, тому вона проводиться рідко [143,144]. Хірургічна ізоляція легеневих вен ефективно відновлює синусовий ритм у пацієнтів з постійною ФП на тлі вади мітрального клапана.
Альтернативні джерела енергії
Використання альтернативних джерел енергії дозволяє викликати блокаду внутрішньопередсердного проведення без хірургічного розрізу. Подібне втручання більш коротке і менш інвазивне і не вимагає зупинки серця. У невеликих рандомізованих дослідженнях ці методи приводили до збільшення частоти відновлення синусового ритму, підвищення толерантності до фізичного навантаження і зниження концентрацій мозкового натрійуретичного пептиду в плазмі і ризику інсульту [140].
Радіочастотна абляція: синусовий ритм зберігається приблизно в 85% випадків через 1 рік і в 52% випадків через 5 років. Тривалість аритмії і розмір лівого передсердя дозволяють передбачити розвиток рецидивів.
Ефективність кріоабляції через 1 рік становила 87%.
Високоінтенсивний спрямований ультразвук викликає нагрівання тканини, коагуляційний некроз і блокаду проведення. Через 18 місяців ефективність втручання досягла 86%. Факторами, що погіршують результати втручання, були значне збільшення розміру лівого передсердя, похилий вік, тривале збереження ФП, артеріальна гіпертонія і апное під час сну [33].
Представляється перспективним застосування інших методів, зокрема торакоскопії і відеоспостереження, однак їх поки спеціально не порівнювали зі стандартним хірургічним лікуванням ФП.
Роль вегетативної нервової системи
Абляція нервового сплетення або перетин блукаючого нерва використовуються для контролю або лікування пароксизмальної ФП. Віддалені результати втручання поки не відомі. Перші дослідження не підтвердили його переваги перед ізоляцією легеневих вен.
Лікування після хірургічної абляції
Після хірургічної абляції відбувається зворотне ремоделювання, яке часто ускладнюється аритміями. Антиаритмічну і антикоагулянтну терапію продовжують протягом принаймні 3-х місяців. Рішення про припинення лікування приймають на підставі клінічного обстеження, ЕКГ і ехокардіографії через 3, 6 і 12 місяців.
Рекомендації щодо хірургічної абляції ФП
|
Рекомендації
|
Клас
|
Рівень
|
Джерело
|
|
Хірургічна абляція ФП можлива у пацієнтів, яким проводяться операції на серці
|
IIa
|
A
|
139,141,142
|
|
Хірургічна абляція можлива при безсимптомній ФП, якщо проводиться хірургічне втручання, а ризик мінімальний
|
IIb
|
C
|
|
|
Мінімально інвазивна хірургічна абляція ФП можлива, якщо не проводиться хірургічне втручання. Її виконують за неефективності катетерної абляції
|
IIb
|
C
|
|
Коментар робочої групи:
Спеціальні рекомендації щодо лікування фібриляції передсердь шляхом абляції
Таблиця 18. Застосування антикоагулянтів до та після процедур абляції та імплантації пристроїв.
|
|
Алгоритм дії
|
Рівень доказів
|
|
Антиагреганти
|
|
|
|
Первина профілактика інфаркту міокарда
|
Відмінити антиагреганти за 3-7 діб до процедури, в залежності від препарату.
|
Нерандомізоване дослідження, думка експкртів
|
|
Подвійна антиагрегантна терапія після стентування або гострого коронарного синдрому
|
|
Нерандомізоване дослідження, думка експертів
|
|
Період невисокого ризику
|
Продовжити тільки аспірин (невисокий ризик ускладнень)
|
|
Період високого ризику
|
Продовжити терапію в повному обсязі (високий ризик ускладнень)
|
|
Терапія варфарином
|
Відмінити варфарин за 3-6 днів до процедури, або продовжувати під контролем МНВ (нижня межа рекомендованого МНВ), вирішує лікар в залежності від оцінки ризиків
|
Міжнародний консенсус експертів
|
|
Нові пероральні антикоагулянти
|
Відмінити за 1-3 дні до процедури або продовжувати в залежності від оцінки ризику. Відновити після досягнення надійного гемостазу.
|
Нерандомізовані дослідження, Консенсус експертів
|
З'явилась деяка інформація щодо застосування НПАК при лікуванні пацієнтів з фібриляцією передсердь, що потребують процедури ізоляції легеневих вен.
За результатами одного багатоцентрового не експериментального дослідження 290 пацієнтів, методика лікування (відхилена виробником) шляхом безперервного застосування дабігатрану у дозі 150 мг 2 рази/добу окрім дози, прийнятої вранці, коли проводилась операція (незалежно від функції нирок), гепаринізація під контролем активованого часу згортання крові під час операції та відновлення прийому дабігатрану через 0 – 3 години після від’єднання провідника у кілька разів підвищували ризик виникнення кровотечі та тромбоемболічних ускладнень у порівнянні із безперервною терапією антагоністами вітаміну К (МНВ 2.0–3.5).
Два інші дослідження з подібним протоколом та застосуванням препарату у дозі 150 мг 2 рази на добу, відповідно, 110 мг 2 рази на добу (у японських пацієнтів), проте відновлення абляції ввечері не виявило різниці щодо ризику виникнення кровотечі та тромбоемболічних ускладнень.
Крім того, за результатами іншого дослідження, в якому прийом дабігатрану було припинено раніше (за 36 годин за умови нормальної функції нирок), вводився еноксапарин у дозі 0,5 мг/кг одразу після абляції та через 12 годин, та відновлено прийом дабігатрану через 22 години після абляції, у 123 пацієнтів не спостерігалось ризику виникнення кровотеч або тромбоемболічних явищ.
Інше широке дослідження методом «випадок-контроль» показало, що методика лікування при припиненні застосування дабігатрану за≥24 годин перед абляцією та відновлення його прийому через 4 години після абляції була такою ж ефективною та безпечною, як і лікування за допомогою безперервного прийому варфарину.
У рандомізованому дослідженні ROCKET AF при використанні ривароксабану під час проведення абляції у обмеженої кількості пацієнтів не було виявлено різниці щодо риску виникнення кровотеч та тромбоемболічних ускладнень порівняно з АВК.
У багатоцентровому дослідженні (Lakkireddy еt al., 2013) за участі 642 пацієнтів та було доведено безпечність та ефективність безперервної терапії ривароксабаном при проведенні процедури абляції у пацієнтів із ФП.
На сьогоднішній день у багатьох дослідженнях (Dillier et al, 2013; Stepanyan et al, 2013; Bockstall et al, 2013; Gadiyaram et al, 2013; Musat et al, 2013; Gangireddy et al, 2013; Eitel et al., 2013) показано, що терапія ривароксабаном у пацієнтів, яким здійснюється абляція, в порівнянні із АВК однаково ефективна в попередженні тромбоемболічних подій та безпечна.
Таким чином, з наявними даними, у випадку лікування методом «бриджинг-терапії» або безперервної антикоагулянтної терапії, НПАК вважаються ефективними, в той час як різке припинення прийому НПАК і/або відсутність «бриджинг-терапії» може бути менш безпечним, як щодо ризику тромбоемболічних ускладнень, так і ризику кровотечі.
4.4 Додаткова терапія
Попередження або уповільнення ремоделювання міокарда на тлі артеріальної гіпертонії, серцевої недостатності або запалення (наприклад, після хірургічного втручання) дозволяє уникнути розвитку ФП (первинна профілактика) або знизити частоту рецидивів аритмії або її трансформації в постійну форму (вторинна профілактика) [143]. З цією метою зазвичай застосовують інгібітори ферменту (АПФ), блокатори рецепторів ангіотензину II (БРА), антагоністи альдостерону, статини і омега-3 поліненасичені жирні кислоти.
4.4.1 Інгібітори АПФ та блокатори рецепторів ангіотензину II
Інгібітори АПФ і БРА пригнічують аритмогенну дію ангіотензину II, який стимулює розвиток фіброзу і гіпертрофії передсердь внаслідок порушення утилізації кальцію, зміни функції іонних каналів, активації медіаторів окислювального стресу і посилення запалення. В експериментальних умовах переконливо доведені антиаритмичні і протифіброзні властивості інгібіторів АПФ і БРА за ФП [144,145].
Первинна профілактика
Застійна серцева недостатність. При ретроспективному аналізі результати великих рандомізованих досліджень у хворих з дисфункцією ЛШ і серцевою недостатністю було виявлено зниження частоти розвитку ФП при лікуванні інгібіторами АПФ і БРА у порівнянні з плацебо. За даними декількох мета-аналізів, терапія препаратами цих класів достовірно знижує ризик ФП на 30-48% [145-148]. Сприятливий ефект був менш вираженим у пацієнтів з серцевою недостатністю та збереженою систолічною функцією ЛШ [49].
Артеріальна гіпертонія.
При мета-аналізах була відзначена перевага терапії на основі інгібіторів АПФ або БРА, однак тільки в одному мета-аналізі було виявлено статистично значуще зниження відносного ризику ФП на 25% [147]. Ця тенденція в основному відображала значне зниження частоти вперше виявленої ФП (на 33%) при лікуванні лозартаном у порівнянні з атенололом (6.8 vs. 10.1 на 1000 пацієнтів-років, відповідно) у дослідженні LIFE, в яке включали пацієнтів з гіпертрофією ЛШ [150]. Тим не менш, результати подальшого дослідження VALUE [151] і ретроспективних досліджень в США і Великобританії (на підставі баз даних) показали, що терапія на основі інгібіторів АПФ або БРА дозволяє затримати розвиток ФП у пацієнтів з артеріальною гіпертонією, в тому числі у звичайній клінічній практиці.
Серцево-судинні фактори ризику.
Ефективність інгібіторів АПФ і БРА в профілактиці ФП була менш очевидною у пацієнтів з множинними факторами ризику, включаючи артеріальну гіпертонію, цукровий діабет, коронарну хворобу серця, цереброваскулярні хвороби, захворювання периферичних артерій, гіперхолестеринемію і т.п., які брали участь у дослідженнях HOPE і TRANSCEND [143]. У цих дослідженнях раміприл і телмісартан, відповідно, не знижували ризик розвитку ФП у порівнянні з плацебо.
Вторинна профілактика
У кількох відносно невеликих проспективних рандомізованих контрольованих дослідженнях було показано, що інгібітори АПФ або БРА у поєднанні з антиаритмічними засобами, зазвичай аміодароном, здійснюють додатковий сприятливий вплив на ризик рецидивів ФП після кардіоверсії у порівнянні з антиаритмічною терапією [152,153]. При мета-аналізі цих досліджень було виявлено достовірне зниження ризику розвитку рецидивів ФП на 45-50% [145-148]. Однак у подвійному сліпому, плацебо-контрольованому дослідженні CAPRAF не підтверджений сприятливий ефект кандесартану після відновлення синусового ритму у пацієнтів, які не отримували антиаритмічні препарати [154].
Дані, що обгрунтовують застосування інгібіторів АПФ або БРА у пацієнтів з пароксизмальною або персистуючою ФП, яким не проводиться електрична кардіоверсія, залишаються суперечливими. У рандомізованих контрольованих дослідженнях у хворих на артеріальну гіпертонію було виявлено зниження частоти рецидивів пароксизмальної ФП на фоні терапії на основі БРА чи інгібіторів АПФ в порівнянні з атенололом або амлодипіном, а також при комбінованій терапії БРА або інгібіторами АПФ і аміодароном в порівнянні з монотерапією аміодароном [145]. У кількох відносно невеликих дослідженнях був відзначений сприятливий ефект інгібіторів АПФ / БРА у пацієнтів з незначними змінами серця (в основному артеріальна гіпертонія без гіпертрофії ЛШ) і пароксизмальної або недавно розвинутої персистуючої ФП [155,156].
Проте в найбільшому дослідженні GISSI-AF у 1442 пацієнтів із серцево-судинними факторами ризику (у 85% артеріальна гіпертонія) і пароксизмальною або персистуючою ФП (незабаром після кардіоверсії) приєднання валсартану до оптимальної медикаментозної терапії (включаючи антиаритмічні засоби та інгібітори АПФ) протягом 1 року не призвело до зниження часу до першого рецидиву ФП (відношення шансів 0,99; 95% ДІ 0.85-1.15; P = 0.84) і числа пацієнтів, у яких спостерігалося більше 1 рецидиву ФП (26.9% vs. 27.9%), у порівнянні з плацебо [157]. Валсартан не давав також додаткового ефекту у невеликого числа пацієнтів без супутніх серцево-судинних захворювань, але з дилатацією лівого передсердя.
Попередні результати японського дослідження J-RHYTHM II у 318 пацієнтів з артеріальною гіпертонією і пароксизмальною ФП не підтвердили сприятливий вплив кандесартану в порівнянні з амлодипіном на частоту і тривалість рецидивів ФП, які реєстрували при щоденному моніторуванні по телефону, або частоту трансформації ФП в постійну форму (8 % vs. 14%) протягом 1 року. У ретроспективних дослідженнях інгібітори АПФ і БРА не знижували частоту рецидивів ФП після абляції легеневих вен.
Ефективність у профілактиці серцево-судинних результатів
У дослідженні LIFE терапія на основі лозартану знижувала ризик серцево-судинних результатів у порівнянні з атенололом у хворих з ФП. Так, частота первинної комбінованої кінцевої точки (серцево-судинна смерть, інсульт та інфаркт міокарда) знизилася на 42%, серцево-судинна смертність – на 42%, частота інсульту – на 45%. Була відзначена також тенденція до зниження загальної смертності. Проте ні в дослідженні VALUE [151], ні в дослідженні GISSI-AF [157] не було виявлено поліпшення результатів на тлі терапії на основі БРА порівняно з амлодипіном або плацебо. У дослідженні ACTIVE I у 9016 пацієнтів з ФП і факторами ризику лікування ірбесартаном не привело до зниження сумарної частоти інсульту, інфаркту міокарда та судинної смерті, але значно знизило частоту госпіталізацій з приводу серцевої недостатності.
Таким чином, у хворих з дисфункцією і гіпертрофією ЛШ виявлено значне зниження частоти розвитку вперше виявленої ФП при лікуванні інгібіторами АПФ або БРА, проте їх користь переконливо не доведена у пацієнтів з помірним органічним ураженням серця і рецидивуючої ФП. Перевага одного класу інгібіторів ренін-ангіотензин-альдостеронової системи над іншим не встановлено [146,147,155]. Антиаритмічний ефект інгібіторів АПФ і БРА у хворих з ФП вивчається в декількох спеціальних дослідженнях, а також у рамках більш масштабних досліджень.
4.4.2 Антагоністи альдостерону
У пацієнтів з первинним гіперальдостеронізмом ризик розвитку ФП в 12 разів вищий, ніж у пацієнтів з есенціальною гіпертонією. У хворих з ФП спостерігали збільшення рівнів альдостерону в плазмі. Застосування спіронолактону в дослідах на собаках пригнічувало розвиток фіброзу передсердь і перешкоджало розвитку індукованої ФП. Роль антагоністів альдостерону в клінічних дослідженнях спеціально не вивчалася, однак попередні дані свідчать про те, що спіронолактон знижує частоту рецидивів ФП після електричної кардіоверсії у пацієнтів з артеріальною гіпертонією і легкою дисфункцією ЛШ. В даний час продовжуються декілька досліджень спіронолактону і еплеренону.
4.4.3 Статини
Запалення може бути ключовим механізмом розвитку деяких форм ФП. В епідеміологічних та наглядових дослідженнях у пацієнтів з вперше розвинутою і рецидивуючою ФП відзначали збільшення рівнів С-реактивного білка і запальних цитокінів (інтерлейкінів 1b і 6 і фактора некрозу пухлини). Профілактичний ефект статинів при ФП пов'язують з поліпшенням обміну ліпідів і профілактикою прогресування атеросклерозу, протизапальною і антиоксидантною дією, поліпшенням ендотеліальної функції і придушенням активації нейрогуморальних систем, зміною плинності мембран і провідності іонних каналів [158]. Статини беруть участь у регуляції активності різних металопротеїназ; цей ефект може відігравати роль у регуляції структурного ремоделювання при ФП (дилатація та фіброз). У дослідах на тваринах з ФП статини придушували електричне та структурне ремоделювання передсердь і перешкоджали розвитку ФП [159].
Первинна профілактика
Високо якісні дослідження у хворих з ФП були поодинокими, а базу даних в основному складають результати спостережних і ретроспективних досліджень [159]. У деяких дослідженнях, особливо у пацієнтів з дисфункцією ЛШ і серцевою недостатністю, було виявлено зниження ризику розвитку вперше виявленої ФП на 20-50%, проте результати лікування у пацієнтів з артеріальною гіпертонією, коронарною хворобою серця і ОКС менш однозначні, хоча спостерігалася загальна тенденція на користь статинів [159]. Статини знижували частоту розвитку ФП у пацієнтів з постійним водієм ритму на 57%, проте дослідження були ретроспективними і занадто невеликими, щоб спеціально рекомендувати застосування статинів для профілактики ФП після імплантації постійного водія ритму [160].
Післяопераційна ФП.
У декількох ретроспективних, спостережних і рандомізованих контрольованих дослідженнях [159], включаючи ARMYDA-3 [161], а також у систематизованому огляді [161] було виявлено зниження частоти післяопераційної ФП на фоні терапії статинами. Однак в декількох великих ретроспективних дослідженнях не було відзначено зниження частоти розвитку ФП після операцій; більше того, вказували навіть на їх аритмогенні властивості. Тим не менш, за даними мета-аналізу всіх досліджень в хірургічній практиці (3 рандомізованих контрольованих дослідження і 10 спостережних досліджень в цілому у 17643 пацієнтів), відносний ризик розвитку будь-якої ФП при лікуванні статинами склав 0.78 (95% ДІ 0.67-0.90; P < 0.001), а вперше виявленої – 0.66 (95% ДІ 0.51-0.84; P <0.001). Продемонстрована залежність ефекту статинів від дози.
Вторинна профілактика
Ефективність статинів у профілактиці пароксизмальної або недавно розвинутої ФП була вищою, ніж у профілактиці рецидивуючої персистуючої ФП або ФП після абляції лівого передсердя [159]. Рандомізовані дослідження не підтвердили користь статинів після кардіоверсії [163]. За даними мета-аналізу, ефективність статинів у профілактиці ФП залежала від типу дослідження і вибірки пацієнтів [164,165]. Більш виражений ефект спостерігався в ранніх спостережних дослідженнях.
Таким чином, дані, що підтверджують ефективність статинів у первинній або вторинній профілактиці ФП (за винятком післяопераційної), недостатні для того, щоб дати однозначні рекомендації. В даний час немає загальної думки з приводу інтенсивності та тривалості лікування статинами або вибору препарату.
4.4.4. Поліненасичені жирні кислоти
Омега-3, або n-3 ПНЖК (в основному ейкозапентаєнова і докозагексаєнова кислоти) – це універсальні компоненти біологічних мембран. Ці кислоти надають стабілізуючу дію на мембрани, пригнічують викликане розтягуванням вкорочення рефрактерного періоду серця, знижують флюоресцентную анизотропию мембран і окислювальний стрес [161]. Крім того, ПНЖК здійснюють пряму електрофізіологічну дію на деякі іонні канали, включаючи натрієві та ультрашвидкі калієві канали, і обмін натрію і кальцію. В експериментах ПНЖК зменшували електричне ремоделювання передсердь та їх структурні зміни [159].
Первинна профілактика
Загальна популяція. Результати епідеміологічних досліджень виявилися суперечливими [159]. Хоча в дослідженнях Cardiovascular Health Study і Kuopio Ischaemic Heart Disease Risk Factor Study було виявлено значне зниження ризику розвитку ФП на 30-35% на тлі збільшення споживання ПНЖК, інші великі популяційні дослідження не підтвердили ці дані. Більш висока ефективність у профілактиці ФП певної кислоти, наприклад, докозагексаєнової, не доведена.
Післяопераційна ФП.
Хоча в двох відкритих дослідженнях лікування ПНЖК призвело до значного зниження частоти ФП після коронарного шунтування, ці результати не були підтверджені в подвійних сліпих, плацебо-контрольованих, рандомізованих контрольованих дослідженнях [166,167]. Тривалість ФП та госпіталізації не відрізнялася між групами.
Вторинна профілактика
Дані про ефективність ПНЖК у вторинній профілактиці ФП обмежені і суперечливі. В одному ретроспективному дослідженні застосування ПНЖК асоціювалося зі зниженням частоти рецидивів ФП після ізоляції легеневих вен. Попередні результати двох невеликих рандомізованих контрольованих досліджень показали, що лікування ПНЖК, розпочате за 1-4 тижні до кардіоверсії, не впливало на частоту рецидивів аритмії протягом від 6 місяців до 2 років. Проводиться кілька проспективних, рандомізованих клінічних досліджень. В даний час не можна дати якісь рекомендації з приводу застосування ПНЖК для первинної або вторинної профілактики ФП.
Рекомендації щодо первинної профілактики ФП за допомогою додаткових засобів
|
Рекомендації
|
Клас
|
Рівень
|
Джерело
|
|
Інгібітори АПФ і БРА можна застосовувати для первинної профілактики ФП у пацієнтів з серцевою недостатністю і зниженою фракцією викиду
|
IIa
|
A
|
145-149
|
|
Інгібітори АПФ і БРА можуть застосовуватися для первинної профілактики ФП у пацієнтів з артеріальною гіпертонією, особливо гіпертрофією ЛШ
|
IIa
|
B
|
147,150,151
|
|
Статини можна застосовувати для первинної профілактики ФП після аорто-коронарного шунтування (окремо або в комбінації з втручаннями на клапанах)
|
IIa
|
B
|
161,162
|
|
Статини можуть застосовуватися для первинної профілактики ФП у пацієнтів із захворюванням серця, особливо серцевою недостатністю
|
IIb
|
B
|
164,165
|
|
Лікування інгібіторами АПФ, БРА і статинами не рекомендується для первинної профілактики ФП у пацієнтів без серцево-судинних захворювань
|
III
|
C
|
|
Рекомендації щодо вторинної профілактики ФП за допомогою додаткових засобів
|
Рекомендації
|
Клас
|
Рівень
|
Джерело
|
|
Лікування інгібіторами АПФ і БРА можливо у пацієнтів з рецидивуючою ФП, які отримують антиаритмічну терапію
|
IIb
|
B
|
145-147, 152-153
|
|
БРА та інгібітори АПФ можуть застосовуватися для профілактики пароксизмальної ФП, а також у пацієнтів з персистуючою ФП без серйозного захворювання серця, яким проводиться електрична кардіоверсія, якщо є інші показання до призначення препаратів цих класів (наприклад, артеріальна гіпертонія)
|
IIb
|
B
|
145,155-156
|
5. Особливі групи
5.1 Серцева недостатність
Деякі механізми розвитку серцевої недостатності можуть сприяти появі ФП, оскільки вони створюють субстрат або тригер аритмії [44,168]. ФП – це потужний і незалежний фактор ризику серцевої недостатності. Ці стани часто поєднуються один з одним [44], частково внаслідок спільності факторів ризику. Розвиток ФП у пацієнта з серцевою недостатністю часто призводить до погіршення його стану, призводить до розвитку епізодів декомпенсації серцевої недостатності, збільшує ризик тромбоемболічних ускладнень і погіршує віддалений прогноз. При лікуванні пацієнтів з серцевою недостатністю та ФП слід враховувати наступні аспекти [44]: (1) Необхідно виявляти і по можливості усувати потенційні тригери і вторинні причини.
(2) Слід оптимізувати терапію серцевої недостатності.
Як і за інших станів, для контролю частоти шлуночкового ритму бажане застосування бета-блокаторів, а не серцевих глікозидів, оскільки перші знижують частоту серцевих скорочень не тільки в спокої, але і при фізичному навантаженні. Комбінація дигоксину і бета-блокатора може контролювати частоту шлуночкового ритму в спокої більш ефективно, ніж монотерапія.
Терапія бета-блокаторами окремо або в комбінації з дигоксином асоціювалася зі зниженням смертності у порівнянні з лікуванням одним дигоксином [169]. Бета-блокатори впливають на смертність і захворюваність у хворих на систолічну серцеву недостатність. Нещодавно під час мета-аналізу було виявлено зниження частоти розвитку ФП на 27% у пацієнтів з систолічною серцевою недостатністю, які отримували бета-блокатори [170].
Хоча дилтіазем ефективно зменшує частоту серцевих скорочень під час фізичного навантаження, він пригнічує скоротливість міокарда і збільшує ризик серцевої недостатності. Тим не менш, у пацієнтів з серцевою недостатністю та збереженою фракцією викиду дилтіазем в комбінації з дигоксином більш ефективно контролював частоту серцевих скорочень протягом 24 год і при навантаженні, ніж монотерапія дигоксином або недигідропіридиновим антагоністом кальцію.
Стратегія контролю ритму не мала переваг перед стратегією контролю частоти серцевих скорочень у пацієнтів з ФП [90]. Катетерна абляція лівого передсердя у хворих на серцеву недостатність може привести до поліпшення функції ЛШ, толерантності до фізичного навантаження та якості життя (див. Розділ 4.3.5.3) [93,94].
Профілактика тромбоемболій розглядається в розділі 4.1, однак серцева недостатність на фоні систолічної дисфункції сама по собі є чинником ризику інсульту і тромбоемболій, а за наявності ФП зазвичай показана терапія пероральними антикоагулянтами. Застосування аспірину в поєднанні з пероральними антикоагулянтами не рекомендується, враховуючи підвищений ризик кровотечі, а також наявні дані про підвищення частоти госпіталізацій з приводу серцевої недостатності при лікуванні аспірином.
Рекомендації щодо контролю частоти серцевих скорочень у пацієнтів з ФП і серцевою недостатністю
|
Рекомендації
|
Клас
|
Рівень
|
Джерело
|
|
Препаратами першої лінії для контролю частоти шлуночкового ритму у пацієнтів з серцевою недостатністю та низькою фракцією викиду є бета-блокатори
|
I
|
A
|
169,171
|
|
Якщо монотерапія не забезпечує адекватний контроль частоти серцевих скорочень, слід додати дигоксин
|
I
|
B
|
171,172
|
|
У гемодинамічно нестабільних хворих на гостру серцеву недостатність і низькою фракцією викиду лікування рекомендується починати з аміодарону
|
I
|
B
|
173
|
|
За відсутності додаткових провідних шляхів для контролю частоти серцевих скорочень у пацієнтів з ФП і гострою систолічною серцевою недостатністю альтернативою аміодарону є дигоксин
|
I
|
C
|
|
|
У пацієнтів з постійною ФП і показаннями до ресинхронізації серця (функціональний клас III-IV за NYHA, фракція викиду ≤35% і QRS≥130 мс) для контролю частоти серцевих скорочень може бути виконана абляція атріовентрикулярного вузла, якщо інші заходи не ефективні або протипоказані
|
IIa
|
B
|
105,109,110,174
|
|
Пацієнтам з серцевою недостатністю та збереженою фракцією викиду може бути призначений недигідропіридиновий антагоніст кальцію
|
IIb
|
C
|
|
|
Бета-блокатор може бути альтернативою недигідропіридиновому антагоністові кальцію у пацієнтів з серцевою недостатністю та збереженою фракцією викиду
|
IIb
|
C
|
|
|
Недигідропіридинові антагоністи кальцію не рекомендується застосовувати для контролю частоти серцевих скорочень у пацієнтів з систолічною серцевою недостатністю
|
III
|
C
|
|
Рекомендації щодо контролю ритму у пацієнтів з ФП і серцевою недостатністю
|
Рекомендації
|
Клас
|
Рівень
|
Джерело
|
|
Дефібриляція рекомендується пацієнтам з ФП, ішемією міокарда, що зберігається, гіпотонією і набряком легень, якщо висока частота шлуночкового ритму не знижується під впливом лікарських засобів
|
I
|
C
|
|
|
У пацієнтів з ФП і важкою серцевою недостатністю (функціональний клас III-IV за NYHA) або нестабільною серцевою недостатністю (≤4 тижнів) для утримання синусового ритму можна застосовувати тільки аміодарон
|
I
|
C
|
|
|
Застосування аміодарону доцільно для медикаментозної кардіоверсії або поліпшення результатів електричної кардіоверсії у пацієнтів з ФП
|
IIa
|
B
|
46,74,80,175
|
|
У пацієнтів з ФП і стабільною серцевою недостатністю (I-II функціональний клас за NYHA) для профілактики серцево-судинних госпіталізацій може застосовуватися дронадерон
|
IIa
|
C
|
|
|
У пацієнтів з серцевою недостатністю і персистуючою ФП, що супроводжується симптомами, які зберігаються незважаючи на адекватний контроль частоти серцевих скорочень, можливі електрична кардіоверсія і контроль ритму
|
IIb
|
B
|
90, 93,94, 97,176
|
|
Катетерна абляція (ізоляція легеневих вен) можлива у пацієнтів з серцевою недостатністю та рефрактерною ФП
|
IIb
|
B
|
93,94
|
Коментар робочої групи:
Покази до ресинхронізуючої терапії у пацієнтів з постійною формою фібриляції передсердь
Імплантація пристроя для кардіоресинхронізації показана пацієнтам з фібриляцією передсердь, які мають прояви застійної СН III та IV функциональний клас по NYHA, тривалість QRS> 120 мс та ФВ ЛШ <35% при умові, що бівентрикулярна стимуляція може бути досягнута у 100%. З метою досягнення 100% бівентрикулярної стимуляції таким пацієнтам виконують абляцію АВ-вузла. Також при недостатньому медикаментозному контролі ЧСС хворим з метою контролю ЧСС може бути запропонована комбінована терапія: Аблація АВ-вузла та імплантація CRT.
|
Рекомендації
|
Клас
|
Рівень
|
|
1.Паціенти з СН , широкими QRS, низькою ФВ
1А. CRT необхідно рекомендувати хворим з хронічною СН, тривалістю QRS> 120 мс та ФВ ЛШ <35%, котрі залишаються у III та амбулаторному IV функциональному класі по NYHA, незважаючи на адекватну медикаментозну терапію при умові, що бівентрикулярна стимуляція може бути досягнута у 100%.
|
IIa
|
B
|
|
1Б. Абляція AV-вузла має бути проведена у випадку непостійної бівентрикулярної стимуляції
|
IIa
|
B
|
|
2. Пацієнти з неконтролюємою частотою серцевих скорочень, котрі є кандидатами для абляції АВ – вузла.
CRT необхідно рорекомендувати у хворих зі зниженою ФВ ЛШ, котрим показана абляція АВ-вузла з метою контроля ЧСС.
|
IIa
|
B
|
Можливо проведення заміни ШВР на CRT пристрій у пацієнтів з симптомами СН, ФВ < 35% та високим відсотком шлуночкової стимуляції, у яких залишається III, IV ФК по NYHA незважаючи на адекватну медикаментозну терапію.
Алгоритм ведення хворих з серцевою недостатністю та постійною фібриляцією передсердь
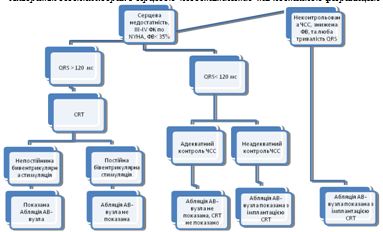
5.2 Спортсмени
У популяційних дослідженнях виявлена U-зворотна залежність між інтенсивністю фізичної активності і частотою розвитку ФП. Вона може свідчити про те, що позитивні антиаритмічні ефекти фізичних навантажень можуть нівелюватися при різкому збільшенні фізичної активності [177,178]. У професійних спортсменів, у тому числі колишніх, і людей, що активно займаються спортом, частота ФП збільшується в 2-10 разів [179,180]. Причини виявленої залежності, ймовірно, мають як функціональне (підвищення активності симпатичної системи, навантаження об'ємом при навантаженні, ваготонія в спокої), так і структурне (гіпертрофія і дилатація передсердь) походження. Роль препаратів, що збільшують активність пацієнта, не встановлена.
Домогтися зниження частоти серцевих скорочень до цільових значень у спортсменів важко. Бета-блокатори погано переносяться (або їх застосування навіть заборонено, якщо пацієнт бере участь у змаганнях з певних дисциплін), а дигоксин і недигідропіридинові антагоністи кальцію не здатні адекватно знизити частоту серцевих скорочень при ФП, пов'язаної з фізичним навантаженням. Якщо частота серцевих скорочень при нападі ФП є прийнятною для спортсмена, а гемодинамічні порушення відсутні (запаморочення, непритомність, раптова втома), то заняття спортом можна відновити. Призначати монотерапію блокаторами калієвих каналів для лікування ФП у спортсменів слід обережно [181]. Ці препарати можуть викликати розвиток тріпотіння передсердь з проведенням 1: 1 при високій активності симпатичної системи. Пацієнтам з тріпотінням передсердь може знадобитися абляція, після якої зазвичай доводиться продовжувати медикаментозну терапію («гібридна» терапія).
У деяких спортсменів з пароксизмальною ФП для невідкладного відновлення ритму можна застосовувати флекаїнід або пропафенон («таблетка в кишені»; див. Розділ 4.2.1.2.) [67]. Такі пацієнти не повинні займатися спортом доти, поки зберігається аритмія, і протягом 1-2 періодів напіввиведення антиаритмічного препарату. У деяких випадках можуть бути використані немедикаментозні методи лікування, наприклад, катетерна абляція [182].
Доцільність антикоагуляції визначають з урахуванням наявності факторів ризику тромбоемболічних ускладнень (див. Розділ 4.1). Однак антикоагулянтні препарати не можна застосовувати у спортсменів, якщо існує загроза травми.
Рекомендації щодо лікування ФП у спортсменів
|
Рекомендації
|
Клас
|
Рівень
|
Джерело
|
|
При застосуванні блокаторів натрієвих каналів для купіювання аритмії («таблетка в кишені») не слід займатися спортом, поки зберігається аритмія або протягом 1-2 періодів напіввиведення антиаритмічного препарату
|
IIa
|
C
|
|
|
Абляція гирла можлива у спортсменів з документованим тріпотінням передсердь, особливо якщо планується терапія флекаїнідом або пропафеноном
|
IIa
|
C
|
|
|
Для профілактики рецидивів ФП у спортсменів може бути проведена абляція
|
IIa
|
C
|
|
|
Якщо у спортсмена встановлена специфічна причина ФП (наприклад, гіпертиреоз), то до її усунення пацієнтові не рекомендується брати участь у змаганні або займатися спортом
|
III
|
C
|
|
|
За наявності ознак порушення гемодинаміки (наприклад, запаморочення) не рекомендується продовжувати займатися спортом
|
III
|
C
|
|
5.3 Вади клапанів серця
ФП часто розвивається у пацієнтів з вадами клапанів серця. Збільшення розміру лівого передсердя наголошується на ранньому етапі прогресуючої мітральної вади серця, а розвиток пароксизмальної або постійної ФП вважають показанням до раннього черезшкірного або хірургічного втручання на клапані [64]. ФП часто розвивається також на пізніх стадіях вади аортального клапана, коли дилатація ЛШ і збільшення кінцевого діастолічного тиску відображаються на функції лівого передсердя.
Лікування ФП у пацієнтів з вадою клапана серця проводять за стандартною схемою, хоча зазвичай віддають перевагу стратегії контролю частоти серцевих скорочень, враховуючи низьку ймовірність стійкого відновлення ритму. У пацієнтів з вадами клапанів серця є високий ризик розвитку тромбоемболій, тому «поріг» для призначення антикоагулянтів повинен бути низьким (розділ 4.1).
Рекомендації щодо лікування ФП у пацієнтів з вадою клапана серця
|
Рекомендації
|
Клас
|
Рівень
|
Джерело
|
|
Пацієнтам з мітральним стенозом і ФП (пароксизмальною, персистуючою або постійною) показана терапія пероральними антикоагулянтами (МНВ 2,0-3,0)
|
I
|
C
|
|
|
Пацієнтам з ФП і клінічно значущою мітральною регургітацією показана терапія пероральними антикоагулянтами (МНВ 2,0-3,0)
|
I
|
C
|
|
|
У випадку розвитку ФП пацієнтам з безсимптомним середньо-тяжким або тяжким мітральним стенозом може бути проведена черезшкірна балонна дилатація мітрального отвору, якщо відсутній тромб у лівому передсерді
|
IIa
|
C
|
|
|
Раннє оперативне втручання на мітральному клапані можливо у пацієнтів з тяжкою мітральною регургітацією, збереженою функцією ЛШ і знову виявленою ФП навіть за відсутності симптомів, особливо якщо може бути виконана реконструктивна операція
|
IIa
|
C
|
|
5.4 Гострий коронарний синдром
ФП розвивається у 2-21% пацієнтів з ГКС [49]. Широке застосування черезшкірних втручань на коронарних артеріях, особливо в гостру фазу, призвело до зниження частоти розвитку ФП. Лікування інгібіторами АПФ, БРА або бета-блокаторами, розпочате на ранньому етапі після інфаркту міокарда, також, ймовірно, сприяло зниженню частоти ФП [49]. ФП частіше розвивається у пацієнтів похилого віку, а також у хворих з серцевою недостатністю, більш високою частотою серцевих скорочень при надходженні і дисфункцією ЛШ. Її частота не залежить від типу реперфузійної терапії (тромболізис або черезшкірне втручання) [49]. ФП у хворих з ГКС асоціюється зі збільшенням госпітальної летальності та пізньої смертності та підвищенням ризику ішемічного інсульту під час госпіталізації і після виписки. Рекомендації з ведення пацієнтів з ГКС і ФП ґрунтуються переважно на думці експертів, так як відповідні клінічні дослідження не проводилися.
Пацієнтам з ГКС може бути проведена невідкладна електрична кардіоверсія, якщо ФП поєднується з рефрактерною ішемією або порушенням гемодинаміки. Для зменшення частоти серцевих скорочень і потреби міокарда в кисні внутрішньовенно вводять бета-блокатор або недигідропіридиновий антагоніст кальцію. Дигоксин та / або аміодарон внутрішньовенно можуть бути призначені пацієнтам з ГКС і тяжкою дисфункцією ЛШ і серцевою недостатністю. Інформацію про антикоагулянтну терапію у хворих з ФП і ГКС див. Розділ 4.1.
Рекомендації щодо лікування ФП у хворих з гострим коронарним синдромом
|
Рекомендації
|
Клас
|
Рівень
|
Джерело
|
|
Пацієнтам з ГКС і ФП слід провести дефібриляцію, якщо відзначаються тяжке порушення гемодинаміки або рефрактерна ішемія чи не вдається домогтися адекватного контролю частоти серцевих скорочень за допомогою лікарських засобів
|
I
|
C
|
|
|
Для уповільнення частого шлуночкового ритму у пацієнтів з ФП і ГКС рекомендується внутрішньовенне введення аміодарону
|
I
|
C
|
|
|
Для уповільнення частого желудочкового ритму у пацієнтів з ФП і ГКС рекомендується внутрішньовенне введення бета-блокаторів
|
I
|
C
|
|
|
Для уповільнення частого шлуночкового ритму у пацієнтів з ФП і ГКС можливо внутрішньовенне введення недигідропіридинових антагоністів кальцію (верапамілу, дилтіазему), якщо відсутні клінічні ознаки серцевої недостатності
|
IIa
|
C
|
|
|
Для уповільнення частого шлуночкового ритму у пацієнтів з ГКС і ФП, що супроводжується серцевою недостатністю, можливо внутрішньовенне введення дигоксину
|
IIb
|
C
|
|
|
Застосування флекаїніду або пропафенону у пацієнтів з ФП на тлі ГКС не рекомендується
|
III
|
B
|
124
|
5.5 Цукровий діабет
Цукровий діабет і ФП часто поєднуються один з одним, так як вони асоціюються з коронарною хворобою серця, артеріальною гіпертонією і дисфункцією ЛШ, а також дисфункцією вегетативної нервової системи та порушенням функції іонних каналів. За даними популяційних досліджень, частота цукрового діабету у хворих з ФП становить 13%. Цукровий діабет – це незалежний фактор ризику розвитку ФП (відносний ризик 1,4-1,8). Наявність цукрового діабету погіршує прогноз і збільшує ризик смерті і серцево-судинних захворювань. Доцільно забезпечувати контроль різних факторів ризику, в тому числі призначати антигіпертензивні засоби, статини і т.д. Важливе значення цукрового діабету відзначається в усіх схемах стратифікації ризику інсульту, а хворим на діабет рекомендується антитромботична терапія (див. Розділ 4.1).
Рекомендации по лечению ФП у больных сахарным диабетом
|
Рекомендації
|
Клас
|
Рівень
|
Джерело
|
|
Пацієнтам з ФП і цукровим діабетом рекомендується контроль всіх серцево-судинних факторів ризику, включаючи АТ, ліпіди та ін.
|
I
|
C
|
|
5.6 Літні люди
Поширеність ФП у пацієнтів у віці 80 років становить близько 10%, а у віці ≥85 років досягає 18%. У дослідженні SAFE, що проводилося в загальній практиці [43], було показано, що ефективними методами скринінгу ФП є огляд лікаря і виконання ЕКГ за наявності нерегулярного пульсу. У всіх пацієнтів у віці> 75 років щорічний ризик тромбоемболій перевищує 4%. У цьому випадку бажано призначати антагоністи вітаміну К, якщо ризик геморагічних ускладнень не надто високий. Серед окремих компонентів індексу CHADS2 вік ≥75 років асоціюється з більш високим ризиком інсульту і смерті в порівнянні з артеріальною гіпертонією, цукровим діабетом або серцевою недостатністю (див. Індекс CHA2DS2-VASc в розділі 4.1.1). В цілому переносимість антагоністів вітаміну К у літніх людей прийнятна [56]. У рандомізованих контрольованих дослідженнях застосування цих препаратів у хворих з ФП призводило до зниження частоти ішемічного інсульту і серцево-судинних ускладнень і супроводжувалося невеликим збільшенням ризику серйозних кровотеч. У зв'язку з цим антагоністи вітаміну К у літніх людей мали чіткі переваги перед аспірином. Навпаки, ефективність антитромбоцитарних засобів у профілактиці ішемічного інсульту з віком знижується і у віці 77 років відсутній (див. Розділ 4.1). Літнім людям рідко проводять електричну кардіоверсію, так як утримати синусовий ритм часто буває важко [183]. Для контролю частоти серцевих скорочень використовують бета-блокатори і недигідропіридинові антагоністи кальцію. Бета-блокатори слід застосовувати обережно у літніх пацієнтів з ХОЗЛ.
Літні пацієнти з ФП значно відрізняються від пацієнтів молодшого віку:
† Різні супутні захворювання, у тому числі серцево-судинної системи та інших органів.
† Висока захворюваність та поширеність ФП.
† Більш високий ризик тромбоемболічних ускладнень і кровотеч.
† ФП частіше постійна, а не рецидивируюча (пароксизмальна та / або персистуюча).
† Симптоми і скарги часто атипові.
† Частота шлуночкового ритму менш чутлива до дії симпатичної системи.
† Вища ймовірність аритмогенної дії ліків (зниження функції нирок і печінки).
† ФП частіше залишається недіагностованою.
Рекомендації щодо лікування ФП у літніх людей
|
Рекомендації
|
Клас
|
Рівень
|
Джерело
|
|
У всіх пацієнтів у віці 65 років і старше, які звертаються до лікарів загальної практики, слід проводити скринінг ФП (визначити пульс і зареєструвати ЕКГ за наявності аритмії)
|
I
|
В
|
|
5.7 Вагітність
У вагітних жінок без ФП і захворювання серця в анамнезі аритмія розвивається рідко. У пацієнток з раніше діагностованою ФП під час вагітності в 52% випадків розвиваються рецидиви аритмії; при цьому підвищується ризик ускладнень у плода. У пацієнток без вроджених або набутих вад серця ФП зазвичай добре переноситься під час вагітності.
Засоби, що уповільнюють серцевий ритм
Бета-блокатори проникають через плаценту і викликають різні небажані ефекти, включаючи затримку внутрішньоутробного розвитку, пригнічення функції системи дихання у новонародженого, брадикардію та гіпоглікемію, особливо якщо лікування починають на ранніх термінах вагітності (у перші 12-24 тижні). У дітей вагітних жінок з артеріальною гіпертонією, які отримували пропранолол, не було відзначено вроджених вад [184], проте спостерігалася затримка росту. Застосування атенололу протягом першого триместру, але не в більш пізні терміни, супроводжувалося затримкою росту плода. При мета-аналізі досліджень, в яких оцінювався ризик застосування бета-блокаторів у вагітних жінок з артеріальною гіпертонією, було виявлено прикордонне збільшення числа новонароджених з низьким ростом (по відношенню до терміну вагітності).
Дигоксин добре проникає через плаценту, а інтоксикація серцевими глікозидами у матері супроводжувалася смертю плоду. Досвід застосування верапамілу і дилтіазему обмежений, проте їх пероральне призначення для контролю частоти серцевих скорочень зазвичай безпечне.
Відновлення синусового ритму
Флекаїнід застосовували для купіювання аритмій у плода; при цьому він не викликав небажаних ефектів. Аміодарон чинив негативний вплив на плід, тому його можна призначати вагітним жінкам тільки у невідкладних ситуаціях. Призначення будь-яких ліків слід по можливості уникати в першому триместрі вагітності, коли відбувається органогенез.
електрична кардіоверсія
Описано декілька випадків успішної електричної кардіоверсії у вагітних жінок з ФП. Небажаних ефектів у плода при цьому не виявили. Енергія розряду порівнянна у вагітних і невагітних жінок.
Антикоагуляція
Антагоністи вітаміну К чинять тератогенну дію, тому в першому триместрі їх зазвичай заміняють на НФГ або НМГ [185]. За даними одного систематизованого огляду, вроджені вади відзначалися в 6,4% випадків, коли варфарин застосовували протягом всієї вагітності, і були відсутні, коли його замінювали на гепарин на 6-12-му тижнях вагітності. Варфарин легко проникає через плаценту, а у плода може спостерігатися передозування навіть при терапевтичному значенні МНВ у жінки.
НМГ не проходять через плаценту і широко застосовувалися для лікування і профілактики венозних тромбоемболічних ускладнень під час вагітності. Вони не чинили негативний вплив на плід. У третьому триместрі необхідно регулярно проводити лабораторні тести (кожні 10-14 днів), щоб забезпечити адекватну антикоагуляцію. За необхідності слід коригувати дозу. У деяких жінок для збереження адекватного антикоагулянтного ефекту можуть знадобитися високі дози антагоністів вітаміну К і гепарину.
Якщо вагітна жінка з ФП і штучним клапаном серця припиняє прийом антагоністів вітаміну К на 6-12-му тижнях вагітності, то їй слід проводити постійну інфузію НФГ, вводити НФГ в підібраній дозі або НМН підшкірно. Лікування антагоністами вітаміну К може бути відновлено в другому триместрі.
Рекомендації щодо лікування ФП у вагітних жінок
|
Рекомендації
|
Клас
|
Рівень
|
Джерело
|
|
Дефібриляція безпечна у всіх триместрах вагітності. Вона рекомендується при нестабільній гемодинаміці на тлі ФП і високому ризику, пов'язаному з аритмією, для матері або плода
|
I
|
C
|
|
|
Пацієнткам з ФП і високим ризиком тромбоемболій рекомендується антитромботична профілактика протягом всієї вагітності. Препарат (гепарин або варфарин) вибирають з урахуванням триместру вагітності
|
I
|
C
|
|
|
Пероральні антагоністи вітаміну К рекомендується застосовувати з II триместру вагітності. Їх скасовують за 1 міс до передбачуваних пологів
|
I
|
C
|
|
|
Підшкірне введення НМГ в терапевтичних дозах рекомендується протягом першого триместру і останнього місяця вагітності. Альтернативою може бути НФГ (слід домогтися збільшення активованого часткового тромбопластинового часу в 1,5 рази в порівнянні з контролем)
|
I
|
B
|
185
|
|
Для контролю частоти серцевих скорочень слід застосовувати бета-блокатори або недигідропіридинові антагоністи кальцію. Протягом першого триместру вагітності слід зважувати користь бета-блокаторів та потенційний ризик для плоду
|
IIa
|
C
|
|
|
Для купіювання нещодавно розвиненого нападу ФП (якщо необхідне відновлення синусового ритму, а дефібриляція не обгрунтована) у пацієнтів зі стабільною гемодинамікою, які не страждають на захворювання серця, можна ввести внутрішньовенно флекаїнід або ібутилід
|
IIb
|
C
|
|
|
Якщо показаний контроль частоти серцевих скорочень, а бета-блокатори або недигідропіридинові антагоністи кальцію протипоказані, можливе призначення дигоксину
|
IIb
|
C
|
|
5.8 Післяопераційна фібриляція передсердь
ФП – це найчастіше ускладнення після операцій на серці (30% – після аорто-коронарного шунтування [АКШ], 40% – після операцій на клапанах серця і 50% – після АКШ / операції на клапані серця). Частота її досягає піку на 2-4-й день після операції. За даними аналізу 58 досліджень в цілому у 8565 пацієнтів, було показано, що профілактика та / або лікування післяопераційної ФП бета-блокаторами, соталолом або аміодароном, а також передсердна стимуляція (користь її доведена менш переконливо) знижують ризик несприятливих результатів (ФП, інсульт і тривалість госпіталізації) (ВР 0.43; 95% ДІ 0.37-0.51) [186].
Профілактика післяопераційної фібриляції передсердь
Бета-блокатори найбільш ефективні, якщо їх застосовувати до і після операції на серці (ніж тільки до або після операції) [186,187,196]. Скасування бета-блокатора – це фактор ризику розвитку післяопераційної ФП, тому його слід уникати. Принаймні за 1 тиждень до втручання слід почати лікування бета1-адреноблокатором, що не має власної активності.
Профілактичне застосування аміодарону призвело до значного зниження частоти післяопераційної ФП (ВР 0.50; 95% ДІ 0.42-0.59) і скорочення тривалості госпіталізації, а також зниження частоти інсульту і післяопераційних шлуночкових тахіаритмій, але не післяопераційної смертності [188]. Частота ФП у групі аміодарону була нижчою, ніж у групі плацебо (ВР 0.52; 95% ДІ 0.34-0.69), у тому числі у пацієнтів віком <65 років і ≥65 років, хворих, які перенесли АКШ або операцію на клапані сердця АКШ , пацієнтів, які отримували і не отримували бета-блокатори перед операцією. Небажані ефекти періопераційного профілактичного внутрішньовенного введення аміодарону включають розвиток брадикардії і гіпотонії після втручання [189]. При мета-аналізі 14 рандомізованих контрольованих досліджень не був підтверджений зв'язок між зниженням ризику розвитку ФП після операції і сумарною дозою аміодарону [190]. Сприятливий ефект аміодарону був також підтверджений результатами іншого мета-аналізу [186].
Соталол знижував частоту післяопераційної ФП на 64% в порівнянні з плацебо, проте він не впливав на тривалість госпіталізації, ризик інсульту або смертність [186]. Застосування соталолу підвищує ризик розвитку брадикардії і шлуночкової тахікардії типу пірует, особливо за наявності електролітних порушень, тому в хірургічній практиці його застосовують рідко.
Гіпомагніємія – це незалежний фактор ризику післяопераційної ФП. При мета-аналізі 20 рандомізованих досліджень у 2490 пацієнтів було показано, що профілактичне внутрішньовенне введення магнію знижує ймовірність розвитку післяопераційної ФП (ВР 0.54; 95% ДІ 0.38-0.75) [191]. Клінічне значення цього методу лікування недостатньо добре вивчено.
Застосування статинів супроводжується зниженням ризику післяопераційної ФП на 22-34% (див. Розділ 4.4).
У декількох ретроспективних дослідженнях інгібітори АПФ і БРА не чинили вплив на частоту ФП після операцій на серці. Крім того, при їх застосуванні існує ризик погіршення функції нирок на ранніх термінах після операції.
Кортикостероїди володіють потужними протизапальними властивостями. Їх ефективність у профілактиці ФП вивчалася в кардіоторакальної хірургії. За даними мета-аналізу, кортикостероїдна терапія супроводжувалася зниженням частоти післяопераційної ФП на 26-45% і тривалості госпіталізації [192]. Ефект був більш вираженим у пацієнтів, які отримували середні дози (50-210 мг дексаметазону), ніж у хворих, яким призначали більш низькі або високі дози. Враховуючи можливий несприятливий вплив кортикостероїдів на метаболізм глюкози, загоєння рани і ризик інфекцій, їх застосування для профілактики ФП представляється спірним.
При мета-аналізі 8 досліджень було показано, що профілактична стимуляція передсердь знижує частоту післяопераційної ФП незалежно від типу або алгоритму стимуляції (ВР 0.57; 95% ДІ 0.38-0.84; P <0.005) [186], однак в інших дослідженнях не була підтверджена ефективність цього методу [193]. Неадекватна стимуляція може підвищити ймовірність розвитку ФП.
Інші засоби
У невеликих дослідженнях вивчалися також дигоксин, верапаміл, дилтіазем і напроксен. Отримані результати були суперечливими.
Лікування післяопераційної фібриляції передсердь
У більшості пацієнтів зі стабільною гемодинамікою синусовий ритм відновлюється спонтанно протягом 24 год. У першу чергу слід, по можливості, усунути сприятливі фактори (знеболювання, поліпшення гемодинаміки, скасування внутрішньовенних засобів інотропної дії, корекція електролітних і метаболічних порушень, анемії та гіпоксії) [194].
За наявності виражених симптомів або неможливості адекватного контролю частоти серцевих скорочень може бути виконана кардіоверсія. Дефібриляція ефективна в 95% випадків, однак частіше проводять медикаментозну кардіоверсію. Аміодарон і ібутилід за ефективністю перевершували плацебо у пацієнтів з післяопераційною ФП (розділ 4.2.1.3).
Коротко діючі бета-блокатори (наприклад есмолол) особливо корисні при нестабільній гемодинаміці. Можуть застосовуватися також інші засоби, що блокують атріовентрикулярний вузол, такі як недигідропіридинові антагоністи кальцію, однак дигоксин менш ефективний на тлі високого тонусу адренергічної системи.
Препарати, які застосовують для контролю частоти серцевих скорочень у хворих з післяопераційною ФП, перераховані в табл. 15.
У ряді досліджень було відзначено збільшення ризику інсульту після операцій на серці. Антикоагуляція гепарином або антагоністами вітаміну К обгрунтована, якщо ФП зберігається більше 48 год [195]. Перед кардіоверсією слід дотримуватися стандартних запобіжних заходів, що стосуються антикоагуляції (див. Розділ 4.1).
Рекомендації щодо лікування післяопераційної ФП
|
Рекомендації
|
Клас
|
Рівень
|
Джерело
|
|
Для профілактики ФП після операцій на серці рекомендується призначати бета-блокатори перорально за відсутності протипоказань
|
I
|
А
|
186,187
|
|
У пацієнтів, які отримують бета-блокатори (або інші пероральні антиаритмічні препарати для контролю ФП), лікування рекомендується продовжувати до дня операції
|
I
|
B
|
187,196
|
|
Пацієнтам з ФП без порушень гемодинаміки рекомендується контроль частоти шлуночкового ритму
|
I
|
B
|
196
|
|
У пацієнтів з післяопераційною ФП і нестабільною гемодинамікою рекомендується відновлення синусового ритму шляхом дефібриляції
|
I
|
C
|
|
|
У пацієнтів з високим ризиком післяопераційної ФП можливо профілактичне застосування аміодарону перед операцією
|
IIa
|
A
|
186-188
|
|
Якщо післяопераційна ФП зберігається ≥48 год, то за відсутності протипоказань показана антитромботична / антикоагуляційної терапія
|
IIa
|
A
|
195
|
|
Якщо відновлений синусовий ритм, то антикоагуляцію слід продовжувати протягом принаймні 4-х тижнів або триваліше за наявності факторів ризику інсульту
|
IIa
|
B
|
195
|
|
З метою відновлення синусового ритму у пацієнтів з рецидивуючою або рефрактерною післяопераційною ФП доцільне застосування антиаритмічних препаратів
|
IIa
|
C
|
|
|
Для профілактики ФП після операцій на серці може застосовуватися соталол, хоча він може чинити аритмогенну дію
|
IIb
|
A
|
186
|
|
Для профілактики ФП після операцій на серці може проводитися біатріальна стимуляція
|
IIb
|
A
|
186
|
|
Для зниження частоти ФП після операцій на серці можуть застосовуватися кортикостероїди, проте вони можуть викликати небажані ефекти
|
IIb
|
B
|
192
|
5.9 Гіпертиреоз
ФП розвивається у 10-25% хворих гіпертиреозом, особливо у чоловіків і літніх людей. Основна мета лікування – відновлення нормальної функції щитовидної залози, яке може супроводжуватися спонтанним відновленням ритму. Якщо обрана стратегія контролю ритму, то перед кардіоверсією слід нормалізувати функцію щитовидної залози, щоб знизити ризик розвитку рецидивів аритмії. Антиаритмічні засоби і дефібриляція зазвичай неефективні при збереженні тиреотоксикозу.
Бета-блокатори можуть ефективно знизити частоту серцевих скорочень, а в разі тиреоїдного шторму можливо їх внутрішньовенне введення. Альтернативою можуть служити недигідропіридинові антагоністи кальцію, такі як дилтіазем і верапаміл.
Незважаючи на відсутність результатів клінічних досліджень за наявності факторів ризику інсульту рекомендується антикоагулянтна терапія для профілактики системних емболій. Залишається неясним, підвищений ризик тромбоемболій у пацієнтів з ФП, що асоціюється з тиреотоксикозом в анамнезі (лікованим), за відсутності факторів ризику.
У клінічній практиці часто відзначається розвиток гіпертиреозу (а також безсимптомних змін показників функції щитовидної залози) після лікування аміодароном. Виділяють два варіанти гіпертиреозу, спричиненого аміодароном: I типу (підвищена продукція Т4 і Т3, викликана йодом) і II типу (деструктивний тиреоїдит, що супроводжується минущим виділенням Т4 і Т3 з подальшим зниженням функції щитовидної залози). Хоча лікування аміодароном може бути продовжено на тлі ефективної замісної терапії гормонами щитовидної залози, у разі розвитку гіпертиреозу його слід відзначити. Тиреотоксикоз може також розвинутися після відміни аміодарону.
Рекомендації щодо лікування ФП у хворих на гіпертиреоз
|
Рекомендації
|
Клас
|
Рівень
|
Джерело
|
|
Пацієнтам з активним захворюванням щитовидної залози рекомендується антитромботична терапія з урахуванням наявності інших факторів ризику інсульту
|
I
|
C
|
|
|
Для контролю частоти шлуночкового ритму у пацієнтів з ФП на тлі тиреотоксикозу рекомендується застосування бета-блокаторів за відсутності протипоказань
|
I
|
C
|
|
|
Якщо застосування бета-блокатора неможливо, для контролю частоти серцевих скорочень у пацієнтів з ФП і тиреотоксикозом рекомендується призначення недигідропіридинового антагоніста кальцію (дилтіазема або верапамілу)
|
I
|
C
|
|
|
Якщо бажаний контроль ритму, то перед кардіоверсією необхідно нормалізувати функцію щитовидної залози, інакше велика ймовірність рецидиву
|
I
|
C
|
|
|
Після нормалізації функції щитовидної залози рекомендації з антитромботичної профілактики відповідають таким у пацієнтів без гіпертиреозу
|
I
|
C
|
|
5.10 Синдром Вольффа-Паркінсона-Уайта
На відміну від атріовентрикулярного вузла, більшість додаткових провідних шляхів не затримують проведення електричних імпульсів, тому у пацієнтів з синдромом передчасного збудження і ФП існує загроза швидкого проведення імпульсів через додаткові пучки, що може призвести до розвитку тахікардії і раптової серцевої смерті внаслідок фібриляції шлуночків. Відповідно, у цієї категорії пацієнтів ФП розглядається як загрозлива для життя аритмія. Інформацію щодо медикаментозні контролі частоти серцевих скорочень у пацієнтів з додатковими провідними шляхами див. Розділ 4.3.3.
Раптова смерть і стратифікація ризику
Частота раптової серцевої смерті у пацієнтів з синдромом Вольффа-Паркінсона-Уайта становить від 0,15 до 0,39% протягом 3-22 років. Виділяють ряд факторів ризику раптової смерті: мінімальна тривалість інтервалу RR <250 мс при спонтанній або індукованій ФП, клінічно явна тахікардія в анамнезі, наявність множинних додаткових шляхів проведення і аномалія Ебштейна.
Надшлуночкові аритмії, такі як передсердна тахікардія або тріпотіння передсердь, у пацієнтів з додатковими провідними шляхами можуть супроводжуватися проведенням 1: 1, що призводить до швидкої активації шлуночків і розвитку фібриляції шлуночків.
Ефективність катетерної абляції додаткових шляхів становить близько 95%, тому це втручання вважають методом вибору [30]. Пацієнтам, які перенесли раптову серцеву смерть, необхідно провести невідкладну абляцію. Успішна катетерна абляція дозволяє усунути ризик раптової серцевої смерті, тому після втручання імплантація кардіовертера-дефібрилятора не потрібна. Доцільність абляції слід обговорювати у пацієнтів з явним синдромом передчасного збудження і високим ризиком ФП, а також у представників небезпечних професій, таких як водії громадського транспорту, пілоти або професійні спортсмени.
Показання до катетерної абляції додаткових провідних шляхів за відсутності клінічних симптомів залишаються спірними (особливо у дітей) [197]. У більшості пацієнтів з безсимптомним синдромом передчасного збудження прогноз сприятливий; раптова серцева смерть рідко виявляється першим проявом захворювання. Приблизно у 20% таких пацієнтів спостерігається частий шлуночковий ритм при ФП, індукованої під час електрофізіологічного тестування. У динаміці в окремих пацієнтів розвиваються клінічно явні аритмії або раптова серцева смерть.
Передбачуване значення позитивних результатів інвазивного електрофізіологічного тесту вважають низьким і недостатнім для широкого застосування цієї проби за відсутності клінічної симптоматики. Рішення про катетерну абляцію додаткових провідних шляхів при безсимптомному перебігу синдрому передчасного збудження слід приймати індивідуально після детального обговорення з хворим (і його родичами) природного перебігу захворювання та ризику раптової серцевої смерті в порівнянні з ускладненнями самої абляції.
Рекомендації щодо лікування ФП у пацієнтів з синдромом Вольффа-Паркінсона-Уайта
|
Рекомендації
|
Клас
|
Рівень
|
Джерело
|
|
Для профілактики раптової серцевої смерті у пацієнтів з ФП рекомендується катетерна абляція додаткових провідних шляхів
|
I
|
A
|
30
|
|
Після перенесеної раптової серцевої смерті пацієнтів з проведенням додатковими пучками необхідно негайно направити до спеціалізованого центру для катетерної абляції
|
I
|
C
|
|
|
Представникам ризикованих професій (пілоти, водії громадського транспорту), у яких на ЕКГ визначаються ознаки проведення додатковими шляхами, рекомендується катетерна абляція
|
I
|
B
|
30
|
|
Пацієнтам з безсимптомним проведенням додатковими шляхами і високим ризиком розвитку ФП показана катетерна абляція
|
I
|
B
|
198
|
|
За відсутності симптомів катетерна абляція додаткових провідних шляхів може бути виконана тільки після обговорення з пацієнтом користі і ризику втручання
|
IIa
|
B
|
198
|
5.11 Гіпертрофічна кардіоміопатія
У пацієнтів з гіпертрофічною кардіоміопатією (ГКМП) ризик розвитку ФП вище, ніж у загальній популяції (близько 20-25%; щорічна захворюваність 2%). ФП викликає погіршення перебігу ГКМП. За відсутності тромбу в лівому передсерді пацієнтам з гострим нападом ФП показана електрична чи медикаментозна кардіоверсія. Найбільш ефективним засобом профілактики пароксизмальної ФП і рецидивів аритмії вважають аміодарон. Ефективність дронедарона не встановлена. Дизопірамід в поєднанні з бета-блокатором викликає зниження градієнта тиску в виносному тракті лівого шлуночка. При хронічній ФП для контролю частоти серцевих скорочень зазвичай застосовують бета-блокатори і верапаміл. В окремих випадках обгрунтована абляція атріовентрикулярного вузла та імплантація постійного водія ритму. За відсутності протипоказань хворим на ГКМП і пароксизмальну, персистуючу або постійну ФП показана терапія пероральними антикоагулянтами.
Результати абляції ФП у хворих на ГКМП сприятливі, проте втручання менш ефективне, ніж у загальній популяції пацієнтів з ФП. Абляція лівого передсердя при пароксизмальній ФП значно більш ефективна, ніж при персистуючій аритмії. Ризик рецидиву високий у пацієнтів з вираженою дилатацією передсердь і важкою дистолічною дисфункцією. Частота відновлення синусового ритму після радіочастотної катетерної абляції у пацієнтів з ГКМП і рефрактерною ФП, що зберігається незважаючи на лікування різними антиаритмічними препаратами, включаючи аміодарон, склала 67%. Втручання призвело до значного поліпшення функціонального класу за NYHA протягом 3-х років.
Досвід хірургічної абляції у пацієнтів з ГКМП обмежений. У найбільшій серії 10 пацієнтів перенесли операцію лабіринт-III у поєднанні з міоектомією за наявності обструкції вихідного тракту ЛШ. Збільшення післяопераційної летальності відзначено не було. Протягом в середньому 15 місяців у значної частки пацієнтів зберігався синусовий ритм [199]. Хоча наявні дані суперечливі, міоектомія в цілому дає сприятливий ефект у хворих на ГКМП.
Рішення про імплантації кардіовертера-дефібрилятора хворим на ФП слід приймати обережно, враховуючи більш високий ризик помилкового спрацьовування приладу, особливо протягом першого року після втручання.
Рекомендації щодо лікування ФП у хворих на гіпертрофічну кардіоміопатію
|
Рекомендації
|
Клас
|
Рівень
|
Джерело
|
|
Пацієнтам з ГКМП і з нещодавно розвинутою ФП рекомендується електрична чи медикаментозна кардіоверсія
|
I
|
B
|
200
|
|
За відсутності протипоказань пацієнтам з ГКМП і ФП рекомендується терапія пероральними антикоагулянтами (МНВ 2,0-3,0)
|
I
|
B
|
200
|
|
Для відновлення та контролю синусового ритму у пацієнтів з ГКМП рекомендується застосування аміодарону (або дизопіраміду у поєднанні з бета-блокатором)
|
IIa
|
C
|
|
|
Якщо ФП рефрактерна до лікарських засобів, можлива катетерна абляція
|
IIa
|
C
|
|
|
Пацієнтам з ГКМП і рефрактерною ФП може бути виконана абляція (у поєднанні з міоектомією перегородки за наявності показань)
|
IIa
|
C
|
|
5.12 Захворювання легень
ФП часто зустрічається у хворих з хронічними захворюваннями легень і має несприятливе прогностичне значення (розвиток гіпоксії на тлі загострень). Ключове значення мають лікування захворювання легенів і корекція метаболічних порушень, так як антиаритмічні засоби і електрична кардіоверсія зазвичай не ефективні при збереженні порушеної функції легень. При важкій ХОЗЛ часто розвивається мульфокальна передсердна тахікардія, яку можна сплутати з ФП.
Бронходилататори, особливо теофілін і агоністи бета-блокатори, можуть спровокувати розвиток ФП; контролювати частоту шлуночкового ритму в таких випадках буває важко. Неселективні бета-блокатори, соталол, пропафенон і аденозин протипоказані хворим з бронхоспазмом, тому бажано призначення недигідропіридинових антагоністів кальцію. Селективні бета 1 адреноблокатори (наприклад бісопролол) в невеликих дозах часто добре переносяться і ефективні. Для відновлення синусового ритму можна внутрішньовенно ввести флекаїнід. За наявності порушень гемодинаміки показана електрична кардіоверсія. У рефрактерних випадках для контролю частоти шлуночкового ритму можуть знадобитися абляція атріовентрикулярного вузла і стимуляція шлуночків.
Рекомендації щодо лікування ФП у піцієнтів із захворюванням легень
|
Рекомендації
|
Клас
|
Рівень
|
Джерело
|
|
У пацієнтів з ФП, що розвинулася на тлі гострого захворювання легенів або загострення хронічної хвороби легенів, лікування слід починати з корекції гіпоксемії і ацидозу
|
I
|
C
|
|
|
Якщо у хворого із захворюванням легенів ФП викликає порушення гемодинаміки, слід провести дефібриляцію
|
I
|
C
|
|
|
Для контролю частоти шлуночкового ритму у пацієнтів з обструктивними захворюваннями легень застосовують недигідропіридинові антагоністи кальцію (дилтіазем або верапаміл)
|
IIa
|
C
|
|
|
В якості альтернативи для контролю частоти серцевих скорочень можна застосовувати селективні бета 1 адреноблокатори (наприклад бісопролол) в невеликих дозах
|
IIa
|
C
|
|
|
Пацієнтам з бронхоспастичним синдромом, у яких розвивається ФП, не рекомендується призначати теофілін і бета-адреноміметики
|
III
|
C
|
|
|
Неселективні бета-блокатори, соталол, пропафенон і аденозин не рекомендується призначати пацієнтам з обструктивними захворюваннями легень, у яких розвивається ФП
|
III
|
C
|
|
Коментар робочої групи:
5.13.Застосування нових пероральних антикоагулянтів або антагоністів вітаміну К у пацієнтів з фібриляцією передсердь та злоякісними пухлинами
Як і фібриляція передсердь, багато видів раку виникає у пацієнтів літнього віку. На відміну від профілактики венозної тромбоемболії, існує обмежена кількість даних контрольованих досліджень антитромботичної терапії у пацієнтів з фібриляцією передсердь та злоякісними пухлинами. Злоякісна пухлина у стадії загострення звичайно була критерієм виключення із досліджень НПАК при ФП. Незважаючи на наявність деякої кількості пацієнтів, хворих на рак, у клінічних дослідженнях фази 3 було неможливо здійснити аналіз у підгрупах через відсутність інформації щодо типу та стадії раку. Протитромботична терапія у пацієнтів із фібриляцією передсердь та злоякісною пухлиною потребує узгодження дій між кардіологом та онкологом. Слід враховувати вплив раку на перебіг захворювання та смертність, методику лікування раку та очікуваний вплив пухлини та терапії на ризик розвитку тромбоемболічних явищ і виникнення кровотечі.
Пацієнти із злоякісними пухлинами мають підвищений ризик розвитку тромбоемболічних явищ
Багато форм раку прямо або опосередковано впливають на систему згортання крові. Деякі пухлини виділяють протромботичні фактори, а інші спричиняють запальні реакції за рахунок гуморальних факторів імунного захисту або прямо взаємодіючи з імунною системою. Застосування антикоагулянтної терапії може бути виправданим через зростання ризику розвитку тромбоемболії.
Лікування раку може підвищувати ризик виникнення кровотечі.
Кожна форма лікування раку: операція, променева або хіміотерапія може спричинити місцеву кровотечу з ран (при операції), пошкодження тканин (при променевій терапії) або системні антипроліферативні ефекти, що знижують кількість і функцію тромбоцитів (при хіміотерапії та деяких формах променевої терапії). Крім того, багато видів злоякісних пухлин пов'язані з ризиком кровотеч із слизової оболонки, наприклад, бронхіальна карцинома, урогенітальні кровотечі, рак голови та шиї. Основний ризик кровотечі, спричиненої застосуванням хіміотерапії, опосередкований мієлосупресивним ефектом терапії, що визначається кількістю тромбоцитів. Зазвичай, виражені мієлосупресивні ефекти виражаються у вигляді лейкопенії <1000 × 109/л та кількості тромбоцитів <50 × 109/л. Деякі види хіміотерапії можуть прямо впливати на тромбоцитарну функцію або систему коагуляції крові. Цього слід уникати. В подальшому, мієлосупресія зменшує кількість еритроцитів та знижує коефіцієнт безпеки у випадку виникнення кровотечі. Ступінь мієлосупресії суттєво змінюється залежно від терапії від легкої форми до затяжних періодів майже повної аплазії. Онкологи можуть найкращим чином визначити побічні реакції з боку системи згортання крові, пов’язані із спеціальною запланованою терапією. Незважаючи на це, взаємодія НПАК та специфічних хіміотерапевтичних засобів ще недостатньо вивчена і тому вимагає обережності.
Практичні рекомендації
Пацієнти із злоякісними пухлинами та фібриляцією передсердь потребують багатопланового догляду з боку кардіологів та онкологів, у тому числі ретельне планування протитромботичної терапії.
У разі необхідності у антикоагулянтній терапії для пацієнтів зі злоякісними пухлинами, перевагу слід надати лікуванню антагоністами вітаміну К або гепарином у зв'язку з наявністю достатнього клінічного досвіду лікування цими препаратами, з можливістю здійснення пильного моніторингу та здатністю до усунення симптомів.
Наявність злоякісних пухлин у пацієнтів з фібриляцією передсердь підвищує ризик інсульту. У зв'язку з цим за можливості, слід продовжити лікування антикоагулянтами, у тому числі НПАК.
На основі даних щодо пацієнтів з венозною емболією, терапія НПАК при дозовому режимі, необхідному для лікування фібриляції передсердь, також може попередити розвиток венозної емболії. Таким чином, при застосуванні НПАК немає потреби у додатковій антикоагулянтній терапії (наприклад, терапії низькомолекулярним гепарином).
У багатьох пацієнтів, що мають злоякісні пухлини та отримують терапію з помірним мієлосупресивним впливом, доцільним є продовження лікування НПАК.
До пацієнтів, що мають злоякісні пухлини та отримують НПАК і потребують хірургічного видалення пухлини, застосовуються ті ж принципи лікування, що й для пацієнтів, які потребують планового хірургічного втручання.
Пацієнтам, що отримують променеву терапію або хіміотерапію без вираженого мієлосупресивного впливу, слід продовжити лікування НПАК, за умови пристосування доз до очікуваних від лікування змін у функціях органів (особливо печінки та нирок).
При призначенні мієлосупресивної хіміотерапії та променевої терапії, багатопрофільна бригада лікарів, у тому числі кардіологи та онкологи повинні розглянути необхідність тимчасового зменшення дози або призупинки терапії НПАК. Слід розглянути доцільність особливих форм моніторингу, у тому числі:
(a) Проведення періодичних аналізів крові, включаючи підрахунок кількості тромбоцитів.
(б) Ретельне обстеження щодо симптомів кровотечі.
(в) Регулярний моніторинг функції печінки та нирок.
Для всіх пацієнтів, що отримують лікування антикоагулянтами, слід розглянути доцільність захисту шлунку за допомогою ІПП або блокаторів Н2-рецепторів.
Пацієнтів, що мають злоякісні новоутворення, слід повідомити про необхідність контролю симптомів кровотечі (петехійний крововилив, кровохаркання, чорний стул) та звернення до лікаря у разі виникнення цих симптомів.